Cho kẽm dư tác dụng với 100 ml dung dịch HCl 5M. Thu được V lít khí.(đktc) - Tính C% của dung dịch sau phản ứng.
Câu 3. Cho 1 lượng kẽm (Zn) dư tác dụng với 100 ml dung dịch axit HCI, phản ứng kết thúc thu được 6,72 lít khí (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính khối lượng kẽm đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
c, \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,1}=6\left(M\right)\)
Có 500 ml dung dịch X chứa Na + , NH 4 + , CO 3 2 - và SO 4 2 - . Lấy 100 ml dung dịch X tác dụng với lượng dư dung dịch HCl thu được 2,24 lít khí. Lấy 100 ml dung dịch X cho tác dụng với lượng dư dung dịch BaCl2 thu được 43 gam kết tủa. Lấy 200 ml dung dịch X tác dụng với lượng dư dung dịch NaOH thu được 8,96 lít khí NH 3 . Các phản ứng hoàn toàn, các thể tích khí đều đo ở đktc. Tính tổng khối lượng muối có trong 300 ml dung dịch X?
A. 23,8 gam.
B. 86,2 gam.
C. 71,4 gam.
D. 119,0 gam.
Có 500 ml dung dịch X chứa Na+, NH4+, CO32– và SO42–. Lấy 100 ml dung dịch X tác dụng với lượng dư dung dịch HCl thu được 2,24 lít khí. Lấy 100 ml dung dịch X cho tác dụng với lượng dư dung dịch BaCl2 thu được 43 gam kết tủa. Lấy 200 ml dung dịch X tác dụng với lượng dư dung dịch NaOH thu được 8,96 lít khí NH3. Các phản ứng hoàn toàn, các thể tích khí đều đo ở đktc. Tính tổng khối lượng muối có trong 300 ml dung dịch X ?
A. 23,8 gam.
B. 86,2 gam.
C. 71,4 gam.
D. 119,0 gam.
Chọn đáp án C
Xét trong 100 ml dung dịch X: 2H⁺ + CO32– → CO2 + H2O ⇒ nCO32– = nkhí = 0,1 mol.
Ba2+ + CO32– → BaCO3 || Ba2+ + SO42– → BaSO4 ⇒ nSO42– = (43 - 0,1 × 197) ÷ 233 = 0,1 mol.
NH4+ + OH– → NH3 + H2O ⇒ nNH4+ = nNH3 = 0,4 ÷ 2 = 0,2 mol.Bảo toàn điện tích: nNa+ = 0,2 mol.
⇒ mmuối trong 300ml X = 3 × (0,2 × 23 + 0,2 × 18 + 0,1 × 60 + 0,1 × 96) = 71,4(g) ⇒ chọn C.
Có 500 ml dung dịch X chứa Na + , NH 4 + , CO 3 2 - và SO 4 2 - . Lấy 100 ml dung dịch X tác dụng với lượng dư dung dịch HCl thu được 2,24 lít khí. Lấy 100 ml dung dịch X cho tác dụng với lượng dư dung dịch BaCl 2 thu được 43 gam kết tủa. Lấy 200 ml dung dịch X tác dụng với lượng dư dung dịch NaOH thu được 8,96 lít khí NH 3 . Các phản ứng hoàn toàn, các thể tích khí đều đo ở đktc. Tính tổng khối lượng muối có trong 300 ml dung dịch X ?
A. 23,8 gam.
B. 86,2 gam.
C. 71,4 gam.
D. 119,0 gam.
Khi cho 112g dung dịch HCl (d=1,12g/ml) tác dụng với dung dịch NaHCO3 dư. sau phản ứng thu được 4,48 lít khí. tính C%, CM của dung dịch HCl
\(HCl+NaHCO_3\rightarrow NaCl+CO_2+H_2O\\ N_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ m_{HCl}=n_{CO_2}=0,2\left(mol\right)\\ V_{ddHCl}=\dfrac{112}{1,12}=100\left(ml\right)=0,1\left(l\right)\\ \Rightarrow C_{MddHCl}=\dfrac{0,2}{0,1}=2\left(M\right)\\ m_{HCl}=0,2.36,5=7,3\left(g\right)\\ C\%_{ddHCl}=\dfrac{7,3}{112}.100\approx6,518\%\)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: NaHCO3 + HCl --> NaCl + CO2 + H2O
0,2<------------0,2
=> \(C\%\left(HCl\right)=\dfrac{0,2.36,5}{112}.100\%=6,518\%\)
\(V_{ddHCl}=\dfrac{112}{1,12}=100\left(ml\right)=0,1\left(l\right)\)
=> \(C_M\left(HCl\right)=\dfrac{0,2}{0,1}=2M\)
Có 500 ml dung dịch X chứa Na+, NH4+, CO32– và SO42–. Lấy 100 ml dung dịch X tác dụng với lượng dư dung dịch HCl thu được 2,24 lít khí. Lấy 100 ml dung dịch X có tác dụng với lượng dư dung dịch BaCl2 thu được 43 gam kết tủa. Lấy 200 ml dung dịch X tác dụng với lượng dư dung dịch NaOH thu được 8,96 lít khí NH3. Các phản ứng hoàn toàn, thể tích khí đều đo ở đktc. Khối lượng muối có trong 300 ml X là
A. 71,4 gam.
B. 23,8 gam.
C. 47,6 gam.
D. 119,0 gam.
Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.
Có 500 ml dung dịch X chứa Na+, NH4+, CO32– và SO42–. Lấy 100 ml dung dịch X tác dụng với lượng dư dung dịch HCl thu được 2,24 lít khí. Lấy 100 ml dung dịch X có tác dụng với lượng dư dung dịch BaCl2 thu được 43 gam kết tủa. Lấy 200 ml dung dịch X tác dụng với lượng dư dung dịch NaOH thu được 8,96 lít khí NH3. Các phản ứng hoàn toàn, thể tích khí đều đo ở đktc. Khối lượng muối có trong 300 ml X là
A. 71,4 gam.
B. 23,8 gam.
C. 47,6 gam.
D. 119,0 gam.
Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.
Có 500 ml dung dịch X chứa Na + , NH 4 + , CO 3 2 - và SO 4 2 - . Lấy 100 ml dung dịch X tác dụng với lượng dư dung dịch HCl thu được 2,24 lít khí. Lấy 100 ml dung dịch X cho tác dụng với lượng dư dung dịch BaCl 2 thu được 43 gam kết tủa. Lấy 200 ml dung dịch X tác dụng với lượng dư dung dịch NaOH thu được 8,96 lít khí NH 3 . Các phản ứng hoàn toàn, các thể tích khí đều đo ở đktc. Tổng khối lượng muối có trong 300 ml dung dịch X là
A. 71,4 gam
B. 23,8 gam.
C. 86,2 gam
D. 119 gam.
Chọn A
Gọi số mol Na + , NH 4 + , CO 3 2 - và SO 4 2 - trong 100ml dung dịch X lần lượt là x, y, z và t.
Bảo toàn điện tích có: x + y – 2z – 2t = 0 (1)
Cho 100ml X tác dụng với HCl dư:
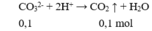
→ z = 0,1 (2)
Cho 100ml X tác dụng với BaCl2 dư:
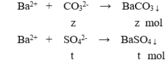
m↓ = 43 (gam) → 197z + 233t = 43 (3)
Cho 100 ml X tác dụng với NaOH
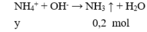
→ y = 0,2 (4)
Từ (1); (2); (3); (4) có x = y = 0,2; z = 0,1; t = 0,1.
Tổng khối lượng muối trong 300ml dung dịch là:
m = 3. (0,2.23 + 0,2.18 + 0,1.60 + 0,1.96) = 71,4 gam.
Có 500 ml dung dịch X chứa Na+, NH4+, CO32- và SO42- . Lấy 100 ml dung dịch X tác dụng với lượng dư dung dịch HCl thu được 2,24 lít khí. Lấy 100 ml dung dịch X cho tác dụng với lượng dư dung dịch BaCl2 thu được 43 gam kết tủa. Lấy 200 ml dung dịch X tác dụng với lượng dư dung dịch NaOH thu được 8,96 lít khí NH3. Các phản ứng hoàn toàn, các thể tích khí đều đo ở đktc. Tổng khối lượng muối có trong 300 ml dung dịch X ?
A. 71,4 gam.
B. 86,2 gam.
C. 119 gam.
D. 23,8 gam.
Đáp án : A
Trong 100 ml X : nCO3 = nCO2 = 0,1 mol
, mkết tủa = mBaCO3 + mBaSO4 = 43 => nSO4 = 0,1 mol
Trong 200 ml X : nNH3 = nNH4 = 0,4 mol
=> Trong 300 ml X có : 0,3 mol CO32- ; 0,3 mol SO42- ; 0,6 mol NH4+ và 0,6 mol Na+ ( BT điện )
=> mmuối = 71,4g