
Những câu hỏi liên quan
Biến thiên entanpi của phản ứng (kí hiệu là Delta H) có thể hiểu đơn giản là nhiệt tỏa ra hoặc thu vào khi phản ứng hóa học xảy ra. Nếu phản ứng tỏa nhiệt thì Delta H có dấu âm và ngược lại, nếu phản ứng thu nhiệt thì Delta H có dấu dương. Khi một phản ứng hóa học xảy ra, các liên kết trong chất phản ứng bị cắt đứt và các liên kết mới được hình thành, tạo nên chất sản phẩm. Để tính Delta H của phản ứng, người ta dựa vào năng lượng các liên kết left(E_{lk}right). E_{lk} là năng lượng cần cung cấp...
Đọc tiếp
Biến thiên entanpi của phản ứng (kí hiệu là \(\Delta H\)) có thể hiểu đơn giản là nhiệt tỏa ra hoặc thu vào khi phản ứng hóa học xảy ra. Nếu phản ứng tỏa nhiệt thì \(\Delta H\) có dấu âm và ngược lại, nếu phản ứng thu nhiệt thì \(\Delta H\) có dấu dương. Khi một phản ứng hóa học xảy ra, các liên kết trong chất phản ứng bị cắt đứt và các liên kết mới được hình thành, tạo nên chất sản phẩm. Để tính \(\Delta H\) của phản ứng, người ta dựa vào năng lượng các liên kết \(\left(E_{lk}\right)\). \(E_{lk}\) là năng lượng cần cung cấp để cắt đứt một liên kết thành các nguyên tử ở thể khí. Năng lượng tỏa ra khi hình thành liên kết đó từ các nguyên tử ở thể khí cũng có giá trị bằng giá trị của \(E_{lk}\) nhưng có dấu ngược lại.
\(E_{lk}\) của một số liên kết được cho trong bảng sau:
| Liên kết | C\(\equiv\)C\(\) | C-C | C-H | H-H |
| \(E_{lk}\left(kJ/mol\right)\) | 839,0 | 343,3 | 418,4 | 432,0 |
Xét phản ứng: \(C_2H_2+2H_2\rightarrow C_2H_6\left(1\right)\)
Dựa vào bảng số liệu trên hãy:
a. Tính năng lượng cần cung cấp để phá vỡ liên kết của các chất tham gia trong phản ứng (1) (Lưu ý hệ số của các chất trong phương trình phản ứng).
b. Tính năng lượng tỏa ra khi hình thành các liên kết trong chất sản phẩm của phản ứng (1)
c. Từ các kết quả trên, xác định \(\Delta H\) của phản ứng (1) và cho biết phản ứng (1) tỏa nhiệt hay thu nhiệt.
\(a.E_r=839,0+2\cdot418,4+2\cdot432,0=2539,8kJ\\ b.E_p=343,3+6\cdot418,4=2853,7kJ\\ c.\Delta_rH^{^{ }0}=2539,8-3197=-313,9kJ\cdot mol^{-1}\\ \Delta H< 0:pư.thu.nhiệt\)
Đúng 1
Bình luận (1)
\(a.E_{reactants}=839,0+2\cdot432,0=1703kJ\\ b.E_{products}=343,3+6\cdot432,0=2935,3kJ\\ c.\Delta_rH^{^o}_{298}=E_r-E_p=1703-2935,3=1232,3kJ\cdot mol^{^{ }-1}.\)
\(\Delta H< 0\) => Phản ứng (1) thu nhiệt
Đúng 0
Bình luận (3)
Trong biểu thức của nguyên lí thứ nhất của nhiệt động lực học
Q
Δ
U
+
A
. Quy ước về dấu nào sau đây là đúng? A.
Q
0
: Vật nhận nhiệt lượng của các vật khác.
Q
0
: Vật truyền nhiệt lượng cho các vật khác. B.
A
0
: Vật thực hiện công;
A
...
Đọc tiếp
Trong biểu thức của nguyên lí thứ nhất của nhiệt động lực học Q = Δ U + A . Quy ước về dấu nào sau đây là đúng?
A. Q > 0 : Vật nhận nhiệt lượng của các vật khác. Q < 0 : Vật truyền nhiệt lượng cho các vật khác.
B. A > 0 : Vật thực hiện công; A > 0 : Vật nhận công lên các vật khác.
C. Δ U > 0 : Vật sinh công; Δ U < 0 : Vật nhận công.
D. Các quy ước trên đều đúng.
Trong biểu thức của nguyên lí thứ nhất của nhiệt động lực học
Q
Δ
U
+
A
. Quy ước về dấu nào sau đây là đúng? A. Q 0: Vật nhận nhiệt lượng của các vật khác. Q 0: Vật truyền nhiệt lượng cho các vật khác B. A 0: Vật thực hiện công; A 0: Vật nhận công lên các vật khác C.
Δ
U...
Đọc tiếp
Trong biểu thức của nguyên lí thứ nhất của nhiệt động lực học Q = Δ U + A . Quy ước về dấu nào sau đây là đúng?
A. Q > 0: Vật nhận nhiệt lượng của các vật khác. Q < 0: Vật truyền nhiệt lượng cho các vật khác
B. A > 0: Vật thực hiện công; A < 0: Vật nhận công lên các vật khác
C. Δ U > 0 : Vật sinh công; Δ U < 0 : Vật nhận công
D. Các quy ước trên đều đúng
Trong biểu thức của nguyên lí thứ nhất của nhiệt động lực học
Q
Δ
U
+
A
. Quy ước về dấu nào sau đây là đúng? A. Q 0: Vật nhận nhiệt lượng của các vật khác. Q 0: Vật truyền nhiệt lượng cho các vật khác. B. A 0: Vật thực hiện công; A 0: Vật nhận công lên các vật khác C.
Δ
U
0
: Vật sinh công;
Δ
U
0
: Vật nhận cô...
Đọc tiếp
Trong biểu thức của nguyên lí thứ nhất của nhiệt động lực học Q = Δ U + A . Quy ước về dấu nào sau đây là đúng?
A. Q > 0: Vật nhận nhiệt lượng của các vật khác. Q < 0: Vật truyền nhiệt lượng cho các vật khác.
B. A > 0: Vật thực hiện công; A < 0: Vật nhận công lên các vật khác
C. Δ U > 0 : Vật sinh công; Δ U < 0 : Vật nhận công.
D. Các quy ước trên đều đúng.
Nêu hệ thức của nguyên lí 1 nhiệt động lực học.Nêu tên,đơn vị và quy ước dấu của các đại lượng trong hệ thức,
Vận dụng: Người ta truyền nhiệt cho một bình khí làm khí dãn ra đẩy pittong chuyển động? Bình khí nhận nhiệt lượng hay truyền nhiệt lượng.Hãy dựa vào quy ước dấu về nhiệt lượng và xác định dấu của công A và nhiệt lượng Q
Giúp em trả lời câu hỏi này với ạ
Đọc tiếp
Nêu hệ thức của nguyên lí 1 nhiệt động lực học.Nêu tên,đơn vị và quy ước dấu của các đại lượng trong hệ thức,
Vận dụng: Người ta truyền nhiệt cho một bình khí làm khí dãn ra đẩy pittong chuyển động? Bình khí nhận nhiệt lượng hay truyền nhiệt lượng.Hãy dựa vào quy ước dấu về nhiệt lượng và xác định dấu của công A và nhiệt lượng Q
Giúp em trả lời câu hỏi này với ạ
chọn câu sai khi nói về phản ứng nhiệt hạch và phân hạchA.phản ứng nhiệt hạch là phản ứng kết hợp hai hạt nhân nhẹ thành hạt nhân nặng hơnB.con người đã thực hiện được phản ứng phân hạch có kiểm soát đượcC.điều kiện xảy ra phản ứng phân hạch và nhiệt hạch phải có các notron chậmD.năng lượng tỏa ra của phản ứng nhiệt hạch lớn hơn và sạch hơn của phân hạch
Đọc tiếp
chọn câu sai khi nói về phản ứng nhiệt hạch và phân hạch
A.phản ứng nhiệt hạch là phản ứng kết hợp hai hạt nhân nhẹ thành hạt nhân nặng hơn
B.con người đã thực hiện được phản ứng phân hạch có kiểm soát được
C.điều kiện xảy ra phản ứng phân hạch và nhiệt hạch phải có các notron chậm
D.năng lượng tỏa ra của phản ứng nhiệt hạch lớn hơn và sạch hơn của phân hạch
A đúng
B đúng, con người kiểm soát phản ứng phân hạch bằng lò phản ứng hạt nhân
D đúng, đặc biệt phản ứng nhiệt hạch không kèm theo tia phóng xạ, nên sạch hơn phân hạch.
C là đáp án sai.
Đúng 0
Bình luận (0)
Liệt kê tối thiểu 5 ví dụ về :
a. Phản ứng tỏa nhiệt
b. Phản ứng thu nhiệt
c. Quá trình thu nhiệt
Bạn em đã lập bảng về mối quan hệ giữa một số kim loại với một số dung dịch muối như sau :Chú thích : Dấu X là có phản ứng hoá học xảy ra.Dấu O là không xảy ra phản ứng.Hãy : Sửa lại những dấu X và O không đúng trong các ô của bảng.Bổ sung dấu X hoặc dấu O vào những dấu chấm trong các ô trống.Viết các phương trình hoá học của phản ứng xảy ra theo dấu X.
Đọc tiếp
Bạn em đã lập bảng về mối quan hệ giữa một số kim loại với một số dung dịch muối như sau :
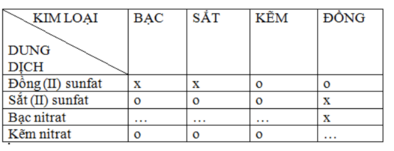
Chú thích : Dấu X là có phản ứng hoá học xảy ra.
Dấu O là không xảy ra phản ứng.
Hãy :
Sửa lại những dấu X và O không đúng trong các ô của bảng.
Bổ sung dấu X hoặc dấu O vào những dấu chấm trong các ô trống.
Viết các phương trình hoá học của phản ứng xảy ra theo dấu X.
ta có bảng về mối quan hệ giữa một kim loại với một số dung dịch muối:
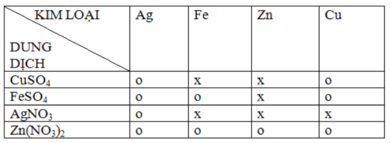
Viết các phương trình hóa học của phản ứng xảy ra theo dấu x
Fe + CuSO 4 → FeSO 4 + Cu
Zn + CuSO 4 → ZnSO 4 + Cu
Zn + FeSO 4 → ZnSO 4 + Fe
Fe + 2 AgNO 3 → Fe NO 3 2 + 2Ag
Zn + 2 AgNO 3 → Zn NO 3 2 + 2Ag
Cu + 2 AgNO 3 → Cu NO 3 2 + 2Ag
Đúng 0
Bình luận (0)
Có các phát biểu về cân bằng hóa học: 1. Cân bằng hóa học là một cân bằng bền. 2. Nếu phản ứng thuận tỏa nhiệt ( ∆ H 0 ) thì khi tăng nhiệt độ cân bằng sẽ bị chuyển dịch về phía trái (phản ứng nghịch). 3. Nếu phản ứng thuận tỏa nhiệt thì phản ứng nghịch thu nhiệt. 4. Nếu trong phản ứng mà số mol khí tham gia bằng số mol khí tạo thành thì áp suất không ảnh hưởng tới cân bằng hóa học. 5. Hằng số cân bằng bị thay đổi khi nồng độ các chất thay đổi. 6. Trong biểu thức về hằng số cân bằng có mặt nồng...
Đọc tiếp
Có các phát biểu về cân bằng hóa học:
1. Cân bằng hóa học là một cân bằng bền.
2. Nếu phản ứng thuận tỏa nhiệt ( ∆ H < 0 ) thì khi tăng nhiệt độ cân bằng sẽ bị chuyển dịch về phía trái (phản ứng nghịch).
3. Nếu phản ứng thuận tỏa nhiệt thì phản ứng nghịch thu nhiệt.
4. Nếu trong phản ứng mà số mol khí tham gia bằng số mol khí tạo thành thì áp suất không ảnh hưởng tới cân bằng hóa học.
5. Hằng số cân bằng bị thay đổi khi nồng độ các chất thay đổi.
6. Trong biểu thức về hằng số cân bằng có mặt nồng độ của tất cả các chất tham gia phản ứng.
Hãy chọn các phát biểu sai.
A. 1 và 5
B. 1 và 6
C. 1 , 5, 6
D. 1 , 3 , 5 ,6.
Đáp án C
1. Sai: cân bằng hóa học là cân bằng động
2. đúng: phản ứng nghịch thu nhiệt, khi tăng nhiệt độ cân bằng sẽ chuyển về phía làm giảm nhiệt độ (thu nhiệt).
3. đúng
4. đúng
5. sai, nồng độ thay đổi không làm thay đổi hằng số cân bằng. Hằng số cân bằng chỉ thay đổi khi thay đổi nhiệt độ.
6. sai: chỉ tính những chất khí hoặc những chất tan trong dung dịch, nếu là chất rắn thì không được tính.
=> Đáp án C
Đúng 0
Bình luận (0)













