Đốt cháy hoàn toàn 9,4 gam một hợp chất hữu cơ đơn chức X cần 15,68 lít khí O2 (đktc), thu được CO2 và H2O có số mol bằng nhau. Xác định CTĐGN của X

Những câu hỏi liên quan
Đốt cháy hoàn toàn 5,8 gam một hợp chất hữu cơ đơn chức X cần 8,96 lít khí O2 (đktc), thu được CO2 và H2O có số mol bằng nhau. CTĐGN của X là: A. C2H4O B. C3H6O C. C4H8O D. C5H10O
Đọc tiếp
Đốt cháy hoàn toàn 5,8 gam một hợp chất hữu cơ đơn chức X cần 8,96 lít khí O2 (đktc), thu được CO2 và H2O có số mol bằng nhau. CTĐGN của X là:
A. C2H4O
B. C3H6O
C. C4H8O
D. C5H10O
Đáp án : B
Đặt nCO2 = nH2O = x; bảo toàn khối lượng => X = 0,3 mol
Bảo toàn C và H => nO = 0,1; Tỉ lệ C:H:O = 3 : 6 : 1
Đúng 0
Bình luận (0)
Để đốt cháy hoàn toàn 8,9 gam chất hữu cơ X phải dùng hết 8,4 lít khí oxi (đktc). Sản phẩm cháy gồm có 6,3 gam H2O và 7,84 gam lít hỗn hợp khí gồm CO2 và N2 (đktc). Xác định CTĐGN của X
Ta có: \(n_{O_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
Theo ĐLBT KL, có: mX + mO2 = mH2O + mCO2 + mN2.
⇒ 44nCO2 + 28nN2 = 8,9 + 0,375.32 - 6,3 = 14,6 (1)
Mà: \(n_{CO_2}+n_{N_2}=\dfrac{7,84}{22,4}=0,35\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CO_2}=0,3\left(mol\right)=n_C\\n_{N_2}=0,05\left(mol\right)\Rightarrow n_N=0,05.2=0,1\left(mol\right)\end{matrix}\right.\)
- Đốt cháy X thu CO2, H2O và N2 → X chứa C, H, N, có thể có O.
Ta có: \(n_{H_2O}=\dfrac{6,3}{18}=0,35\left(mol\right)\Rightarrow n_H=0,35.2=0,7\left(mol\right)\)
⇒ mC + mH + mN = 0,3.12 + 0,7.1 + 0,1.14 = 5,7 (g) < 8,9 (g)
Vậy: X chứa C, H, O và N.
⇒ mO = 8,9 - 5,7 = 3,2 (g) \(\Rightarrow n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của X là CxHyOzNt.
\(\Rightarrow x:y:z:t=0,3:0,7:0,2:0,1=3:7:2:1\)
Vậy: CTĐGN của X là C3H7O2N.
Đúng 2
Bình luận (0)
Hỗn hợp E gồm hai ancol đơn chức X và Y (MX MY), là đồng đẳng kế tiếp. Đốt cháy hoàn toàn a gam E bằng
O
2
, thu được 2,912 lít khí
C
O
2
(đktc) và 3,24 gam
H
2
O
. Đun nóng b gam E với
H
2
S
O
4
đặc, thu được hỗn hợp các chất hữu cơ Z gồm: 0,12 mol hai olefin (c...
Đọc tiếp
Hỗn hợp E gồm hai ancol đơn chức X và Y (MX < MY), là đồng đẳng kế tiếp. Đốt cháy hoàn toàn a gam E bằng O 2 , thu được 2,912 lít khí C O 2 (đktc) và 3,24 gam H 2 O . Đun nóng b gam E với H 2 S O 4 đặc, thu được hỗn hợp các chất hữu cơ Z gồm: 0,12 mol hai olefin (có khối lượng 4,20 gam) và một lượng ancol dư. Đốt cháy hoàn toàn Z cần vừa đủ 21,84 lít khí O 2 (đktc). Hiệu suất phản ứng tạo olefin của X và Y lần lượt là
A. 50% và 20%
B. 60% và 40%
C. 40% và 40%
D. 50% và 30%
1.Đốt hoàn toàn 4,2g một este E thu được 6,16g CO2 và 2,52g H2O . Công thức cấu tạo của E là ?2.Este X tạo bởi ancol no đơn chức và axitcacboxylic không no ( có 1 liên kết đôi ) đơn chức . Đốt cháy m mol X thu được 22,4 lít co2 (đktc) và 9g H2O . giá trị của m là bao nhiêu ?3.đốt cháy hoàn toàn 0,1 gam một chất hữu cơ X cần 4,48 lít khí oxi (đktc) thu được nco2:nh2o1:1 . Biết rằng X tác dụng với NAOH tạo ra 2 chất hữu cơ . CTCT của X là ?
Đọc tiếp
1.Đốt hoàn toàn 4,2g một este E thu được 6,16g CO2 và 2,52g H2O . Công thức cấu tạo của E là ?
2.Este X tạo bởi ancol no đơn chức và axitcacboxylic không no ( có 1 liên kết đôi ) đơn chức . Đốt cháy m mol X thu được 22,4 lít co2 (đktc) và 9g H2O . giá trị của m là bao nhiêu ?
3.đốt cháy hoàn toàn 0,1 gam một chất hữu cơ X cần 4,48 lít khí oxi (đktc) thu được nco2:nh2o=1:1 . Biết rằng X tác dụng với NAOH tạo ra 2 chất hữu cơ . CTCT của X là ?
1. CxHyOz + O2 \(\rightarrow\) CO2 + H2O
4,2g m 6,16 2,52
Áp dụng ĐLBTKL: 4,2 + m = 6,16 + 2,52 suy ra: m = 4,48g.
Số mol C: nC = nCO2 = 6,16:44 = 0,14 mol; số mol H: nH = 2nH2O = 2.2,52:18 = 0,28 mol; số mol O: nO = 2nO2 = 2.4,48:32 = 0,28 mol.
x:y:z = 0,14:0,28:0,28 = 1:2:2. Suy ra: CTĐG: (CH2O2)n, công thức này trùng với công thức cấu tạo: HCOOH.
Đúng 0
Bình luận (0)
Câu 2:
Đặt công thức: CnH2n+1COOCmH2m+1
CnH2n-1COOCmH2m+1+(......)O2\(\rightarrow\)(n+1+m)CO2+(n+m)H2O
\(n_{CO_2}=1mol\)
\(n_{H_2O}=0,5mol\)
Dựa theo hệ số cân bằng ta có:
nX=\(n_{CO_2}-n_{H_2O}\)=1-0,5=0,5mol
Đúng 0
Bình luận (0)
Chỗ đặt công thức là CnH2n-1COOCmH2m+1
Mình ghi nhầm thành CnH2n+1
Đúng 0
Bình luận (0)
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!Bài 1:Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.Bài 2:Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/...
Đọc tiếp
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm hiđrocacbon A và hợp chất hữu cơ B có công thức CxHyOz ( x ≥ 2 ), cần dùng vừa đủ 14,56 lít O2 (đktc), thu được 8,96 lít CO2 (đktc) và 9,9 gam H2O. Xác định công thức phân tử của A và B
Hỗn hợp X gồm một axit cacboxylic (no, đơn chức) và một ancol (đơn chức, có khả năng tách nước tạo thành olefin). Đốt cháy hoàn toàn 3,00 gam X bằng O2, thu được 2,912 lít khí CO2 (đktc) và 2,88 gam H2O. Đun nóng m gam X (có mặt H2SO4 đặc), thu được hỗn hợp các chất hữu cơ Y gồm: axit, ancol dư và 0,02 mol este. Cho Y tác dụng với Na (dư), thu được 952 mL khí H2 (đktc). Hiệu suất phản ứng este hóa bằng A. 60,00% B. 26,67% C. 40,00% D. 66,67%
Đọc tiếp
Hỗn hợp X gồm một axit cacboxylic (no, đơn chức) và một ancol (đơn chức, có khả năng tách nước tạo thành olefin). Đốt cháy hoàn toàn 3,00 gam X bằng O2, thu được 2,912 lít khí CO2 (đktc) và 2,88 gam H2O. Đun nóng m gam X (có mặt H2SO4 đặc), thu được hỗn hợp các chất hữu cơ Y gồm: axit, ancol dư và 0,02 mol este. Cho Y tác dụng với Na (dư), thu được 952 mL khí H2 (đktc). Hiệu suất phản ứng este hóa bằng
A. 60,00%
B. 26,67%
C. 40,00%
D. 66,67%
Chọn đáp án C
X gồm axit dạng CnH2nO2 và ancol dạng CmH2m + 2O.
đốt 3 , 0 g a m X + O 2 → t 0 0 , 13 m o l C O 2 + 0 , 16 m o l H 2 O
tương quan đốt có n C m H 2 m + 2 O = ∑ n H 2 O – ∑ n C O 2 = 0 , 03 m o l
mX = mC + mH + mO ⇒ nO trong X = 0,07 mol
⇒ n C n H 2 n O 2 = 0 , 02 m o l (bảo toàn O).
⇒ có phương trình:
∑nC = 0,02n + 0,03m = 0,13 mol
⇔ 2n + 3m = 13
⇒ nghiệm: n = 2; m = 3 (chú ý do ancol tách được anken ⇒ m ≥ 2).
⇒ m gam hỗn hợp X gồm 2x mol CH3COOH và 3x mol C3H7OH.
♦ phản ứng: C H 3 C O O H + C 3 H 7 O H ⇄ C H 3 C O O C 3 H 7 + H 2 O
neste = 0,02 mol
⇒ nancol dư = (3x – 0,02) mol;
naxit dư = (2x – 0,02) mol.
phản ứng:
1OH + 1Na → 1ONa + 1 2 .H2↑
⇒ ∑ n O H + C O O H = 2 n H 2
= 2 × 0,0425 mol.
⇒ (3x – 0,02) + (2x – 0,02) = 0,085
⇒ x = 0,025 mol
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 4,6 gam một chất hữu cơ X, sau phản ứng thu được 4,48 lít CO2 (đktc) và 5,4 gam H2O. Công thức đơn giản nhất (CTĐGN) của X là: A. C2H6. B. CH3. C. C2H6O. D. CH3O.
Đọc tiếp
Đốt cháy hoàn toàn 4,6 gam một chất hữu cơ X, sau phản ứng thu được 4,48 lít CO2 (đktc) và 5,4 gam H2O. Công thức đơn giản nhất (CTĐGN) của X là:
A. C2H6.
B. CH3.
C. C2H6O.
D. CH3O.
Đáp án C
,nC = nCO2 = 0,2 mol ; nH = 2nH2O = 0,6 mol
Có : mX = mC + mH + mO => nO = 0,1 mol
=> nC : nH : nO = 0,2 : 0,6 : 0,1 = 2 : 6 : 1
Vậy CTĐG nhất là C2H6O
Đúng 0
Bình luận (0)
Hỗn hợp E gồm hai axit cacboxylic đơn chức X, Y (là đồng đẳng kế tiếp,
M
X
M
Y
). Đốt cháy hoàn toàn 3,88 gam E bằng O2, thu được 6,16 gam CO2 và 2,52 gam H2O. Đun nóng m gam E với 6,4 gam ancol metylic (xúc tác H2SO4 đặc), thu được hỗn hợp các chất hữu cơ Z gồm: 0,08 mol hai este (có khối lượng 6,2 gam), hai axit và ancol dư. Đốt cháy hoàn toàn Z cần vừa đủ 15,12 lít khí O2 (đktc). Hiệu suất phản ứng tạo este...
Đọc tiếp
Hỗn hợp E gồm hai axit cacboxylic đơn chức X, Y (là đồng đẳng kế tiếp, M X < M Y ). Đốt cháy hoàn toàn 3,88 gam E bằng O2, thu được 6,16 gam CO2 và 2,52 gam H2O. Đun nóng m gam E với 6,4 gam ancol metylic (xúc tác H2SO4 đặc), thu được hỗn hợp các chất hữu cơ Z gồm: 0,08 mol hai este (có khối lượng 6,2 gam), hai axit và ancol dư. Đốt cháy hoàn toàn Z cần vừa đủ 15,12 lít khí O2 (đktc). Hiệu suất phản ứng tạo este của X và Y lần lượt là
A. 60% và 40%
B. 50% và 40%
C. 50% và 50%
D. 60% và 30%
Chọn đáp án A
+ Tìm công thức các axit:
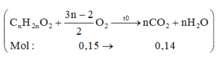
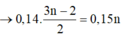
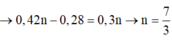
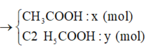
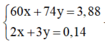
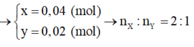
+ Phản ứng este hóa:
C H 3 C O O H + C H 3 O H → C H 3 C O O C H 3 + H 2 O a a
C 2 H 5 C O O H + C H 3 O H → C 2 H 5 C O O C H 3 + H 2 O b b
Theo bài:
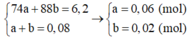
+ Sơ đồ phản ứng 2 (Đốt cháy Z):
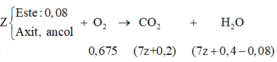
Bảo toàn nguyên tố oxi:
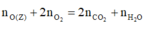
![]()
![]()
![]()
![]()
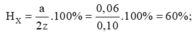
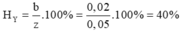
Đúng 0
Bình luận (0)