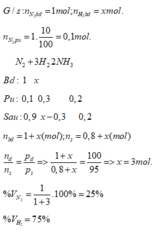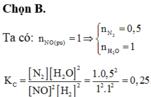Cách tính số mol ban đầu, số mol sau phản ứng, số mol phản ứng, chi tiết

Những câu hỏi liên quan
Thực hiện phản ứng tổng hợp amoniac: N2 + 3H2 - 2NH3 . ∆rH0298 0 Nồng độ mol ban đầu của các chất như sau: [N2] 0,5 mol/l; [H2] 0,6 mol/l. Khi phản ứng đạt cân bằng nồng độ mol của [NH3] 0,1 mol/l. a/ Tính hằng số cân bằng của phản ứng ? b/ Nêu các biện pháp tác động lên hệ cân bằng để tăng hiệu suất tổng hợp NH3 ?
Đọc tiếp
Thực hiện phản ứng tổng hợp amoniac: N2 + 3H2 -> 2NH3 . ∆rH0298 <0
Nồng độ mol ban đầu của các chất như sau: [N2] = 0,5 mol/l; [H2] = 0,6 mol/l. Khi phản ứng đạt cân bằng nồng độ mol của [NH3] = 0,1 mol/l.
a/ Tính hằng số cân bằng của phản ứng ?
b/ Nêu các biện pháp tác động lên hệ cân bằng để tăng hiệu suất tổng hợp NH3 ?a)Tại tđ cân bằng:
\(\left[N_2\right]=0,5-\dfrac{1}{2}.0,1=0,5-0,05=0,45\left(M\right)\)
\(\left[H_2\right]=0,6-\dfrac{3}{2}.0,1=0,6-0,15=0,45\left(M\right)\)
\(\Rightarrow k_c=\dfrac{\left[NH_3\right]^2}{\left[N_2\right].\left[H_2\right]^3}=\dfrac{0,1^2}{0,45.0,45^3}\approx0,244\)
b) Để tăng H tổng hợp \(NH_3\), chúng ta có thể:
- Tăng P bằng cách giảm V (chọn P phù hợp)
- Giảm nhiệt độ của hệ ( chọn nhiệt độ phù hợp)
- Thêm \(N_2;H_2\)
Đúng 2
Bình luận (0)
Chỉ mình là tại sao số mol O2 pứng < số mol O2 ban đầu thì lại dư vậy ạ . Có phải là số mol O2 phản ứng nghĩa là nó phản ứng nhưng vẫn chưa hết vì < ban đầu nếu lớn hơn ban đầu thì là dư ạ
Cái này thì mình giải thích đơn giản là có nghĩa ví dụ đề cho nO2=0.3mol. Nhưng khi ta tính theo phương thì nO2=0.1mol.Từ đây ta suy ra được là O2 dư .Bạn cứ làm nếu thấy nO2 pứng nhỏ hơn nO2 đề thì nó dư thôi. Nếu ko hiểu nữa thì inbox riêng cho mình nha .facebook Lê Đoàn Hương Giang .mình 2k7 nha
Đúng 0
Bình luận (0)
Hỗn hợp
N
2
và
H
2
trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol
N
2
đã phản ứng là 10%. Thành phần phần trăm số mol
N
2
trong hỗn hợp ban đầu là A. 20%. B. 25%. C. 10%. D. 5%.
Đọc tiếp
Hỗn hợp N 2 và H 2 trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol N 2 đã phản ứng là 10%. Thành phần phần trăm số mol N 2 trong hỗn hợp ban đầu là
A. 20%.
B. 25%.
C. 10%.
D. 5%.
Hỗn hợp
N
2
và
H
2
trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol
N
2
đã phản ứng là 10%. Thành phần phần trăm số mol
N
2
trong hỗn hợp ban đầu là A. 20%. B. 25%. C. 10%. D. 5%.
Đọc tiếp
Hỗn hợp N 2 và H 2 trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol N 2 đã phản ứng là 10%. Thành phần phần trăm số mol N 2 trong hỗn hợp ban đầu là
A. 20%.
B. 25%.
C. 10%.
D. 5%.
Chọn B
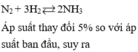
Áp suất thay đổi 5% so với áp suất ban đầu => n s a u n t r ư ớ c = 95 100
Giả sử trước phản ứng có 1 mol => sau phản ứng có 0,95 mol
ntrước – nsau = 2nN2 pư = 0,05 mol
è nN2 ban đầu = 0,025:10% = 0,25 =>%nN2 = 25%
Đúng 0
Bình luận (0)
Một hỗn hợp N2 và H2 được lấy vào bình phản ứng có nhiệt độ được giữ không đổi. Sau một thời gian phản ứng, áp suất của các khí trong bình giảm 10% so với áp suất ban đầu. Biết rằng tỉ lệ số mol N2 đã phản ứng là 10%. Tính thành phần phần trăm số mol N2 trong hỗn hợp đầu? A. 50% B. 49% C. 47% D. 48%
Đọc tiếp
Một hỗn hợp N2 và H2 được lấy vào bình phản ứng có nhiệt độ được giữ không đổi. Sau một thời gian phản ứng, áp suất của các khí trong bình giảm 10% so với áp suất ban đầu. Biết rằng tỉ lệ số mol N2 đã phản ứng là 10%. Tính thành phần phần trăm số mol N2 trong hỗn hợp đầu?
A. 50%
B. 49%
C. 47%
D. 48%
Thực hiện phản ứng tổng hợp amoniac :
N
2
+
3
H
2
↔
2
NH
3
Nồng độ mol ban đầu của các chất như sau :[
N
2
] 1 mol/l ; [
H
2...
Đọc tiếp
Thực hiện phản ứng tổng hợp amoniac :
N 2 + 3 H 2 ↔ 2 NH 3
Nồng độ mol ban đầu của các chất như sau :
[ N 2 ] = 1 mol/l ; [ H 2 ] = 1,2 mol/l
Khi phản ứng đạt cân bằng nồng độ mol của [ NH 3 ] = 0,2 mol/1. Tính hiệu suất của phản ứng tổng hợp amoniac.
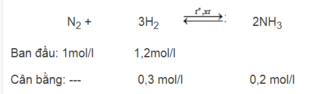
Theo PTHH thì 1 mol N 2 cần 3 mol H 2 . Ở đây chỉ có 1,2 mol H 2 , vì H 2 thiếu nên tác dụng hết. Hiệu suất phải tính theo lượng chất tác dụng hết. Số mol H 2 đã tác dụng là 0,3 mol.
Vậy h = (0,3 : 1,2). 100 = 25
Đáp số : h = 25%.
Đúng 0
Bình luận (0)
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là: A. 15% và 85% B. 82,35% và 77,5% C. 25% và 75% D. 22,5% và 77,5%
Đọc tiếp
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là:
A. 15% và 85%
B. 82,35% và 77,5%
C. 25% và 75%
D. 22,5% và 77,5%
Đáp án C
Giả sử có 1 mol hỗn hợp đầu. Gọi x và y (mol) lần lượt là số mol của N₂ và H₂ trong 1 mol hỗn hợp đầu
Gọi n₁, P₁ và n₂, P₂ lần lượt là số mol hỗn hợp khí + áp suất trong bình ban đầu và lúc sau
⇒ n₁ = x + y = 1 (1)
Khi nhiệt độ không đổi
⇒ n₁ / n₂ = P₁ / P₂
Áp suất khí trong bình giảm 5% so với áp suất ban đầu ⇒ P₁ / P₂ = 20 / 19
⇒ n₁ / n₂ = 20 / 19 (2)
Số mol của nito đã phản ứng là 10% ⇒ N₂ pứ 0,1x mol
N₂ + 3H₂ → 2NH₃
Trước: x y 0
Pứ 0,1x 0,3x 0,2x
Sau: n N₂ = 0,9x ; n H₂ = y - 0,3x ; n NH₃ = 0,2x
⇒ n₂ = 0,9x + y - 0,3x + 0,2x
⇒ n₂ = 0,8x + y (3)
Từ (1) (2) & (3) ta có:
(x + y) / (0,8x + y) = 20 / 19
⇒ 3x - y = 0 (4)
Giải hệ (1) & (4) cho ta: x = 0,25 mol và y = 0,75 mol
Thành phần phần trăm về số mol của N₂ và H₂ trong hỗn hợp đầu là:
%N₂ = 25% và %H₂ = 75%
Đúng 0
Bình luận (0)
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là: A. 15% và 85% B. 82,35% và 77,5% C. 25% và 75% D. 22,5% và 77,5%.
Đọc tiếp
Cho hỗn hợp N2 và H2 vào bình phản ứng có nhiệt độ không đổi. Sau một thời gian phản ứng, áp suất khí trong bình giảm 5% so với áp suất ban đầu. Biết tỉ lệ số mol của nitơ đã phản ứng là 10%. Thành phần phần trăm về số mol của N2 và H2 trong hỗn hợp đầu là:
A. 15% và 85%
B. 82,35% và 77,5%
C. 25% và 75%
D. 22,5% và 77,5%.
Xét phản ứng: 2NO + 2H2
→
N2 + 2H2O(k) xảy ra trong bình kín dung tích 2 lít, ở t°C. Ban đầu mỗi chất trong bình có 3 mol. Khi phản ứng đạt trạng thái cân bằng, số mol NO còn lại là 2 mol. Hằng số cân bằng Kc của phản ứng ở nhiệt độ đã cho là A. 0,0625 B. 0,25 C. 3,4 D. 7,0.
Đọc tiếp
Xét phản ứng: 2NO + 2H2 → N2 + 2H2O(k) xảy ra trong bình kín dung tích 2 lít, ở t°C. Ban đầu mỗi chất trong bình có 3 mol. Khi phản ứng đạt trạng thái cân bằng, số mol NO còn lại là 2 mol. Hằng số cân bằng Kc của phản ứng ở nhiệt độ đã cho là
A. 0,0625
B. 0,25
C. 3,4
D. 7,0.










 A.
A.