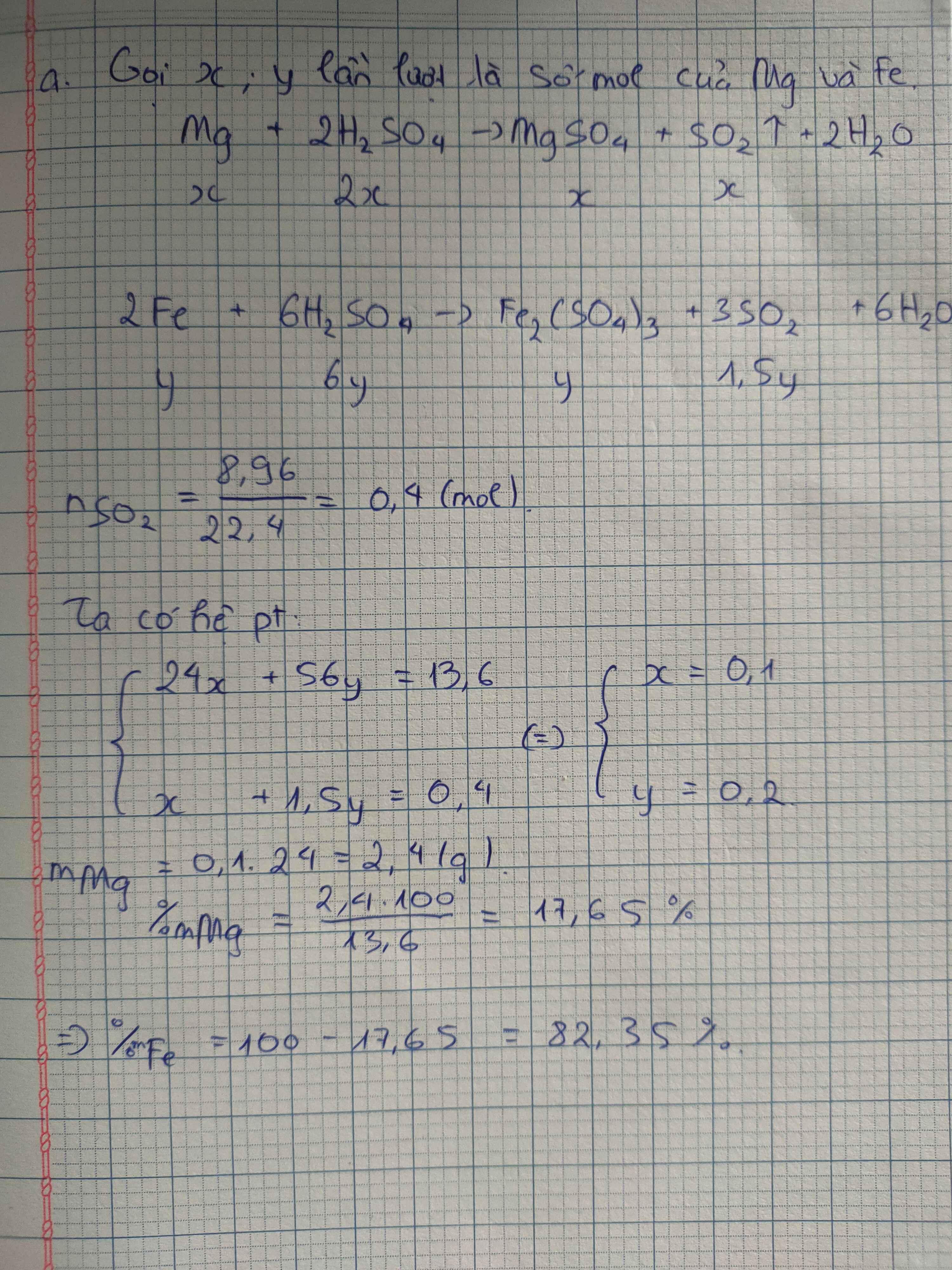cho bột sắt tan hoàn toàn trong 300g dd H2SO4 đặc nóng ,nồng độ 78,4% thu đc 16,8l khí SO2(đktc) và dd A . tính nồng độ % cuả chất tan trong dd A

Những câu hỏi liên quan
Cho bột iron tác dụng hoàn toàn với lượng dư dd H2SO4 đặc, nồng độ 78,4% thu được dd A trong đó nồng độ % của Fe2(SO4)3 và H2SO4 dư = nhau, giải phóng SO2. Tính nồng độ % của Fe2(SO4)3 và H2SO4 dư
Giả sử có 1 mol Fe tác dụng
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
1---->3----------->0,5------->1,5
Giả sử khối lượng dd H2SO4 78,4% là m (gam)
=> \(m_{H_2SO_4\left(bđ\right)}=\dfrac{m.78,4}{100}=0,784m\left(g\right)\)
=> \(m_{H_2SO_4\left(dư\right)}=0,784m-3.98=0,784m-294\left(g\right)\)
mdd sau pư = 1.56 + m - 1,5.64 = m - 40 (g)
Do C% của Fe2(SO4)3 và H2SO4 dư là bằng nhau
=> \(m_{Fe_2\left(SO_4\right)_3}=m_{H_2SO_4\left(dư\right)}\)
=> 400.0,5 = 0,784m - 294
=> m = \(\dfrac{30875}{49}\left(g\right)\)
mdd sau pư = \(\dfrac{28915}{49}\left(g\right)\)
=> \(C\%_{Fe_2\left(SO_4\right)_3}=C\%_{H_2SO_4\left(dư\right)}=\dfrac{200}{\dfrac{28915}{49}}.100\%=33,89\%\)
Đúng 4
Bình luận (0)
Cho 11,8g hỗn hợp gồm Cu,Al td H2SO4 20% sau phản ứng thu được 6,72l khí H2,dd A và chất rắn không tan B.Hoà tan B trong dd H2SO4 đặc nóng thu được 2,24l SO2(đktc)
a.Tính % mỗi khối lượng trong hh
b.Tính nồng độ % các chất trong dd A.
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
0,2<-----0,3<-----------0,1-------------0,3
Cu + 2H2SO4 ---> CuSO4 + SO2 + 2H2O
0,1<---------------------------------0,1
\(\rightarrow\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Cu}=0,1.64=6,4\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{5,4}{11,8}.100\%=45,76\%\\\%m_{Cu}=100\%-45,76\%=54,24\%\end{matrix}\right.\)
\(m_{ddA}=\dfrac{0,3.98}{20\%}+5,4-0,3.2=151,8\left(g\right)\\ C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1.342}{151,8}.100\%=22,53\%\)
Đúng 3
Bình luận (0)
Hoà tan hoàn toàn 13,6 gam hh A gồm Fe và Mg vào dd H2SO4 đặc, nóng 98% thu được dd X 8,96 lít khí SO2 (đktc).
a. Xác định thành phần % về khối lượng mỗi kim loại trong hỗn hợp ?
b. Tính nồng độ % các chất trong dd X .
#_giải chi tiết giùm nha mn_#
Cho bột sắt tác dụng hoàn toàn với lượng dư dung dịch H2SO4 đặc, nóng nồng độ 78,4%, thu được dung dịch A, trong đó nồng độ phần trăm của Fe2(SO4)3 và H2SO4 dư bằng nhau, giải phóng khí SO2.a) Tính nồng độ phần trăm của muối sắt và H2SO4 dư trong dung dịch A.b) Tính thể tích dung dịch NaOH 2M cần để tác dụng hết với 50 gam dung dịch A.
Đọc tiếp
Cho bột sắt tác dụng hoàn toàn với lượng dư dung dịch H2SO4 đặc, nóng nồng độ 78,4%, thu được dung dịch A, trong đó nồng độ phần trăm của Fe2(SO4)3 và H2SO4 dư bằng nhau, giải phóng khí SO2.
a) Tính nồng độ phần trăm của muối sắt và H2SO4 dư trong dung dịch A.
b) Tính thể tích dung dịch NaOH 2M cần để tác dụng hết với 50 gam dung dịch A.
Cho a gam hỗn hợp bột kim loại gồm Zn và Cu (Zn chiếm 97,5% về khối lượng) tác dụng hết với dd HCl dư thu đc khí A. Lượng khí A vừa đủ để pứ hoàn toàn với b gam một oxit sắt đc đặt trong một ống sứ nung đỏ. Hơi nước thoát ra từ ống sứ cho hấp thụ hoàn toàn vòa 173g dd H2SO4 97,1% đc dd H2SO4 có nồng độ nhỏ hơn nồng độ của dd axit ban đầu là 13,1% (dd C). Đun nóng 17,5 g dd C với 5% khối lượng chất sản phẩm rắn có trong ống sứ (pứ hoàn toàn) thì thấy có khí SO2 thoát ra1. Tìm công thức hóa học củ...
Đọc tiếp
Cho a gam hỗn hợp bột kim loại gồm Zn và Cu (Zn chiếm 97,5% về khối lượng) tác dụng hết với dd HCl dư thu đc khí A. Lượng khí A vừa đủ để pứ hoàn toàn với b gam một oxit sắt đc đặt trong một ống sứ nung đỏ. Hơi nước thoát ra từ ống sứ cho hấp thụ hoàn toàn vòa 173g dd H2SO4 97,1% đc dd H2SO4 có nồng độ nhỏ hơn nồng độ của dd axit ban đầu là 13,1% (dd C). Đun nóng 17,5 g dd C với 5% khối lượng chất sản phẩm rắn có trong ống sứ (pứ hoàn toàn) thì thấy có khí SO2 thoát ra
1. Tìm công thức hóa học của oxit sắt
2. Tính a,b
Mọi người giúp vs ạ B1 Hòa tan 4g NaOH vào H2O tạo thành dung dịch A. Trung hòa hoàn toàn dung dịch A bằng 200ml dd H2SO4 nồng độ x (M). Tính xB2 Đốt cháy 0.36g bột Mg trong không khí thu đc chất rắn A. Hòa tan hết A trong lượng vừa đủ là 100ml dd hcl loãng thu đc dd A1 . tính nồng độ mol của dd hcl đã dùng và nồng độ muối trong dung dich A
Xem chi tiết
B1:
2NaOH+H2SO4\(\rightarrow\)Na2SO4+2H2O
nNaOH=\(\frac{4}{40}=0.1\)mol
=>nH2SO4=\(\frac{1}{2}\)nNaOH=0.05 mol
=>CM=\(\frac{n_{H2SO42}}{V}\)=\(\frac{0.05}{200}\)=2,5.10-4 (M)
Đúng 0
Bình luận (0)
B2:
Mg+\(\frac{1}{2}\)O2\(\underrightarrow{t^0}\)MgO (1)
MgO+2HCl\(\rightarrow\)MgCl2+H2O (2)
nMg(1)=\(\frac{0,36}{24}=0,015mol\)
=>nMgO(1)=0,015=nMgO(2)
nHCl(2)=2nMgO(2)=0,03mol
=>CM(HCl)=\(\frac{n_{HCl}}{V}=\frac{0,03}{100}=3.10^{-4}M\)
Đúng 0
Bình luận (0)
Khử hoàn toàn 4,176 g một oxit của kim loại M bằng khí co dư thu đc chất rắn X và hỗn hợp khí Y. Dẫn toàn bộ Y vào dd nước vôi trong dư thấy xuất hiện 7,2 g kết tủa. Hòa tan hoàn toàn lượng X ở trên vào dd h2so4 nồng độ 80%(dd đặc), đun nóng thu đc V lít khí so2(so2 là sản phẩm khí duy nhất) và dd Z. Trong dd Z chỉ chứa 1 chất tan là muối sùnat của kim loại M có nồng đọ 61,069%.làm lạnh dd z thấy tách ra 5,8 g muối rắn. Lọc muối tách ra thấy nồng độ phần trăm của muối trong dd còn lại là 57,215%...
Đọc tiếp
Khử hoàn toàn 4,176 g một oxit của kim loại M bằng khí co dư thu đc chất rắn X và hỗn hợp khí Y. Dẫn toàn bộ Y vào dd nước vôi trong dư thấy xuất hiện 7,2 g kết tủa. Hòa tan hoàn toàn lượng X ở trên vào dd h2so4 nồng độ 80%(dd đặc), đun nóng thu đc V lít khí so2(so2 là sản phẩm khí duy nhất) và dd Z. Trong dd Z chỉ chứa 1 chất tan là muối sùnat của kim loại M có nồng đọ 61,069%.làm lạnh dd z thấy tách ra 5,8 g muối rắn. Lọc muối tách ra thấy nồng độ phần trăm của muối trong dd còn lại là 57,215%. Xác định công thức của muối kim loại và công thức của muối rắn. Tính V. Các phảm ứng xảy ra hoàn toàn, thể tích các khí đo ở đktc.
hòa tan hết 17.2 g hh X gồm Fe và 1 oxit sắt vào 200 gam dd HCl 14.6% thu đc ddA và 2.24 lít H2 đktc. thêm 33 g nước vào dd A được dd B .Nồng độ % của HCl trong HCl trong dd B là 2.92% .Mặt khác, cũng hòa tan hết 17.2 g hhX vào dd H2SO4 đặc nóng thì thu được V lít khí SO2 duy nhất đktc
1. x đ CTHH của oxit sắt
2. Tính khoảng giá trị của V
Hoà tan hoàn toàn 4,8 g Mg vào 200ml dd HCl thu đc dd A và khí B a, tính V khí B(đktc) b, tính Cm nồng độ chất có trong A c, cho dd NaOH 2M vừa đủ vào A. Tính V dd NaOH cần dùng
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2-->0,4----->0,2------->0,2
a
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b
\(CM_{MgCl_2}=\dfrac{0,2}{0,2}=1M\)
c
\(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\)
0,2------>0,4
\(V_{dd.NaOH}=\dfrac{0,4}{2}=0,2\left(l\right)\)
Đúng 3
Bình luận (0)