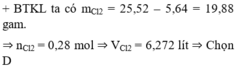Câu 56: Đốt cháy hỗn hợp bột Al và Mg trong bình dụng khi Clo dư, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng chất rắn trong bình tăng 4,26 gam. Thể tích khí Clo đã phản ứng ở đktc là? A. 1,344 lit B. 13,44 lit C. 2,688 lit. D. 26,88 lit

Những câu hỏi liên quan
Đốt cháy bột Al trong bình khí Clo dư, sau khi phản ứng xảy ra hoàn toàn khối lượng chất rắn trong bình tăng 4,26 gam. Khối lượng Al đã phản ứng là ?
m tăng là m Cl2 phản ứng:
nCl2 = \(\dfrac{4,26}{72}\)= 0,06 (mol)
PTHH: 2Al + 3Cl \(\rightarrow\) 2AlCl3
0,04mol \(\leftarrow\) 0,06mol
\(\rightarrow\) mAl = 0,04 x 27 = 1,08 (g)
Đúng 0
Bình luận (0)
Đốt cháy bột Al trong bình khí clo dư, sau phản ứng xảy ra hoàn toàn khối lượng chất rắn trong bình tăng 4,26 g .khối lượng Al đã phản ứng
Xem chi tiết
Khối lượng chất rắn trong bình tăng là khối lượng khí clo phản ứng
\(n_{Cl_2}=\dfrac{4,26}{71}=0,06\left(mol\right)\\ PTHH:2Al+3Cl_2\underrightarrow{t^o}2AlCl_3\)
Theo pthh, ta có: \(n_{Al}=\dfrac{2}{3}n_{Cl_2}=\dfrac{2}{3}.0,06=0,04\left(mol\right)\)
\(m_{Al}=0,04.27=1,08\left(g\right)\)
Đúng 2
Bình luận (0)
2Al + 3Cl2 => 2AlCl3
mCl pư = m chất rắn tăng = 4,26 (g)
=> nCl= 0,12
=> nAl pư = 1/3 nCl = 0,04 => mAl pư= 1,08 (g)
Đúng 1
Bình luận (1)
Khối lượng chất rắn trong bình tăng bằng chính khối lượng của \(Cl_2\) phản ứng
\(m_{Cl_2\left(pứ\right)}=4,26\left(g\right)\Rightarrow n_{Cl_2\left(pứ\right)}=0,06\left(mol\right)\)
PTHH: \(2Al+3Cl_2\rightarrow2AlCl_3\)
\(0,04\leftarrow0,06\) \(\left(mol\right)\)
\(m_{Al}=0,04\cdot27=1,08\left(g\right)\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Đốt cháy nhôm trong bình khí clo, sau phản ứng thấy khối lượng chất rắn trong bình tăng thêm 4,26 gam. Khối lượng Al đã tham gia phản ứng là (Cl=35,5, Al=27)
A. 1,08 g
B. 5,34 g
C. 6,42 g
D. 5,4 g
Đáp án A
Khối lượng chất rắn tăng bằng khối lượng của Cl2 => Số mol Cl2
=> Số mol Al tham gia phản ứng => Khối lượng Al tham gia phản ứng:
nCl2 = 4,26/71 = 0,06 mol
=> nAl = 0,06x2/3 = 0, 04 mol
=> mAl = 0,04 x 27 = 1,08 gam.
Đúng 0
Bình luận (0)
đốt cháy bột Al trong bình khí Cl dư, sau khi phản ứng xảy ra hoàn toàn khối lượng chất tăng thêm 4,26g khối lượng Al đã phản ứng là
Xem chi tiết
2Al + 3Cl2 => 2AlCl3
mCl pư = m chất rắn tăng = 4,26 (g)
=> nCl= 0,12
=> nAl pư = 1/3 nCl = 0,04 => mAl pư= 1,08 (g)
Đúng 0
Bình luận (0)
ai giúp vs ạ bài 9 hóa học 8 trong sbt các anh chị giúp e vs ạ e chẳng giải đc câu nào ngày mai là nộp ạ
Đúng 0
Bình luận (0)
Đốt cháy 5,64 gam hỗn hợp gồm Mg, Al trong khí Cl2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 25,52 gam hỗn hợp muối. Thể tích khí Cl2 (đktc) đã phản ứng là
A. 3,136 lít.
B. 4,928 lít.
C. 12,544 lít.
D. 6,272 lít.
Chọn đáp án D
+ BTKL ta có mCl2 = 25,52 – 5,64 = 19,88 gam.
⇒ nCl2 = 0,28 mol ⇒ VCl2 = 6,272 lít ⇒ Chọn D
Đúng 0
Bình luận (0)
Đốt cháy 5,64 gam hỗn hợp gồm Mg, Al trong khí C l 2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 25,52 gam hỗn hợp muối. Thể tích khí C l 2 (đktc) đã phản ứng là
A. 12,544 lít
B. 4,928 lít
C. 6,272 lít
D. 3,136 lít
Đáp án C
Bảo toàn khối lượng có: m k h í = m m u ố i – m K L = 25,52 – 5,64 = 19,88 gam
→ n k h í = 19,88/71 = 0,28 mol, V k h í = 0,28.22,4 = 6,272 lít.
Đúng 0
Bình luận (0)
Đốt cháy 5,64 gam hỗn hợp gồm Mg, Al trong khí
Cl
2
dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 25,52 gam hỗn hợp muối. Thể tích khí
Cl
2
(đktc) đã phản ứng là A. 3,136 lít. B. 4,928 lít. C. 12,544 lít. D. 6,272 lít.
Đọc tiếp
Đốt cháy 5,64 gam hỗn hợp gồm Mg, Al trong khí Cl 2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 25,52 gam hỗn hợp muối. Thể tích khí Cl 2 (đktc) đã phản ứng là
A. 3,136 lít.
B. 4,928 lít.
C. 12,544 lít.
D. 6,272 lít.
Đốt cháy 5,64 gam hỗn hợp gồm Mg, Al trong khí C l 2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 25,52 gam hỗn hợp muối. Thể tích khí C l 2 (đktc) đã phản ứng là
A. 12,544 lít.
B. 4,928 lít.
C. 6,272 lít.
D. 3,136 lít.
Đốt cháy hoàn toàn 15,6gam hỗn hợp 2 kim loại Mg và Al trong bình đựng khí oxi, sau phản ứng xảy ra hoàn toàn thu được 28,4gam hỗn hợp 2 oxit. Thể tích khí oxi(ở đktc) đã dùng để đốt cháy lượng kim loại trên
Theo ĐLBT KL, có: mKL + mO2 = m oxit
⇒ mO2 = 28,4 - 15,6 = 12,8 (g)
\(\Rightarrow n_{O_2}=\dfrac{12,8}{32}=0,4\left(mol\right)\Rightarrow V_{O_2}=0,4.22,4=8,96\left(l\right)\)
Đúng 1
Bình luận (0)