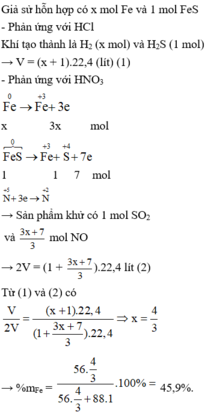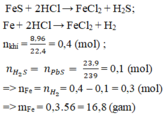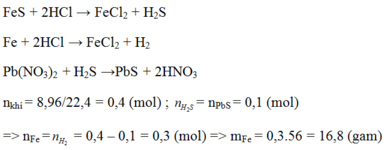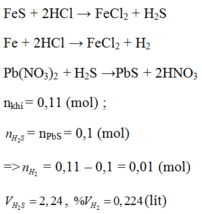Cho 7,2 gam hỗn ha gồm Fe và FeS tác dụng với dung dịch HCL dư thu được 2.24 lít hỗn hợp khí (ở đktc). Tính số mol của Fe và FeS trong hỗn hợp ban đầu

Những câu hỏi liên quan
Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư), thu được 2,464 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 (dư), thu được 23,9g kết tủa màu đen. a) Viết các phương trình hóa học của phản ứng đã xảy ra. b) Hỗn hợp khí thu được gồm những khí nào? Thể tích mỗi khí là bao nhiêu (đktc)? c) Tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu?
Đọc tiếp
Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư), thu được 2,464 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 (dư), thu được 23,9g kết tủa màu đen.
a) Viết các phương trình hóa học của phản ứng đã xảy ra.
b) Hỗn hợp khí thu được gồm những khí nào? Thể tích mỗi khí là bao nhiêu (đktc)?
c) Tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu?
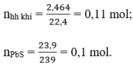
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) Theo PT (2) ⇒ nFeS = nH2S = 0,1 mol
⇒ mFeS = 0,1 × 88 = 8,8g.
Theo PT (1) nFe = nH2 = 0,01 mol ⇒ mFe = 56 × 0,01 = 0,56g.
Đúng 1
Bình luận (0)
Cho hỗn hợp Fe và Fes tác dụng với dung dịch HCl dư thu được 6,72 lít hỗn hợp khí (đktc) . Dẫn hỗn hợp này qua dung dịch Pb(NO3)2 dư thu được 47,8g kết tủa đen . Tính khối lượng và thành phần phần trăm theo khối lượng của Fe và FeS trong hỗn hợp ban đầu ?
\(n_{PbS}=\dfrac{47,8}{239}=0,2\left(mol\right)\)
Bảo toàn S: \(n_{FeS}=n_{H_2S}=0,2\left(mol\right)\)
\(n_{H_2}=\dfrac{6,72}{22,4}-0,2=0,1\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1<----------------------0,1
=> mFe = 0,1.56 = 5,6 (g)
mFeS = 0,2.88 = 17,6 (g)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{5,6+17,6}.100\%=24,138\%\\\%m_{FeS}=\dfrac{17,6}{5,6+17,6}.100\%=75,862\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Hỗn hợp X gồm Fe và FeS. Cho m gam X tác dụng hết với dung dịch HCl dư, thu được V lít khí (đktc). Mặt khác, m gam X tác dụng hết với dung dịch
HNO
3
dư, thu được dung dịch Y chỉ chứa một muối nitrat duy nhất và 2V lít hỗn hợp khí (đktc) gồm NO và
SO
2
.
Phần trăm khối lượng của Fe trong X là A. 45,9% B. 54,1% C. 43,9% D. 52,1%
Đọc tiếp
Hỗn hợp X gồm Fe và FeS. Cho m gam X tác dụng hết với dung dịch HCl dư, thu được V lít khí (đktc). Mặt khác, m gam X tác dụng hết với dung dịch HNO 3 dư, thu được dung dịch Y chỉ chứa một muối nitrat duy nhất và 2V lít hỗn hợp khí (đktc) gồm NO và SO 2 . Phần trăm khối lượng của Fe trong X là
A. 45,9%
B. 54,1%
C. 43,9%
D. 52,1%
cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư) , tgu được 2,464 lít hỗn hợp khí ( điều kiện tiêu chuẩn ) . Cho hỗn hợp khí này đi qua dung dịch Pb(NO) (dư) , thu được 2,39 gam kết tủa màu đen : a) viết phương trình hóa học của các phản ứng xảy ra ; b) hỗn hợp khí thu được gồm những khí nào ? Thể tích mỗi khí thu được là bao nhiêu ? ; c) tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu ?
Đọc tiếp
cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư) , tgu được 2,464 lít hỗn hợp khí ( điều kiện tiêu chuẩn ) . Cho hỗn hợp khí này đi qua dung dịch Pb(NO) (dư) , thu được 2,39 gam kết tủa màu đen : a) viết phương trình hóa học của các phản ứng xảy ra ; b) hỗn hợp khí thu được gồm những khí nào ? Thể tích mỗi khí thu được là bao nhiêu ? ; c) tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu ?
cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư) , tgu được 2,464 lít hỗn hợp khí ( điều kiện tiêu chuẩn ) . Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 (dư) , thu được 2,39 gam kết tủa màu đen : a) viết phương trình hóa học của các phản ứng xảy ra ; b) hỗn hợp khí thu được gồm những khí nào ? Thể tích mỗi khí thu được là bao nhiêu ? ; c) tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu ?
Đọc tiếp
cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư) , tgu được 2,464 lít hỗn hợp khí ( điều kiện tiêu chuẩn ) . Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 (dư) , thu được 2,39 gam kết tủa màu đen : a) viết phương trình hóa học của các phản ứng xảy ra ; b) hỗn hợp khí thu được gồm những khí nào ? Thể tích mỗi khí thu được là bao nhiêu ? ; c) tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu ?
a)Fe + 2HCl ->FeCl2 + H2\(\uparrow\)
0.01 0.01
FeS + 2HCl ->FeCl2 + H2S\(\uparrow\)
0.1 0.1
H2S + Pb(NO3)2->PbS \(\downarrow\) + 2HNO3
0.1 0.1
nPbS =2.39/239=0.1 mol , n (hỗn hợp khí) =2.464/22.4=0.11 mol
n(H2)+n(H2S)=0.11 ->n(H2)=0.01 mol
V(H2)=n * 22.4 = 0.01*22.4=0.224(l)
V(H2S)=n*22.4=0.1*22.4=2.24(l)
m(Fe)=n*M=0.01*56=0.56(g)
m(FeS)=n*M=0.1*88=8.8(g)
Đúng 0
Bình luận (0)
Hòa tan hỗn hợp gồm Fe và FeS vào dung dịch HCl dư, thu được 8,96 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch
Pb
NO
3
2
dư thì thu được 23,9 gam kết tủa đen. Khối lượng Fe trong hỗn hợp đầu là A. 11,2 B. 16,8 C. 5,6 D. 8,4
Đọc tiếp
Hòa tan hỗn hợp gồm Fe và FeS vào dung dịch HCl dư, thu được 8,96 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb NO 3 2 dư thì thu được 23,9 gam kết tủa đen. Khối lượng Fe trong hỗn hợp đầu là
A. 11,2
B. 16,8
C. 5,6
D. 8,4
Hòa tan hỗn hợp gồm Fe và FeS vào dung dịch HCl dư, thu được 8,96 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 dư thì thu được 23,9 gam kết tủa đen. Khối lượng Fe trong hỗn hợp đầu là:
A. 11,2
B. 16,8
C. 5,6
D. 8,4
Cho hỗn hợp Fe và FeS vào dung dịch HCl (dư) thu được 2,24 lít hỗn hợp khí (ở đktc) có tỉ khối so với H2 là 9. Thành phần % số mol của Fe trong hỗn hợp trên là:
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
Đặt nH2 = x mol; nH2S = y mol
Ta có: nkhí = x + y = 0,1 mol;
mkhí = 2x + 34y = 0,1.9.2 = 1,8 gam
Giải hệ ta có: x = 0,05 và y = 0,05
Suy ra nFe = 0,05. nFeS = 0,05 mol.
Vậy %nFe = 50%.
Đúng 2
Bình luận (1)
\(n_{\uparrow}=\dfrac{2,24}{22,4}=0,1mol\)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{FeS}=y\left(mol\right)\end{matrix}\right.\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
\(\Rightarrow x+y=0,1\left(1\right)\)
\(d_{\uparrow}\)/H2=9\(\Rightarrow\overline{M_{\uparrow}}=9\cdot2=18\)
Sơ đồ chéo:
Fe 56 70
18
FeS 88 38
\(\Rightarrow\dfrac{n_{Fe}}{n_{FeS}}=\dfrac{70}{38}=\dfrac{35}{19}=\dfrac{x}{y}\)(2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{7}{108}\\y=\dfrac{19}{540}\end{matrix}\right.\)
\(\%Fe=\dfrac{\dfrac{7}{108}}{\dfrac{7}{108}+\dfrac{19}{540}}\cdot100\%=64,81\%\)
Đúng 3
Bình luận (1)
Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl dư , thu được 2,464 lít hỗn hợp khí X(đktc). Cho hỗn hợp khí này qua dung dịch Pb(NO3)2 dư thu 23,9g kết tủa màu đen . thể tích các khí trong hỗn hợp khí X là: A. 0,224 lít và 2,24 lít B. 0,124 lít và 1,24 lít C. 0,224 lít và 3,24 lít D. Kếtquả khác
Đọc tiếp
Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl dư , thu được 2,464 lít hỗn hợp khí X(đktc). Cho hỗn hợp khí này qua dung dịch Pb(NO3)2 dư thu 23,9g kết tủa màu đen . thể tích các khí trong hỗn hợp khí X là:
A. 0,224 lít và 2,24 lít
B. 0,124 lít và 1,24 lít
C. 0,224 lít và 3,24 lít
D. Kếtquả khác