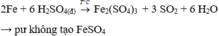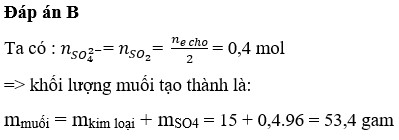so sánh lượng khí sinh ra khi cho cùng 1 lượng Fe lần lượt tác dụng hết với axit sunfuric loãng, dư và axit sunfuric đặc nóng, dư (tạo sản phẩm khử duy nhất là SO2)
- 1 lượng Fe lần lượt tác dụng hết với axit sunfuric loãng, dư và axit sunfuric đặc nóng, dư
Fe + H2SO4 => FeSO4 + H2
1___________1_____________
2Fe + 6H2SO4 => Fe2(SO4)3 + 3SO2 + 6H2O
1_______________1,5________________
=> nH2 < nSO2
Nên lượng khí sinh ra khi cho Fe tác dụng với H2SO4 đặc nóng lớn hơn khi cho Fe tác dụng vs H2SO4 loãng
Đúng 0
Bình luận (0)
Cho 8,37 gam hỗn hợp (Fe, Cu, Al) tác dụng hoàn toàn với lượng dư axit
H
2
S
O
4
đặc nóng được 0,2 mol
S
O
2
là sản phẩm khử duy nhất. Khối lượng muối tạo thành là A. 27,57 gam B. 21,17 gam C. 46,77 gam D. 11,57 gam
Đọc tiếp
Cho 8,37 gam hỗn hợp (Fe, Cu, Al) tác dụng hoàn toàn với lượng dư axit H 2 S O 4 đặc nóng được 0,2 mol S O 2 là sản phẩm khử duy nhất. Khối lượng muối tạo thành là
A. 27,57 gam
B. 21,17 gam
C. 46,77 gam
D. 11,57 gam
Cho 21,4 gam hỗn hợp Al và Fe2O3 tác dụng hết với 51,5 ml dung dịch H2SO4 đặc (d = 1,84 g/ml), đun nóng thu được 6,72 lít khí SO2 (sản phẩm khử duy nhất, đktc). Tính nồng độ % của axit sunfuric, biết lượng axit đã dùng dư 5% so với lượng cần thiết?
\(m_{dd.H_2SO_4}=51,5.1,84=94,76\left(g\right)\)
\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6H2SO4 --> Al2(SO4)3 + 3SO2 + 6H2O
0,2<----0,6<--------------------0,3
=> mAl = 0,2.27 = 5,4 (g)
=> \(n_{Fe_2O_3}=\dfrac{21,4-5,4}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
0,1--->0,3
=> \(m_{H_2SO_4\left(lý.thuyết\right)}=\left(0,6+0,3\right).98=88,2\left(g\right)\)
=> \(m_{H_2SO_4\left(tt\right)}=88,2.105\%=92,61\left(g\right)\)
=> \(C\%=\dfrac{92,61}{94,76}.100\%=97,7\%\)
Đúng 1
Bình luận (0)
Khi cho kim loại tác dụng với dung dịch H2SO4 (đặc, nóng), thu được muối sunfat, các sản phẩm chứa lưu huỳnh (như H2S, S hoặc SO2), không thu được khí H2. Hòa tan 32,3 gam hỗn hợp X gồm Zn và Cu trong m gam dung dịch H2SO4 78,4% (đặc, nóng). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít (đktc) khí SO2 (sản phẩm khí duy nhất), dung dịch Y và 9,6 gam hỗnhợp Z gồm 2 chất rắn có tỷ lệ số mol 1:1.a)Viết các phương trình hóa học xảy ra.b) Tính thành phần phần trăm theo khối lượng của mỗi kim lo...
Đọc tiếp
Khi cho kim loại tác dụng với dung dịch H2SO4 (đặc, nóng), thu được muối sunfat, các sản phẩm chứa lưu huỳnh (như H2S, S hoặc SO2), không thu được khí H2. Hòa tan 32,3 gam hỗn hợp X gồm Zn và Cu trong m gam dung dịch H2SO4 78,4% (đặc, nóng). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít (đktc) khí SO2 (sản phẩm khí duy nhất), dung dịch Y và 9,6 gam hỗn
hợp Z gồm 2 chất rắn có tỷ lệ số mol 1:1.
a)Viết các phương trình hóa học xảy ra.
b) Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp X và tìm m.
Khi cho kim loại tác dụng với dung dịch H2SO4 (đặc, nóng), thu được muối sunfat, các sản phẩm chứa lưu huỳnh (như H2S, S hoặc SO2), không thu được khí H2. Hòa tan 32,3 gam hỗn hợp X gồm Zn và Cu trong m gam dung dịch H2SO4 78,4% (đặc, nóng). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít (đktc) khí SO2 (sản phẩm khí duy nhất), dung dịch Y và 9,6 gam hỗn hợp Z gồm 2 chất rắn có tỷ lệ số mol 1:1. Viết các phương trình hóa học xảy ra, tính thành phần phần trăm theo khối lượng của mỗi kim loại...
Đọc tiếp
Khi cho kim loại tác dụng với dung dịch H2SO4 (đặc, nóng), thu được muối sunfat, các sản phẩm chứa lưu huỳnh (như H2S, S hoặc SO2), không thu được khí H2. Hòa tan 32,3 gam hỗn hợp X gồm Zn và Cu trong m gam dung dịch H2SO4 78,4% (đặc, nóng). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít (đktc) khí SO2 (sản phẩm khí duy nhất), dung dịch Y và 9,6 gam hỗn hợp Z gồm 2 chất rắn có tỷ lệ số mol 1:1. Viết các phương trình hóa học xảy ra, tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp X và tìm m.
Cho 12.6 (g) hỗn hợp Mg và Al theo thỉ lệ mol 3:2 tác dụng với H2SO4 đặc nóng vừa đủ thu đc 0,15 mol sản phẩm?
khử duy nhất là lưu huỳnh..Xác định sản phẩm trên là SO2,S hay H2S
n Mg = a
n Al = b
=> 24a + 27b = 12,6
Tỉ lệ mol => 2a - 3b = 0
Tìm dc a = 0,3 và b = 0,3
Tổng mol e nhường = 0,2*2 + 0,3*3 = 1,2
Tổng mol e nhận: 0,15
=> số oxh của spk của pứ = 1,2 / 0,15 = 8
=> H2S
( S[+6] + 8e = S[-2] )
Đúng 0
Bình luận (1)
n Mg = a
n Al = b
=> 24a + 27b = 12,6
Tỉ lệ mol => 2a - 3b = 0
Tìm dc a = 0,3 và b = 0,3
Tổng mol e nhường = 0,2*2 + 0,3*3 = 1,2
Tổng mol e nhận: 0,15
=> số oxh của spk của pứ = 1,2 / 0,15 = 8
=> H2S
( S[+6] + 8e = S[-2] )
Đúng 0
Bình luận (0)
Khi cho kim loại Fe tác dụng với axit
H
2
S
O
4
đặc, nóng, dư không tạo thành sản phẩm nào trong các sản phẩm sau đây? A. FeS
O
4
B.
H
2
O C. S
O
2
D.
F
e
2
(...
Đọc tiếp
Khi cho kim loại Fe tác dụng với axit H 2 S O 4 đặc, nóng, dư không tạo thành sản phẩm nào trong các sản phẩm sau đây?
A. FeS O 4
B. H 2 O
C. S O 2
D. F e 2 ( S O 4 ) 3
Cho 15 gamhỗn hợp (Fe, Cu, Al) tác dụng hoàn toàn với lượng dư axit H 2 S O 4 đặc nóngđược 0,4 mol S O 2 là sản phẩm khử duy nhất. Khối lượng muối tạo thành là
A. 45,6 gam
B. 53,4 gam
C. 48,77 gam
D. 34,2 gam
Cho các chất tham gia phản ứng: a, S + F2 b, SO2 + H2S c, SO2 + O2 d, S + H2SO4(đặc nóng) e, H2S + Cl2 + H2O f, FeS2 + HNO3 Khi các điều kiện (xúc tác, nhiệt độ) có đủ, số phản ứng tạo ra sản phẩm chứa lưu huỳnh ở mức số oxi hoá +6 là A. 4 B. 3 C. 5 D. 2
Đọc tiếp
Cho các chất tham gia phản ứng:
a, S + F2
b, SO2 + H2S
c, SO2 + O2
d, S + H2SO4(đặc nóng)
e, H2S + Cl2 + H2O
f, FeS2 + HNO3
Khi các điều kiện (xúc tác, nhiệt độ) có đủ, số phản ứng tạo ra sản phẩm chứa lưu huỳnh ở mức số oxi hoá +6 là
A. 4
B. 3
C. 5
D. 2
Đáp án : A
Các phản ứng thỏa mãn : a , c , e , f
Đúng 0
Bình luận (0)
Cho các chất tham gia phản ứng: (1): S+ F2 (2): SO2 + H2S (3): SO2 + O2 (4): S+H2SO4(đặc,nóng) (5): H2S + Cl2 (dư ) + H2O (6): FeS2 + HNO3 Khi các điều kiện xúc tác và nhiệt độ có đủ, số phản ứng tạo ra sản phẩm mà lưu huỳnh ở mức số oxi hoá +6 là A. 4. B. 5. C. 2. D. 3.
Đọc tiếp
Cho các chất tham gia phản ứng:
(1): S+ F2
(2): SO2 + H2S
(3): SO2 + O2
(4): S+H2SO4(đặc,nóng)
(5): H2S + Cl2 (dư ) + H2O
(6): FeS2 + HNO3
Khi các điều kiện xúc tác và nhiệt độ có đủ, số phản ứng tạo ra sản phẩm mà lưu huỳnh ở mức số oxi hoá +6 là
A. 4.
B. 5.
C. 2.
D. 3.
Chọn đáp án A
Các phản ứng thỏa mãn : (1)(3) (5)(6)
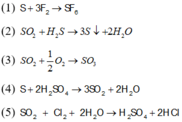
![]()
![]()
Đúng 0
Bình luận (0)