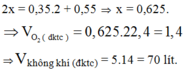Để đốt cháy hoàn toàn 32 gam S cần dùng bao nhiêu lít không khí ở đktc? (S = 32) (Biết oxi chiếm 1/5 thể tích không khí và sản phẩm thu được là khí SO2) A. 112 lít B. 224 lít C. 336 lít D. 448 lít

Những câu hỏi liên quan
Để đốt cháy hoàn toàn m gam lưu huỳnh cần 22,4 lít không khí, thu được V lít khí lưu huỳnh đioxit. Biết các khí đo ở đktc và khí oxi chiếm 20% thể tích không khí. Tìm giá trị của m và V. (Cho S = 32)
PTHH: \(S+O_2\xrightarrow[]{t^o}SO_2\)
Theo PTHH: \(V_{O_2}=22,4\cdot20\%=4,48\left(l\right)=V_{SO_2}\)
\(\Rightarrow n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_S\) \(\Rightarrow m_S=0,2\cdot32=6,4\left(g\right)\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp A gồm 4,8 gam C và 6,4 gam S cần dùng vừa đủ V lít không khí (đktc) . Sau phản ứng thu được hỗn hợp khí B ( gồm CO2 và SO2 ) . Biết trong không khí oxi chiếm 20% và khí nitơ chiếm 80% về thể tích .
a, Viết các phương trình hóa học của phản ứng và tính V
b, Tính khối lượng mol trung bình của B
nC = 4,8/12 = 0,4 mol
nS = 6,4/32 = 0,2 mol
a. C + O2 -> (nhiệt độ) CO2
S + O2 -> (nhiệt độ) SO2
nO2 = nC + nS = 0,6 mol
=> nN2 = 4 x nO2 = 2,4 mol
=> n không khí = 3 mol => V = 67,2 L
b. mB = 44 x 0,4 + 64 x 0,2 = 30,4 g
nB = 0,6 mol
=> M(trung bình của B) = 30,4/0,6 = 50,67 g/mol
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là: A. 70,0 lít B. 78,4 lít C. 84,0 lít D. 56,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít
Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có:
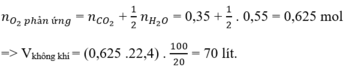
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là : A. 78,4 lít B. 56,0 lít C. 70,0 lít D. 84,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là :
A. 78,4 lít
B. 56,0 lít
C. 70,0 lít
D. 84,0 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiêm gồm: metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là A. 84,0 lít B. 70,0 lít C. 78,4 lít D. 56,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiêm gồm: metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 84,0 lít
B. 70,0 lít
C. 78,4 lít
D. 56,0 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là A. 70,0 lít B. 84,0 lít C. 56,0 lít. D. 78,4 lít.
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 70,0 lít
B. 84,0 lít
C. 56,0 lít.
D. 78,4 lít.
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là: A. 70,0 lít. B. 78,4 lít. C. 84,0 lít. D. 56,0 lít.
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít.
B. 78,4 lít.
C. 84,0 lít.
D. 56,0 lít.
Câu 4. Đốt cháy hoàn toàn 1,12 lít khí C2H4, dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thu được m(g) kết tủa. a. Tính m b. Tính thể tích oxi và thể tích không khí cần dùng.( Biết thể tích khí đo ở đktc, oxi chiếm 20% thể tích không khí,
Đọc tiếp
Câu 4. Đốt cháy hoàn toàn 1,12 lít khí C2H4, dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thu được m(g) kết tủa.
a. Tính m
b. Tính thể tích oxi và thể tích không khí cần dùng.
( Biết thể tích khí đo ở đktc, oxi chiếm 20% thể tích không khí,
a, \(n_{C_2H_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=2n_{C_2H_4}=0,1\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,1.100=10\left(g\right)\)
b, Theo PT: \(n_{O_2}=3n_{C_2H_4}=0,15\left(mol\right)\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=16,8\left(l\right)\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn V lít khí metan trong lọ chứa khí
oxi.
a. Dẫn toàn bộ sản phẩm cháy vào dung dịch bari hidroxit thì thu được 39,4 gam một chất kết tủa màu trắng . Tính V (khí đo ở đktc) ?
b. Nếu đốt lượng khí metan trên trong lọ chứa 13,44 lít khí oxi thì sau phản ứng chất nào dư ? Dư bao nhiêu lít ?
c. Nếu dùng không khí để đốt thì cần bao nhiêu lit không khí ? Biết rằng Voz = 1/5 VKK
Xem chi tiết
Cần gấp ạ !!