hãy cho biết trong thì nghiệm , người ta dùng hóa chất nào để điều khí H2.viết ít nhất 2 phương trình hóa học minh họa
help me với
Trong phòng thí nghiệm, người ta dùng khí hidro (H2) để khử 40 gam sắt (III) Oxit (F*e_{2}*O_{3}) a/ Viết phương trình hóa học xãy ra? b/ Tinh khối lượng sắt thu được? c/ Nếu người ta dùng 0.3 mol khí hidro để khử , thì sau phản ứng chất Cho biết : Fe = 56 O = 16, H = 1 nào dư?
a. \(PTHH:3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\)
b. \(n_{Fe_2O_3}=\dfrac{m_{Fe_2O_3}}{M_{Fe_2O_3}}=\dfrac{40}{160}=0,25\left(mol\right)\)
- Mol theo PTHH : \(3:1:2:3\)
- Mol theo phản ứng : \(0,75\leftarrow0,25\rightarrow0,5\rightarrow0,75\)
\(\Rightarrow n_{Fe}=0,5\left(mol\right)\)
\(\Rightarrow m_{Fe}=n_{Fe}.M_{Fe}=0,5.56=28\left(g\right)\)
c. Ta có : \(n_{Fe_2O_3}=0,25\left(mol\right);n_{H_2}=0,3\left(mol\right)\)
Do \(0,25< 0,3\) ⇒ H2 dư.
Trong phòng thí nghiệm, người ta dùng khí hidro (H2) để khử 40 gam sắt (III) Oxit (F*e_{2}*O_{3}) a/ Viết phương trình hóa học xãy ra? b/ Tinh khối lượng sắt thu được? c/ Nếu người ta dùng 0.3 mol khí hidro để khử , thì sau phản ứng chất Cho biết : Fe = 56 O = 16, H = 1 nào dư?
để điều chế cùng 1 thể tích khí oxi có thể nhiệt phân KMnO4 và KCLO3 . hãy cho biết khối lượng chất nào đã dùng là ít nhất . viết phương trình hóa học và giải thích ............. cần gấp
\(Coi\ n_{O_2} = 1(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 +O_2\\ n_{KMnO_4} = 2n_{O_2} = 2(mol)\\ m_{KMnO_4} = 2.158 = 316(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{KClO_3} = \dfrac{2}{3}(mol)\\ m_{KClO_3} = \dfrac{2}{3}.122,5= 81,6(gam)\\ m_{KClO_3} < m_{KMnO_4} (81,6 <316)\\ \)
Có một bạn học sinh cho rằng: 1 Dùng khí Có hoặc H2 có thể khử các oxit nung nóng sau đây: Fe3O4, CuO,PbO,FexOy về dạng đơn chất 2 Dùng các chất giàu oxi:KCLO3,KMnO4, Hgo, H2O để điều chế O2 trong phòng thí nghiệm Hãy viết các phương trình hóa học mình họa, ghi rõ điều kiện phản ứng
Câu 9. 10/ Cho 16,2g ZnO t ác dụng vói khí H2 đun nóng. a/ Viết phương trình hóa học của phản ứng?
b/ Tính thể tích H2 (đktc) đã dùng? c/ Tính khối lượng Zn điều chế được
10 Trong ph òng th í nghiệm người ta dùng khí CO để khử Fe3O4 v à H2 để khử Fe2O3 ở nhiệt độ cao . trong mỗi pư trên điều có 0,1mol mỗi loại ôxit sắt tham gia
a/ Tính thể tích CO và H2 (đktc) đã dùng? b/ Tính khối lượng kim loại Fe thu được sau mỗi pư
nZnO = 16,2 : 81 = 0,2(mol)
pthh : ZnO + H2 -t--> Zn + H2O
0,2--->0,2-----> 0,2 (mol)
=> VH2 = 0,2 .22,4 = 4,48 (l)
=> mZn = 0,2 . 65 = 13 (g)
2
Fe3O4 + 4CO -t--> 3Fe + 4CO2
0,1-------> 0,4 -------->0,3 (mol)
Fe2O3 + 3H2 -t--> 2Fe + 3H2O
0,1------->0,3 -------->0,2 (mol)
=> VH2 = 0,3 .22,4 = 6,72(L)
=> VCO = 0,2 . 22,4 = 4,48 (L)
mFe= (0,3 + 0,2 ) . 56 = 28 (g)
9.
\(n_{ZnO}=\dfrac{16,2}{81}=0,2mol\)
\(ZnO+H_2\rightarrow\left(t^o\right)Zn+H_2O\)
0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
\(m_{Zn}=0,2.65=13g\)
10.
\(Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)
0,1 0,4 0,3 ( mol )
\(V_{H_2}=0,4.22,4=8,96l\)
\(m_{Fe}=0,3.56=16,8g\)
\(Fe_3O_4+4CO\rightarrow\left(t^o\right)3Fe+4CO_2\)
0,1 0,4 0,3 ( mol )
\(V_{CO}=0,4.22,4=8,96l\)
\(m_{Fe}=0,3.56=16,8g\)
Hình bên là bộ dụng cụ dùng để điều chế một số khí trong phòng thí nghiệm.
(a) Khí C nào trong số các khí sau: H2, C2H2, SO2, Cl2, CO và HCl có thể được điều chế bằng bộ dụng cụ bên?
(b) Hãy chọn các chất A và B tương ứng để điều chế các khí C được chọn và viết các phương trình hóa học tương ứng.
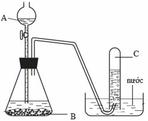
(a) Từ hình ảnh bộ dụng cụ ta thấy đây là bộ dụng cụ để điều chế các khí không tác dụng được với nước, và không tan hoặc rất ít tan trong nước
=> khí C có thể điều chế được là các khí: H2, C2H2, SO2
Cl2 và HCl không điều chế được vì tan trong nước
CO không điều chế được bằng bộ dụng cụ này trong phòng thí nghiệm.
(b)
Điều chế: H2 ; A có thể là HCl hoặc H2SO4 loãng ; B là có thể là kim loại Zn, Fe…
2HCl + Zn → ZnCl2 + H2↑
Điều chế: C2H2; A là H2O ; B là CaC2 rắn
2H2O + CaC2 → Ca(OH)2 + C2H2↑
Điều chế: SO2 ; A là HCl ; B là Na2SO3 rắn
2HCl + Na2SO3 → 2NaCl + SO2↑ + H2O
Dùng phương pháp hóa học để nhận biết các chất khí riêng biệt đựng trong các bình mất nhãn: CO2, SO2, C2H4, CH4, H2, N2 (trình bày theo phương pháp kẻ bảng và viết phương trình hóa học minh họa).
Trong phòng thí nghiệm có 3 lọ hóa chất không màu gồm: dung dịch HCl, dung dịch H2SO4 loãng, nước cất. Em hãy trình bày phương pháp hóa học dùng để nhận biết mỗi lọ hóa chất đó. Viết phương trình hóa học minh họa (nếu có
Dùng quỳ tím:
+ Chuyển màu là \(H_2SO_4,HCl\)
+ Không chuyển màu là nước cất
Dùng \(BaCl_2\):
+ Tạo phản ứng kết tủa: \(H_2SO_4\)
+ Không phản ứng: \(HCl\)
\(PTHH:H_2SO_4+BaCl_2\rightarrow BaSO_4+2HCl\)
Trong phòng thí nghiệm, quá trình điều chế khí Z thường bị lẫn SO2. Để loại bỏ SO2 ra khỏi hỗn hợp khí gồm Z và SO2, có thể dùng dung dịch chứa chất nào trong các chất ( riêng biệt) sau đây: BaCl2, Ca(OH)2, Br2 và K2SO3? Giải thích và viết phương trình hóa học minh họa cho các phản ứng.
Trong phòng thí nghiệm, quá trình điều chế khí Z thường bị lẫn SO2 nên Z là C2H4.
Vậy để tách SO2 ra khỏi hỗn hợp C2H4 và SO2 ta có thể dùng các chất: Ca(OH)2, K2SO3.
PTHH:
SO2 + Ca(OH)2 → CaSO3↓ + H2O
K2SO3 + SO2 + H2O → 2KHSO3