Khí A có cấu tạo gồm C,H và có tỉ khối so với không khí là 0,552 . Công Thức của A là A.CH4 B.C2H4 C.C2H6. D.C2H2

Những câu hỏi liên quan
Biết rằng khí A có tỉ khối đối với không khí là 0,552. Thành phần khí A gồm C và H. Tỉ lệ khối lượng của C và H trong khí A là 3:1.
Xác định công thức hoá học của A
\(\%C = \dfrac{3}{3 +1}.100\% = 75\%\\ \%H = \dfrac{1}{3 + 1}.100\% = 25\%\)
\(M_A = 0,522.29 = 16(đvC)\)
Số nguyên tử C = \(\dfrac{16.75\%}{12} = 1\)
Số nguyên tử H = \(\dfrac{16.25\%}{1} = 4\)
Vậy CTHH của A : \(CH_4\)
Đúng 2
Bình luận (2)
Khí X có tỉ khối so với không khí là 0,552 gồm 2 nguyên tố trong đó có75%C còn lại là H hãy xác định công thức hóa học của x
MX = 0,552.29 = 16 (g/mol)
\(m_C=\dfrac{16.75}{100}=12\left(g\right)=>n_C=\dfrac{12}{12}=1\left(mol\right)\)
\(m_H=16-12=4\left(g\right)=>n_H=\dfrac{4}{1}=4\left(mol\right)\)
=> CTHH: CH4
Đúng 1
Bình luận (0)
Hãy tìm thể tích khí oxi đủ để đốt cháy hết 11,2 lít khí A.
Biết rằng:
- Khí A có tỉ lệ khối đối với không khí là 0,552.
- Thành phần theo khối lượng của khí A là: 75% C và 25% H.
Các thể tích khí đo ở đktc.
dA/kk = 0,552 ⇒ Khối lượng mol của khí A: 29.0,552 = 16 (g)
Đặt CTHH của khí A là CxHy
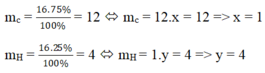
Công thức hóa học của khí A là: CH4
PTPỨ:

Tỉ lệ số mol cũng chính là tỉ lệ thể tích.
Theo phương trình nO2 = 2.nCH4 ⇒ VO2 = 2.VCH4 = 2.11,2 = 22,4(l)
Đúng 0
Bình luận (0)
Hãy tìm thể tích khí oxi đủ để đốt cháy hết 11,2 lít khí A. Biết rằng: – Khí A có tỉ lệ khối đối với không khí là 0,552. Thành phần theo khối lượng của khí A là: 75% C và 25% H (Các thể tích khí đo ở đktc)
Ta có: \(M_A=0,552.29=16\)
Gọi CTTQ của A là \(C_xH_y\) (với x;y thuộc N*)
Ta có: \(x:y=\dfrac{\%m_C}{M_C}:\dfrac{\%m_H}{M_H}=\dfrac{75\%}{12}:\dfrac{25\%}{1}=0,0625:0,25=1:4\)
Suy ra CTDGN của A là \(\left(CH_4\right)_n\)
Mặt khác \(16.n=16\Rightarrow n=1\)
Vậy A là CH4
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=2.\dfrac{11,2}{22,4}=1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=22,4\left(l\right)\)
Đúng 1
Bình luận (0)
Khí A có tỉ số đối với không khí là 0,552 và có thành phần khối lượng 75%C , 25%H. Nếu đốt 11,2 lít A(đktc) thì thể tích Oxi cần dùng là bao nhiêu ?
\(M_A =29.0,552 = 16(đvC)\)
Số nguyên tử C = \(\dfrac{16.75\%}{12} = 1\)
Số nguyên tử H = \(\dfrac{16.25\%}{1} = 4\)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\)
Theo PTHH :
\(V_{O_2} = 2V_{CH_4} = 11,2.2 = 22,4(lít)\)
Đúng 1
Bình luận (1)
Hãy tìm thể tích khí oxi đủ để đốt cháyheets 11,2 lít khí A
Biết rằng:
- Khí A có tỉ khối với không khí là 0,552.
- Thành phần theo khối lượng của khí A là: 75% C và 25% H.
Các thể tích khí đo ở đktc.
Cho m gam chất hữu cơ A có công thức phân tử C4H14O3N2 tác dụng với 400 gam dung dịch KOH 5,6% thu được 0,2 mol hỗn hợp khí B gồm 2 khí điều kiện thường đều làm xanh quỳ tím ẩm có tỉ khối so với H2 là 19 và dung dịch C. Cô cạn dung dịch C thu được a gam chất rắn khan. Giá trị của a và số công thức cấu tạo phù hợp với A là A. 38,8 và 1 B. 40,8 và 4 C. 40,8 và 2 D. 25 và 3
Đọc tiếp
Cho m gam chất hữu cơ A có công thức phân tử C4H14O3N2 tác dụng với 400 gam dung dịch KOH 5,6% thu được 0,2 mol hỗn hợp khí B gồm 2 khí điều kiện thường đều làm xanh quỳ tím ẩm có tỉ khối so với H2 là 19 và dung dịch C. Cô cạn dung dịch C thu được a gam chất rắn khan. Giá trị của a và số công thức cấu tạo phù hợp với A là
A. 38,8 và 1
B. 40,8 và 4
C. 40,8 và 2
D. 25 và 3
Đun hỗn hợp gồm ancol A và axit B (đều là chất có cấu tạo mạch hở, không phân nhánh) thu được este X. Đốt cháy hoàn toàn m gam X thu được 1,344 lít khí CO2 (đktc) và 0,72 gam nước. Lượng oxi cần dùng là 1,344 lít (đktc). Biết tỉ khối hơi của X so với không khí nhỏ hơn 6. Công thức phân tử của X là: A. C3H4O2 B. C6H8O4 C. C3H2O2 D. Đáp án khác
Đọc tiếp
Đun hỗn hợp gồm ancol A và axit B (đều là chất có cấu tạo mạch hở, không phân nhánh) thu được este X. Đốt cháy hoàn toàn m gam X thu được 1,344 lít khí CO2 (đktc) và 0,72 gam nước. Lượng oxi cần dùng là 1,344 lít (đktc). Biết tỉ khối hơi của X so với không khí nhỏ hơn 6. Công thức phân tử của X là:
A. C3H4O2
B. C6H8O4
C. C3H2O2
D. Đáp án khác
Hỗn hợp khí gồm H2 và anken có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất. Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu tạo của anken là: A. CH3-CH CH-CH3 B. CH2CH-CH2-CH3 C. CH2 C(CH3)2 D. CH2 CH2
Đọc tiếp
Hỗn hợp khí gồm H2 và anken có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất. Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu tạo của anken là:
A. CH3-CH = CH-CH3
B. CH2=CH-CH2-CH3
C. CH2 =C(CH3)2
D. CH2 =CH2
Đáp án A
Giả sử có 1 mol hỗn hợp X gồm H2 và anken ![]()
Ta có:
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
![]()
![]()
Phương trình phản ứng:
![]()
Ta có: nX = 1 mol; nY = 0,7 mol
![]()
![]()
Ta có: anken đó là C4H8
X phản ứng với HBr cho 1 sản phẩm duy nhất nên X là But-2-en
Đúng 0
Bình luận (0)














