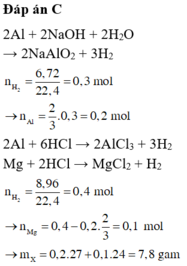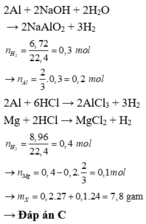Cho 4,8 gam Mg tác dụng vừa đủ với dung dịch HCl, sau phản ứng thu được sản phẩm
gồm MgCl2 và V lít khí H2. Biết thể tích khí đo ở điều kiện chuẩn 25oC, 1bar. Giá trị của V là ? (Mg: 24; Cl: 35,5; H: 1). Biết PTHH là: Mg + 2HCl→MgCl2+ H2

Những câu hỏi liên quan
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 6,45
B. 10,2
C. 7,8
D. 14,55
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí . Mặt khác, cho m gam hỗn hợp tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
A. 10,20.
B. 6,45.
C. 7,80.
D. 14,55.
Đáp án C
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
![]()
![]()
2Al + 6HCl → 2AlCl3 + 3H2
Mg + 2HCl → MgCl2 + H2![]()
![]()
![]()
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí . Mặt khác, cho m gam hỗn hợp tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của m là A. 10,20. B. 6,45. C. 7,80. D. 14,55.
Đọc tiếp
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí . Mặt khác, cho m gam hỗn hợp tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
A. 10,20.
B. 6,45.
C. 7,80.
D. 14,55.
Câu 3 (1 điểm). Cho 4,8 gam Mg tác dụng hoàn toàn với dung dịch HCl, sau phản ứng thu được m gam MgCl2 và khí H2 ở điều kiện tiêu chuẩn.
a.Viết phương trình phản ứng xảy ra.
b.Tính thể tích khí tạo thành (tính theo trên trường).
c.Tính m=?.
\(a.Mg+2HCl\rightarrow MgCl_2+H_2\\ b.n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ n_{H_2}=n_{Mg}=0,2\left(mol\right)\\ V_{H_2}=0,2.22,4=4,48\left(l\right)\\ c.n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\\ m_{MgCl_2}=0,2.95=19\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 4,8 gam magnesium Mg tác dụng hoàn toàn với dung dịch hydrochloric acid HCl dư, sau phản ứng thu được V lít khí hydrogen (ở đktc). Giá trị của V là: (biết Mg=24) *
a. 4,48
b. 2,24
c. 9,916
d. 4,958
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của m là A. 10,20 B. 6,45 C. 7,80 D. 14,55
Đọc tiếp
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
A. 10,20
B. 6,45
C. 7,80
D. 14,55
Cho m gam mg phản ứng với dung dịch HCl sau phản ứng thu được MgCl2 và 4,48 lít khí h2 ở điều kiện tiêu chuẩn xác định giá trị của m (mg=24)
Bước 1 chuyển dữ kiện bài về số mol
bước 2 viết phương trình hóa học
bước 3 dựa vào phương trình hóa học suy ra số mol các chất còn lại trên phương trình hóa học
bước 4 tính theo yêu cầu đề bài
Cho 40 gam hỗn hợp gồm Al và Al2O3 tác dụng vừa đủ với V (ml) dung dịch HCl có nồng độ 2 M sau phản ứng thu được 3,785 lít khí ở điều kiện chuẩn Tinh giá trị V
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\left(2\right)\)
\(n_{H_2}=\dfrac{3.785}{24.79}=0.15\left(mol\right)\Rightarrow n_{Al}=\dfrac{2}{3}\cdot0.15=0.1\left(mol\right),n_{HCl\left(1\right)}=0.15\cdot2=0.3\left(mol\right)\)
\(m_{Al}=0.1\cdot27=2.7\left(g\right)\Rightarrow m_{Al_2O_3}=40-2.7=37.3\left(g\right)\Rightarrow n_{Al_2O_3}=\dfrac{37.3}{102}=0.36\left(mol\right)\)
\(\Rightarrow n_{HCl\left(2\right)}=0.36\cdot6=2.16\left(mol\right)\)
\(n_{HCl}=0.3+2.16=2.46\left(mol\right)\)
\(V_{dd_{HCl}}=\dfrac{2.46}{2}=1.23\left(l\right)\)
Đúng 3
Bình luận (0)
Khi cho 3,12 g kim loại mg phản ứng với dung dịch HCl thu được MgCl2 và 2,23 11 lít điều kiện chuẩn khí hidro ở 25°, 1bar tính khối lượng của MgCl2 thu được sau phản ứng tính hiệu suất của phản ứng
\(n_{Mg}=\dfrac{3,12}{24}=0,13\left(mol\right)\)
\(n_{H_2}=\dfrac{2,2311}{25,79}=0,09\left(mol\right)\)
PTHH :
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
0,09 0,18 0,09 0,09
\(\dfrac{0,13}{1}>\dfrac{0,09}{1}\) --> Mg dư
\(m_{MgCl_2}=0,09.95=8,55\left(g\right)\)
Đúng 1
Bình luận (0)
PTHH :
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
0,13 0,26 0,13 0,13
\(V_{H_2\left(lt\right)}=0,13.24,79=3,2227\left(l\right)\)
\(H=\dfrac{2,2311}{3,2227}.100\%\approx69,23\%\)
Đúng 0
Bình luận (1)