Tính số mol của nước có trong 0,8 lít nước. Biết D = 1 g/ml

Những câu hỏi liên quan
Hòa tan m gam rượu etylic ( D = 0,8 g/ml) vào 108 ml nước ( D= 1 g/ml) tạo thành dung dịch A. Cho dung dịch A tác dụng với kim loại Na dư, thu được 85,12 lít khí H2 (đktc). Tính giá trị m và nồng độ mol của rượu etylic
nH2 = 85,12 : 22,4 = 3,8 (mol) ; nH2O = VH2O.D = 108 (g) => nH2O = 108/18 = 6 (mol)
PTHH:
2Na + 2C2H5OH → 2C2H5ONa + H2↑
x → 0,5x (mol)
2Na + 2H2O → 2NaOH + H2↑
6 → 3 (mol)
Ta có: nH2 = 0,5x + 3 = 3,8
=> x = 1,6 (mol) = nC2H5OH
mC2H5OH = 1,6.46 = 73,6 (g)
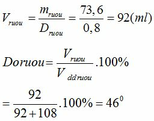
Đúng 0
Bình luận (0)
Bài 9: a) Tính thể tích của hỗn hợp gồm 14 g nitơ và 4 g khí NO.
b) Tính số mol nước có trong 0,8 lít nước. Biết D = 1 g/ml.
a) \(n_{N_2}=\dfrac{14}{28}=0,5\left(mol\right)\)
\(n_{NO}=\dfrac{4}{30}=\dfrac{2}{15}\left(mol\right)\)
\(\Sigma n_{hh}=0,5+\dfrac{2}{15}=\dfrac{19}{30}\left(mol\right)\)
\(\Rightarrow V_{hh}=\dfrac{19}{30}\times22,4=14,867\left(l\right)\)
Đúng 0
Bình luận (0)
b) Đổi 0,8 lít = 800 ml
\(m_{H_2O}=1\times800=800\left(g\right)\)
\(\Rightarrow n_{H_2O}=\dfrac{800}{18}=\dfrac{400}{9}\left(mol\right)\)
Đúng 0
Bình luận (0)
Tính số nguyên tử hiđro có trong 1 lít nước. Biết khối lượng riêng của nước là 1 g/ml.
$m_{H_2O} = 1000.1 = 1000(gam)$
$n_{H_2O} = \dfrac{1000}{18} = \dfrac{500}{9}(mol)$
$n_H = 2n_{H_2O} = \dfrac{1000}{9}(mol)$
Số nguyên tử Hidro = $\dfrac{1000}{9}.6.10^{23} = 6,67.10^{25}$ nguyên tử
Đúng 4
Bình luận (0)
Hòa tan m gam ancol etylic (D 0,8 g/ml) vào 108 ml nước (D 1 g/ml) tạo thành dung dịch X. Cho X tác dụng với Na dư, thu được 85,12 lít (đktc) khí H2. Biết thể tích của X bằng tổng thể tích của ancol và nước. Dung dịch X có độ ancol bằng A. 41o B. 92o C. 46o D. 8o
Đọc tiếp
Hòa tan m gam ancol etylic (D = 0,8 g/ml) vào 108 ml nước (D = 1 g/ml) tạo thành dung dịch X. Cho X tác dụng với Na dư, thu được 85,12 lít (đktc) khí H2. Biết thể tích của X bằng tổng thể tích của ancol và nước. Dung dịch X có độ ancol bằng
A. 41o
B. 92o
C. 46o
D. 8o
Đáp án C
nH2 = 85,12: 22,4 = 3,8 (mol) ; mH2O = VH2O. D = 108 (g) => nH2O = 6 (mol)
Độ rượu = (Vrượu/ Vdd rượu).100%
Na + C2H5OH → C2H5ONa + ½ H2
x →x →x/2 (mol)
Na + H2O → NaOH + ½ H2
6 →3 (mol)
Ta có: x/2 + 3 = 3,8
=> x =1,6 (mol) = nC2H5OH
=> mrượu = 1,6. 46 = 73,6 (g) => Vrượu = mrượu/Drượu = 73,6/ 0,8 = 92 (ml)
=> Độ rượu = [92 / ( 92 + 108)].100% = 460
Đúng 0
Bình luận (0)
Hòa tan m gam ancol etylic (D 0,8 g/ml) vào 108 ml nước (D 1 g/ml) tạo thành dung dịch X. Cho X tác dụng với Na dư, thu được 85,12 lít (đktc) khí H2. Biết thể tích của X bằng tổng thể tích của ancol và nước. Dung dịch X có độ ancol bằng A. 41o. B. 92o. C. 46o. D. 8o
Đọc tiếp
Hòa tan m gam ancol etylic (D = 0,8 g/ml) vào 108 ml nước (D = 1 g/ml) tạo thành dung dịch X. Cho X tác dụng với Na dư, thu được 85,12 lít (đktc) khí H2. Biết thể tích của X bằng tổng thể tích của ancol và nước. Dung dịch X có độ ancol bằng
A. 41o.
B. 92o.
C. 46o.
D. 8o
Đáp án C
nH2 = 85,12: 22,4 = 3,8 (mol) ; mH2O = VH2O. D = 108 (g) => nH2O = 6 (mol)
Độ rượu = (Vrượu/ Vdd rượu).100%
Na + C2H5OH → C2H5ONa + ½ H2
x →x →x/2 (mol)
Na + H2O → NaOH + ½ H2
6 →3 (mol)
Ta có: x/2 + 3 = 3,8
=> x =1,6 (mol) = nC2H5OH
=> mrượu = 1,6. 46 = 73,6 (g) => Vrượu = mrượu/Drượu = 73,6/ 0,8 = 92 (ml)
=> Độ rượu = [92 / ( 92 + 108)].100% = 460
Đúng 0
Bình luận (0)
Hòa tan m gam ancol etylic (D 0,8 g/ml) vào 108ml nước (D 1 g/ml) tạo thành dung dịch X. Cho X tác dụng với Na dư, thu được 85,12 lít (đktc) khí H2. Biết thể tích của X bằng tổng thể tích của ancol và nước. Dung dịch X có độ ancol bằng A. 41o. B. 92o. C. 46o. D. 8o.
Đọc tiếp
Hòa tan m gam ancol etylic (D = 0,8 g/ml) vào 108ml nước (D = 1 g/ml) tạo thành dung dịch X. Cho X tác dụng với Na dư, thu được 85,12 lít (đktc) khí H2. Biết thể tích của X bằng tổng thể tích của ancol và nước. Dung dịch X có độ ancol bằng
A. 41o.
B. 92o.
C. 46o.
D. 8o.
Dung dịch axit sunfuric đặc (D = 1,83 g/ml) chứa 6,4% nước. Hãy cho biết trong 1 lít dung dịch axit này có bao nhiêu mol H 2 SO 4
Một lít H 2 SO 4 đặc có khối lượng là : .
1,83.1000= 1830 (g)
Khối lượng H 2 O có trong 1 lít H 2 SO 4 ặc là :
Khối lượng H 2 SO 4 tinh khiết có trong 1 lít là : 1830- 117,12= 1712,88 (g)
Số mol H 2 SO 4 có trong 1 lít axit sunfuric đặc :
n H 2 SO 4 = 1712,88/98 = 17,48 (mol)
Đúng 0
Bình luận (0)
Bài 9
a) Tính thể tích của hỗn hợp gồm 14 g nitơ và 4 g khí NO.
b) Tính số mol nước có trong 0,8 lít nước. Biết D = 1 g/ml.
a) Ta có :
\(V\left(hh-\text{đ}kt\right)=24.\left(\dfrac{14}{14}+\dfrac{4}{30}\right)=27,2\left(l\right)\)
\(V\left(hh-\text{đ}ktc\right)=22,4.\left(\dfrac{14}{14}+\dfrac{4}{30}\right)\approx25,4\left(l\right)\)
b)
\(Ta-c\text{ó}:mH2O=0,8.1=0,8\left(g\right)=>nH2O=\dfrac{0,8}{18}=\dfrac{2}{45}\left(mol\right)\)
Đúng 0
Bình luận (0)
Cấu 7. Trên chai nước có ghi số 45° a. Hãy giải thích ý nghĩa số ghi trên b. Tính số (ml) rượu có trong 500 (ml) rượu 45° c. Tính khối lượng rượu Etylic có trong 500 (ml) rượu 40°. Biết khối lượng riêng của rượu là 0,8 (g/ml)














