BT:Nung nóng 400g KMnO4 thu được 376g hỗn hợp chất rắn
a)tính khối lượng KMnO4 bị phân huỷ
b)tính thể tích khí oxi thoát ra sau phản ứng ở đktc
c)tính thành phần về khối lượng các chất trong hỗn hợp thu đươc.

Những câu hỏi liên quan
Nung nóng 20 gam hỗn hợp gồm KMnO4 và KClO3, sau một thời gian thu được 18,88 gam chất rắn:
a) Hãy tính khối lượng hỗn hợp chất rắn thu được sau phản ứng.
b) Tính thể tích khí oxi sinh ra trong phản ứng.
a) Sau phản ứng : $m_{chất\ rắn} = 18,88(gam)$
b) Bảo toàn khối lượng :
$m_{O_2} = 20 - 18,8 = 1,12(gam)$
$n_{O_2} = 1,12 : 32 = 0,035(mol)$
$V_{O_2} = 0,035.22,4 = 0,784(lít)$
Đúng 1
Bình luận (0)
Nung m gam hỗn hợp A gồm KMnO4 và KClO3 thu được chất rắn B và khí O2. Lúc đó KClO3 phân hủy hoàn toàn, còn KMnO4 phân hủy không hoàn toàn. Trong B có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn lượng O2 thu được ở trên với không khí (có phần trăm thể tích: 20% O2; 80% N2) theo tỉ lệ thể tích tương ứng là 1:3 tạo thành hỗn hợp khí C. Cho toàn bộ khí C vào bình chứa 0,528 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp khí D gồm 3 khí trong đó O2 chiếm 17,083% về thể tích. a) Tính phần trăm k...
Đọc tiếp
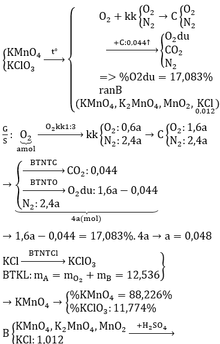
Nung m gam hỗn hợp A gồm KMnO4 và KClO3 thu được chất rắn B và khí O2. Lúc đó KClO3 phân hủy hoàn toàn, còn KMnO4 phân hủy không hoàn toàn. Trong B có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn lượng O2 thu được ở trên với không khí (có phần trăm thể tích: 20% O2; 80% N2) theo tỉ lệ thể tích tương ứng là 1:3 tạo thành hỗn hợp khí C. Cho toàn bộ khí C vào bình chứa 0,528 gam cacbon rồi đốt cháy hết cacbon thu được hỗn hợp khí D gồm 3 khí trong đó O2 chiếm 17,083% về thể tích.
a) Tính phần trăm khối lượng mỗi chất có trong A.
b) Thêm 74,5 gam KCl vào chất rắn B được hỗn hợp E. Cho E vào dung dịch H2SO4 loãng dư, đun nóng nhẹ cho đến phản ứng hoàn toàn. Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn.
1) Để điều chế được 12,32 lít O2 (đxtc) trong phòng thí nghiệm, người ta lấy 79,8 gam hỗn hợp KClO3 và KMnO4 nhiệt phân ở nhiệt độ cao. Tính thành phần phần trăm khối lượng mỗi chất rắn đem nhiệt phân. Sau khi nhiệt phân thì khối lượng chất rắn cìn lại bao nhiêu?2) Toàn bộ khối lượng oxi ở trên được dùng đối chát 11,4 gam cacbon thu được hỗn hợp khí X. Tính thành phần và tỉ khối hỗn hợp khí X sau phản ứng?3) Toàn bộ lượng khí X ở trên cho thổi qua ống sứ chứa 64 gam CuO nung nóng thu được khí Y...
Đọc tiếp
1) Để điều chế được 12,32 lít O2 (đxtc) trong phòng thí nghiệm, người ta lấy 79,8 gam hỗn hợp KClO3 và KMnO4 nhiệt phân ở nhiệt độ cao. Tính thành phần phần trăm khối lượng mỗi chất rắn đem nhiệt phân. Sau khi nhiệt phân thì khối lượng chất rắn cìn lại bao nhiêu?
2) Toàn bộ khối lượng oxi ở trên được dùng đối chát 11,4 gam cacbon thu được hỗn hợp khí X. Tính thành phần và tỉ khối hỗn hợp khí X sau phản ứng?
3) Toàn bộ lượng khí X ở trên cho thổi qua ống sứ chứa 64 gam CuO nung nóng thu được khí Y và hỗn hợp rắn A. Tính khối lượng mỗi chất trong A.
4) Toàn bộ lượng khí Y cho sục qua nước vôi trong dư tạo kết tủa E. Tính khối lượng kết tủa E thu được?
- Hóa 8 ạ -
nhiệt phân hoàn toàn hỗn hợp gồm KMnO4 và KClO3 sau phản ứng thu được 21,65 gam chất rắn A( trong A nguyên tố kali chiếm 36,03% về khối lượng) và khí B. Tính thể tích khí B tạo thành sau phản ứng ở đktc
$n_{Kali} = \dfrac{21,65.36,03\%}{39} = 0,2(mol)$
Gọi $n_{KMnO_4} = a ; n_{KClO_3} = b$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
Bảo toàn Kali : $a + b = 0,2$
$n_{O_2} = 0,5a + 1,5b(mol)$
Bảo toàn khối lượng : $158a + 122,5b = 21,65 + (0,5a + 1,5b).32$
Suy ra: a = b = 0,1
$n_{O_2} = 0,5a + 1,5b = 0,2(mol)$
$V_{O_2} = 0,2.22,4 = 4,48(lít)$
Đúng 1
Bình luận (2)
Đun nóng 48,2gam hỗn hợp X gồm KMnO4 và KClO3 sau một thời gian thu được 43,4gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, đun nóng, sau phản ứng thu được 15,12 lít khí clo (đktc) và dd Z gồm các chất tan MnCl2, KCl, HCl dư. Tính thành phần % về khối lượng của các chất trong hỗn hợp X.
Gọi số mol KMnO4 và KClO3 trong hỗn hợp ban đầu lần lượt là x,y
158x + 122,5y= 48,2 (1)
Bảo toàn elcton toàn quá trình ta có
Mn+7+5e →Mn+2
x 5x
Cl+5 + 6e → Cl–1
y 6y
(về bản chất có 1 phần Cl+5 có 1 phần chuyển sang Cl0, nhưng Cl–1 lại nhường e tạo Cl0 vì vậy để đơn giản ta có thể coi tất cả Cl+5 tạo thành Cl–1)
2Cl–1→ Cl2 +2e
0,675 0,135
2O–2 → O2 + 4e
0,15 0,6
Áp dụng định luật bảo toàn e ta có 5x+6y=1,95 (2)
Từ 1 và 2 ta có hệ phương trình
Giải ta được x=0,15 và y=0,2
% mKMnO4 = 49,17 % và % mKClO3 =50,83%
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 56,1g hỗn hợp gồm KClO3 và KMnO4 ở nhiệt đọ cao,sau phản ứng thu được 8,96 lít khí oxi ở đktc
a)tính thành phần phần trăm khối lượng mỗi chất có trong hỗn hợp đầu
b) Lượng oxi thu được ở trên đốt cháy được khối lượng than có hàm lượng cacbon chiếm 85% (còn lại là tạp chất không cháy)nhiều nhất và ít nhất là bao nhiêu ?
Nhiệt phân hoàn toàn 99,95 gam hỗn hợp KMnO4 và KClO3 sau phản ứng thu đc 14,56 lít khí O2 ở đktc
a) Tính % theo khối lượng mỗi chất có trong hỗn hợp trước phản ứng
b) Tính % khối lượng mỗi chất rắn có trong hỗn hợp sau phản ứng
\(a)n_{KMnO_4} = a; n_{KClO_3} = b\Rightarrow 158a + 122,5b = 99,95(1)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{O_2} = 0,5a +1,5b = \dfrac{14,56}{22,4}=0,65(2)\\ (1)(2)\Rightarrow a = 0,4 ; b = 0,3\\ \%m_{KMnO_4} = \dfrac{0,4.158}{99,95}.100\% = 63,23\%\\ \%m_{KClO_3} = 100\%-63,23\% = 36,77\%\)
\(n_{K_2MnO_4} = n_{MnO_2} = 0,5a = 0,2(mol)\\ n_{KClO_3} = b = 0,3(mol)\\ m_{hh\ sau\ pư} = 99,95 - 0,65.32 = 79,15(gam)\\ \%m_{K_2MnO_4} = \dfrac{0,2.197}{79,15}.100\% = 49,78\%\\ \%m_{MnO_2} = \dfrac{0,2.87}{79,15},100\% = 21,98\%\\ \%m_{KCl} = 28,24\%\)
Đúng 1
Bình luận (0)
![]() ko khó lém bn ơi có câu nèo easy hơm ko
ko khó lém bn ơi có câu nèo easy hơm ko![]()
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 28,05 gam hỗn hợp gồm KClO3 và KMnO4 thì thu được 21,65 gam chất rắn.
a. Tìm thể tích khí H2 thu được ở đktc.
b. Tìm khối lượng các chất trong hỗn hợp ban đầu và các chất trong hỗn hợp sau phản ứng.
\(a) m_{O_2} = 28,05 - 21,65 = 6,4(gam)\\ n_{O_2} = \dfrac{6,4}{32} = 0,2(mol)\\ V_{O_2} = 0,2.22,4 = 4,48(lít)\\ b) n_{KClO_3} =a ; n_{KMnO_4} = b(mol)\\ \Rightarrow 122,5a + 158b = 28,05(1)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{O_2} = 1,5a + 0,5b = 0,2(2) (1)(2)\Rightarrow a = b = 0,1\)
\(m_{KClO_3} = 0,1.122,5 = 12,25(gam)\\ m_{KMnO_4} = 0,1.158 = 15,8(gam)\\ n_{K_2MnO_4} = n_{MnO_2} = 0,5b = 0,05(mol)\\ m_{K_2MnO_4} = 0,05.197 = 9,85(gam)\\ m_{MnO_2} = 0,05.87 = 4,35(gam)\\ n_{KCl} = n_{KClO_3} = 0,1(mol)\\ m_{KCl} = 0,1.74,5 = 7,45(gam)\)
Đúng 2
Bình luận (0)
PT: \(2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
a, Phần này phải là thể tích O2 chứ nhỉ?
Theo ĐLBT KL, có: mKClO3 + mKMnO4 = m chất rắn + mO2
⇒ mO2 = 28,05 - 21,65 = 6,4 (g)
\(\Rightarrow n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\Rightarrow V_{O_2}=0,2.22,4=4,48\left(l\right)\)
b, Giả sử: \(\left\{{}\begin{matrix}n_{KClO_3}=x\left(mol\right)\\n_{KMnO_4}=y\left(mol\right)\end{matrix}\right.\)
⇒ 122,5x + 158y = 28,05 (1)
Theo PT: \(n_{O_2}=\dfrac{3}{2}x+\dfrac{1}{2}y\left(mol\right)\)
\(\Rightarrow\dfrac{3}{2}x+\dfrac{1}{2}y=0,2\left(2\right)\)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
⇒ mKClO3 = 122,5.0,1 = 12,25 (g)
mKMnO4 = 0,1.158 = 15,8 (g)
Theo PT: \(\left\{{}\begin{matrix}n_{KCl}=n_{KClO_3}=0,1\left(mol\right)\\n_{K_2MnO_4}=n_{MnO_2}=\dfrac{1}{2}n_{KMnO_4}=0,05\left(mol\right)\end{matrix}\right.\)
⇒ mKCl = 0,1.74,5 = 7,45 (g)
mK2MnO4 = 0,05.197 = 9,85 (g)
mMnO2 = 0,05.87 = 4,35 (g)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Câu 5: Hỗn hợp A gồm Mg và Fe có tỉ lệ khối lượng tương ứng là 2:3. Cho 8,4 g hỗn hợp A tác dụng hoàn toàn
dung dịch HCl.
a. Tính khối lượng từng chất có trong hỗn hợp A.
b. Tính thể tích khí H2 thoát ra ở đktc
c. Dẫn toàn bộ thể tích khí H2 thu được vào bình đựng 16 g CuO đun nóng. Tính khối lượng chất rắn thu được sau
phản ứng
a)
Có \(\left\{{}\begin{matrix}\dfrac{m_{Mg}}{m_{Fe}}=\dfrac{2}{3}\\m_{Mg}+m_{Fe}=8,4\end{matrix}\right.=>\left\{{}\begin{matrix}m_{Mg}=3,36\left(g\right)\\m_{Fe}=5,04\left(g\right)\end{matrix}\right.\)
b)
\(\left\{{}\begin{matrix}n_{Mg}=\dfrac{3,36}{24}=0,14\left(mol\right)\\n_{Fe}=\dfrac{5,04}{56}=0,09\left(mol\right)\end{matrix}\right.\)
PTHH: Mg + 2HCl --> MgCl2 + H2
_____0,14-------------------->0,14
Fe + 2HCl --> FeCl2 + H2
0,09-------------------->0,09
=> nH2 = 0,23(mol)
=> VH2 = 0,23.22,4 = 5,152(l)
c)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ \(\dfrac{0,2}{1}< \dfrac{0,23}{1}\) => CuO hết, H2 dư
PTHH: CuO + H2 --to--> Cu + H2O
_______0,2-------------->0,2
=> mCu = 0,2.64 = 12,8 (g)
Đúng 1
Bình luận (1)