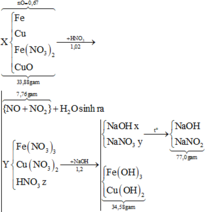
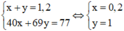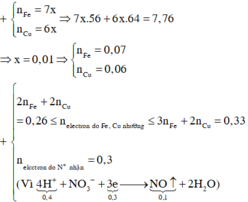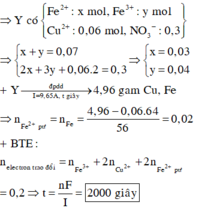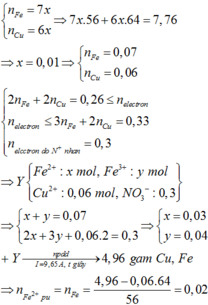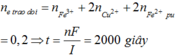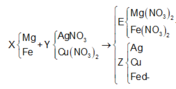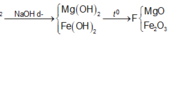Cho 7,76 gam hỗn hợp X gồm Fe và Cu n F e : n C u = 7 : 6 tác dụng với dung dịch chứa 0,4 mol HNO3, thu được dung dịch Y và khí NO (sản phẩm khử duy nhất của N+5). Tiến hành điện phân dung dịch Y với điện cực trơ, cường độ dòng điện không đổi I = 9,65A trong thời gian t giây, thấy khối lượng catot tăng 4,96 gam (kim loại sinh ra bám hết vào catot). Giá trị của t là
A. 2602
B. 2337
C. 2400
D. 2000