Cho 15,62 gam P2O5 vào 400 ml dung dịch NaOH nồng độ aM thu được dung dịch có tổng khối lượng các chất tan bằng 24,2 gam. Giá trị của a
A. 0,2
B. 0,5
C. 0,3
D. 0,4
Cho 15,62 gam P 2 O 5 vào 400 ml dung dịch NaOH nồng độ aM, thu được dung dịch có tổng khối lượng các chất tan bằng 24,2 gam. Giá trị của a là
A. 0,35.
B. 0,2.
C. 0,25.
D. 0,3
Cho 15,62 gam P2O5 vào 400 ml dung dịch NaOH nồng độ a M thu được dung dịch có tổng khối lượng các chất tan bằng 24,2 gam. Giá trị của a là:
A. 0,2
B. 0,3
C. 0,4
D. 0,5
Đáp án B
Hướng dẫn giải:
P2O5+ 3H2O → 2 H3PO4
0,11 0,22mol
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
Nếu chất tan trong dung dịch chỉ chứa các muối thì:
Theo các PT ta có: nH2O= nNaOH= 0,4a (mol)
Áp dụng định luật bảo toàn khối lượng ta có:
mNaOH + mH3PO4= mmuối + mH2O →0,4a. 40 + 0,22.98= 24,2 + 0,4a.18 → a= 0,3 M
Cho 15,62 gam P2O5 vào 400 ml dung dịch NaOH aM (hai chất đều phản ứng hết) thu được dung dịch có tổng khối lượng các chất tan bằng 24,2 gam. Giá trị của a là:
A. 0,2
B. 0,3
C. 0,4
D. 0,5
Đáp án B
P2O5+ 3H2O→ 2 H3PO4
→ nH3PO4= 2. nP2O5= 2.15,62/142= 0,22 mol
H3PO4+ NaOH → NaH2PO4+ H2O
H3PO4+ 2NaOH → Na2HP O4+ 2H2O
H3PO4+ 3NaOH → Na3PO4+ 3H2O
Theo các phương trình trên ta có: nH2O =nNaOH= 0,4a mol
Theo ĐLBT khối lượng:
mH3PO4+ mNaOH=mmuối+ mH2O
→ 0,22.98+ 0,4a.40=24,2+ 18.0,4a →a= 0,3 mol
Câu 8: Cho 99,4 gam P2O5 vào 500 gam nước (dư), thu được dung dịch A.
a. Tính khối lượng chất tan, khối lượng nước trong dung dịch A.
b. Tính nồng độ phần trăm dung dịch A.
c. Tính nồng độ mol/l của dung dịch A. Biết thể tích dung dịch A là 500 ml.
giúp vs ae
\(n_{P_2O_5}=\dfrac{99,4}{142}=0,7\left(mol\right)\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
0,7 2,1 1,4
a, \(m_{H_3PO_4}=1,4.98=137,2\left(g\right)\)
\(m_{ddH_3PO_4}=99,4+500=599,4\left(g\right)\)
Kl nước trong dd A :
\(m_{H_2O}=599,4-137,2=462,2\left(g\right)\)
\(b,C\%_{H_3PO_4}=\dfrac{137,2}{599,4}.100\%\approx22,89\%\)
\(c,C_M=\dfrac{n}{V}=\dfrac{1,4}{0,5}=2,8M\)
Hòa tan 12,6 gam hỗn hợp hai kim loại M (hóa trị II) và M’ (hóa trị III) bằng axit HCl dư, thu được dung dịch A và khí B. Đốt cháy hoàn toàn ½ lượng khí B trên thu được 2,79 gam H2O.
a) Cô cạn dung dịch A thu được m gam hỗn hợp muối khan. Tính giá trị m.
b) Cho lượng khí B còn lại phản ứng hoàn toàn với khí Cl2 vừa đủ (t0C) rồi cho sản phẩm thu được hấp thụ vào 0,2 lít dung dịch NaOH 16% (d = 1,20g/ml). Tính nồng độ % các chất trong dung dịch thu được.
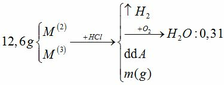
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
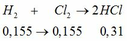
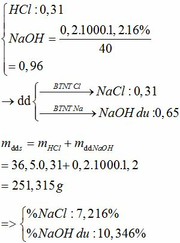
a: hòa tan hoàn toàn 0,3 mol NaOH vào nước thu được 0,5 lít dung dịch NaOH. tính nồng độ mol của dung dịch?
b: hòa tan hoàn tàn 24 gam NaOH vào nước thu được 400ml dung dịch NaOH. tính nồng độ mol của dung dịch?
\(a,C_{M\left(NaOH\right)}=\dfrac{0,3}{0,5}=0,6M\\ b,n_{NaOH}=\dfrac{24}{40}=0,6\left(mol\right)\\ C_{M\left(NaOH\right)}=\dfrac{0,6}{0,4}=1,5M\)
Một hỗn hợp X gồm 0,2 mol Cu và 0,1 mol Fe3O4. Cho X vào 400 ml dung dịch H2SO4 1M. Sau khi phản ứng kết thúc thu được dung dịch A và còn lại x gam chất rắn B không tan. Cho dung dịch A tác dụng với dung dịch NaOH dư rồi đun nóng trong không khí cho các phản ứng xảy ra hoàn toàn. Lọc lấy kết tủa, nung đến khối lượng không đổi thu được y gam chất rắn C. Xác định giá trị của x và y.
Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
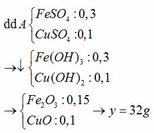
Trộn 1 dung dịch có hòa tan 0,2 mol CuCl2 với dung dịch có hòa tan 20g NaOH, lọc tách được kết tủa và dung dịch trước nước lọc. Nung kết tủa đến khối lượng không đổi thu được a gam chất rắn a) Tính giá trị bằng số của a b) Tính khối lượng các chất có trong dung dịch nước lọc
a) \(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right)\)
\(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\)
Lập tỉ lệ : \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)=> Sau phản ứng NaOH dư
\(n_{Cu\left(OH\right)_2}=n_{CuCl_2}=0,2\left(mol\right)\)
Dung dịch nước lọc gồm NaCl (0,4_mol); NaOH dư ( 0,1 mol)
\(Cu\left(OH\right)_2-^{t^o}\rightarrow CuO+H_2O\)
\(n_{CuO}=n_{Cu\left(OH\right)_2}=0,2\left(mol\right)\)
\(a=m_{CuO}=0,2.80=16\left(g\right)\)
b) \(m_{NaCl}=0,4.58,5=23,4\left(g\right);m_{NaOH}=0,1.40=4\left(g\right)\)