Nguyên tử khối trung bình của K là 39,136. Biết K có ba đồng vị trong đó đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% số nguyên tử.
Nguyên tử khối của đồng vị còn lại là
A. 41.
B. 37.
C. 38.
D. 42.
Trong tự nhiên kali gồm 3 đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của 39K trong KBr là
A. 30,56%.
B. 29,92%.
C. 31,03%.
D. 30,55%.
Đáp án D
%41K = 100 - 93,26 - 0,012 = 6,728%.
Khối lượng nguyên tử trung bình của K là:
MK = 39 x 0,9326 + 40 x 0,00012 + 41 x 0,06728 = 39,13468.
Khối lượng nguyên tử trung bình của Br là:
MBr = 79,92.
Thành phần phần trăm của 39K trong KBr là
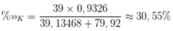
Nguyên tử khối trung bình của K là 39,136. Biết K có bà đồng vị trong đó có 2 đồng vị là ³⁹K (93,26%), ⁴⁰K (0,01%). Tìm số khối đồng vị còn lại của K.
% số nguyên tử của đồng vị còn lại là 100% - 93,26% - 0,01% = 6,73%
Gọi số khố của đồng vị còn lại là A
Ta có :
$39,136 = 39.93,26\% + 40.0,01\% + A.6,73\%$
$\Rightarrow A = 41$
Nguyên tử khối trung bình của Brom là 79.91. Brom có 2 đồng vị, trong đó đồng vị ⁷⁹Br chiếm 54.5% số nguyên tử.
a) Tính nguyên tử khối của đồng vị còn lại
b) Tính % khối lượng của đồng vị ⁷⁹Br có trong phân tử HBrO4
hóa học 10 tính nguyên tử khối của đồng vị còn lại nếu biết nguyên tử khối trung bình của nguyên tố X là 79,91. biết X có hai đồng vị trong đó đồng vị 79X chiếm 54,5% số nguyên tử
Đặt x nguyên tử khối của đồng vị còn lại
Ta có : \(\overline{M}=\dfrac{54,5.79+\left(100-54,5\right).x}{100}=79,91\)
\(\rightarrow x=81\)
Vậy nguyên tử khối của đồng vị còn lại : \(^{81}X\)
Trong tự nhiên kali có 3 đồng vị 39K (93,26%), 41K (x1%), 40K (x2%), nguyên tử khối trung bình của kali là 39,1347. Giá trị x1 và x2 lần lượt là
A. 6,73% và 0,01%.
B. 3,67% và 3,07%.
C. 3,76% và2,98%.
D. 2,89% và 3,85%.
Nguyên tố Liti (Z= 3) có 2 đồng vị, trong đó đồng vị 6Li chiếm 7,5%. Viết kí hiệu nguyên tử đồng vị còn lại, biết nguyên tử khối trung bình của Li là 6,925.
Nguyên tử khối trung bình của Ag là 107 , 87 . Bạc có hai đồng vị , trong đó đồng vị 109Ag chiếm tỉ lệ 44 % . Xác định nguyên tử khối của đồng vị còn lại ?
gọi nguyên tử khối của đồng vị thứ 2 là X
A¯Ag=109.44+x.(109−44)\100
107,87=109.44+56x
⇒5991=56x⇒x≃107
Vậy nguyên tử khối của đồng vị còn lại là x≃107
Nguyên tố X có ba đồng vị X1 chiếm 92,3%, X2 chiếm 4,7% và X3 chiếm 3%. Tổng số khối của ba đồng vị là 87. Số nơtron trong nguyên tử X2 nhiều hơn trong nguyên tử X1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Số khối của ba đồng vị X1, X2, X3 lần lượt là:
A. 27, 28, 32.
B. 26, 27, 34.
C. 28, 29, 30.
D. 29, 30, 28.
Đáp án C
Gọi số khối của ba đồng vị tương ứng x1, x2, x3
Ta có x2= x1 +1
Theo đề ra ta có hệ phương trình
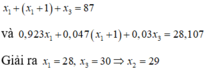
Nguyên tố Cu có hai đồng vị, có nguyên tử khối trung bình là 63,546. Trong đó đồng vị63Cu chiếm 72,7%. Tìm số khối của đồng vị còn lại.
Ta có: \(\overline{M}=\dfrac{72,7.63+29,3.x}{100}\Leftrightarrow x=\dfrac{100.63,546-72,7.63}{29,3}=65\)