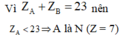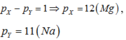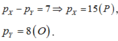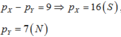A, B ở hai phân nhóm chính liên tiếp trong bảng. B thuộc nhóm 5. Ở trạng thái đơn chất chúng không phản ứng với nhau.Tổng số p trong 2 hạt nhân nguyên tử bằng 23. Vị trí của A trong bảng tuần hoàn là
A. Chu kì 3, nhóm VIA
B. Chu kì 3, nhóm IVA
C. Chu kì 2, nhóm IVA
D. Chu kì 2, nhóm VIA