Hòa tan 23,2 gam hỗn hợp X gồm Fe 3 O 4 và CuO có cùng khối lượng vào dung dịch HNO 3 vừa đủ chứa 0,77 mol HNO 3 thu được bằng dung dịch Y và khí Z gồm NO và NO 2 . Khối lượng mol trung bình của Z bằng
A. 42.
B. 38.
C. 40,667.
D. 35,333
Hòa tan 23,2 gam hỗn hợp X gồm F e 3 O 4 và CuO có cùng khối lượng vào dung dịch H N O 3 vừa đủ chứa 0,77 mol H N O 3 thu được bằng dung dịch Y và khí Z gồm NO và N O 2 . Khối lượng mol trung bình của Z bằng
A. 42.
B. 38.
C. 40,667.
D. 35,333.
Nung 8,8 gam hỗn hợp X gồm Fe và Cu trong khí O2 thu được hỗn hợp chất rắn Y gồm Fe, FeO, Fe2O3, Fe3O4,
CuO và Cu. Để hòa tan hết hỗn hợp Y cần dùng dung dịch H2SO4 đặc, nóng. Sau phản ứng thu được dung dịch Z chứa
23,2 gam muối tan gồm Fe2(SO4)3 và CuSO4. Tính phần trăm về khối lượng của Fe trong hỗn hợp X.
Hỗn hợp X chứa x mol Fe và y mol Cu.
\(\Rightarrow56x+64y=8,8\)
Sau cùng muối thu được gồm Fe2(SO4)3 và CuSO4
Bảo toàn các nguyên tố kim loại:
\(n_{Fe2\left(SO4\right)3}=\frac{1}{2}n_{Fe}=0,5x\)
\(n_{CuSO4}=n_{Cu}=y\)
\(\Rightarrow400.0,5x+160y=23,2\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,02\\y=0,12\end{matrix}\right.\)
\(m_{Fe}=0,02.56=1,12\left(g\right)\)
\(\Rightarrow\%m_{Fe}=\frac{1,12}{8,8}.100\%=12,73\%\)
Hòa tan hoàn toàn 33,88 gam hỗn hợp X gồm Fe, Cu, Fe(NO3)2 và CuO (chứa 31,641% là khối lượng của oxi) vào dung dịch chứa 1,02 mol HNO3 (dùng dư), thu được dung dịch Y (không có muối amoni) và 7,76 gam hỗn hợp khí Z gồm NO và NO2. Cho 48 gam NaOH vào Y, thu được 34,58 gam kết tủa và dung dịch T. Cô cạn T và nung chất rắn khan đến khối lượng không đổi, thu được 77,0 gam rắn. Phần trăm số mol của kim loại Fe trong X gần nhất với
A. 8%
B. 15%
C. 22%
D. 31%
Chọn đáp án B
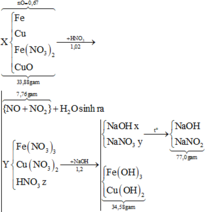
Ta có: 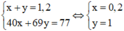
đặt z là nHNO3 dư, BTNT.H Þ nH2O sinh ra = 0,51 – 0,5z
BTNT.N Þ n N O 3 - trong muối của Y là 1 – z = nOH trong kết tủa
Þm Kim loại = 34,58 – 17x(1-z) gam
BTKL Þ 33,88 + 1,02x63 = 34,58 - 17x(l - z) + z + 62 + 7,76 + (0,51 - 0,5z)xl8 Þ z = 0,18

BTNT.N Þ nFe(NO3)2 = (0,09 + 0,11 + 1 -1,02)/2 = 0,09 Þ nFe = 0,14 - 0,09 = 0,05
Vậy %m Fe trong X ![]()
Hòa tan hoàn toàn m (gam) hỗn hợp E gồm: CuO, Al(OH)3, Na2CO3, MgCO3, Mg, Al và Fe ( trong E thì CuO chiếm 27,1% về khối lượng) cần dùng dung dịch chứa 0,3262 mol HCl, sau phản ứng thu được dung dịch X có chứa \(\dfrac{6689m}{3200}\)6689m/3200(gam) muối và 0,1 mol hỗn hợp khí T có tỉ khối so với H2 là 5,2. Phần trăm khối lượng của Al(OH)3 trong E là?
Hòa tan 20,0 gam hỗn hợp gồm CuO và BaO vào nước dư được 250 ml dung dịch X có nồng độ 0,4M.
Viết phương trình phản ứng và tính % khối lượng CuO trong hỗn hợp đầu?
\(BaO+H_2O\rightarrow Ba\left(OH\right)_2\\Tacó:n_{BaO} =n_{Ba\left(OH\right)_2}=0,25.0,4=0,1\left(mol\right)\\ \Rightarrow m_{BaO}=0,1.153=15,3\left(g\right)\\ \Rightarrow\%m_{CuO}=\dfrac{20-15,3}{20}.100=30,72\%\)
Hòa tan hết 0,6 mol hỗn hợp X gồm Mg, Fe(NO3)3 và Fe(NO3)2 trong dung dịch chứa 1,08 mol HNO3, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối có khối lượng là 103,3 gam và 0,1 mol hỗn hợp khí Z gồm NO và N2O. Cô cạn dug dịch Y, lấy muối đem nung đến khối lượng không đổi, thu được 31,6 gam rắn khan. Nếu cho dung dịch NaOH dư vào Y (không có mặt oxi), thu được 42,75 gam hỗn hợp các hiđroxit. Phần trăm khối lượng của Fe(NO3)3 trong hỗn hợp X là:
A. 30,01%
B. 35,01%
C. 43,9%
D. 40,02%
Hòa tan hết 0,6 mol hỗn hợp X gồm Mg, Fe(NO3)2 trong dung dịch chứa 1,08 mol HNO3, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối có khối lượng là 103,3 gam và 0,1 mol hỗn hợp khí Z gồm NO và N2O. Cô cạn dung dịch Y, lấy muối đem nung đến khối lượng không đổi, thu được 31,6 gam rắn khan. Nếu cho dung dịch NaOH dư vào Y (không có mặt oxi), thu được 42,75 gam hỗn hợp các hidroxit. Phần trăm khối lượng của Fe(NO3)3 trong hỗn hợp X là:
A. 30,01%.
B. 35,01%.
C. 43,9%.
D. 40,02%.
Hòa tan hết 0,6 mol hỗn hợp X gồm Mg, Fe(NO3)3 và Fe(NO3)2 trong dung dịch chứa 1,08 mol HNO3, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối có khối lượng là 103,3 gam và 0,1 mol hỗn hợp khí Z gồm NO và N2O. Cô cạn dung dịch Y, lấy muối đem nung đến khối lượng không đổi, thu được 31,6 gam rắn khan. Nếu cho dung dịch NaOH dư vào Y (không có mặt oxi), thu được 42,75 gam hỗn hợp các hiđroxit. Phần trăm khối lượng của Fe(NO3)3 trong X là:
A. 30,01%
B. 43,90%
C. 40,02%
D. 35,01%
Đáp án D
Quy đổi hỗn hợp X về Mg a mol, Fe b mol và NO3 c mol
Hòa tan hết 0,6 mol hỗn hợp X gồm Mg, Fe(NO3)3 và Fe(NO3)2 trong dung dịch chứa 1,08 mol HNO3, kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối có khối lượng là 103,3 gam và 0,1 mol hỗn hợp khí Z gồm NO và N2O. Cô cạn dung dịch Y, lấy muối đem nung đến khối lượng không đổi, thu được 31,6 gam rắn khan. Nếu cho dung dịch NaOH dư vào Y (không có mặt oxi), thu được 42,75 gam hỗn hợp các hiđroxit. Phần trăm khối lượng của Fe(NO3)3 trong X là
A. 30,01%.
B. 35,01%.
C. 43,90%.
D. 40,02%.