Oxi hoá 4,6g etanol bằng CuO, t0 được 6,6g hỗn hợp X gồm Anđêhit ; Axit ; H2O và Ancol dư. Cho toàn bộ X phản ứng với Na dư được 1,68lít H2 đktc . Tính % khối lượng Ancol đã chuyển hoá thành Axit và Anđêhit:
A. 75%
B. 80%
C. 70%
D. 50%
Oxi hóa 4 gam Ancol metylic bằng CuO, t0 thu được 5,6 gam hỗn hợp Anđêhit, nước và Ancol dư. Hiệu suất của phản ứng là :
A. 40%
B. 60%
C. 75%
D. 80%
Lời giải:
nCH3OH = 0,125
CH3OH + O → HCHO + H2O
⇒ mO = 5,6 – 4 = 1,6g ⇒ nO = 0,1
⇒ H =( 0,1 : 0,125).100% = 80%
Đáp án D.
Ancol nào bị oxi hoá tạo ra Anđêhit khi phản ứng với CuO, t0 :
A. tert – butylic
B. iso butylic
C. iso propylic
D. 2 – metyl – butAn – 2 – ol
Lời giải:
Ancol bị oxi hoá tạo ra Anđêhit khi phản ứng với CuO, t0
⇒ Ancol bậc 1 ⇒ Chỉ đáp án B thỏa mãn
Đáp án B.
Cho 2,24 lít propen hợp nước sau đó lấy toàn bộ lượng ancol thu được đem oxi hoá bằng CuO. Lấy hỗn hợp sản phẩm sau phản ứng (hỗn hợp X) với CuO cho tác dụng với Ag2O/dung dịch NH3, t0 thì thu được 4,32 gam Ag. Hãy xác định % khối lượng của anđehit trong hỗn hợp X:
A. 20% B. 40% C. 60% D. 50%
nC3H6 = 2.24/22.4 = 0.1 (mol)
nAg = 4.32/108 = 0.04 (mol)
=> nCH3CH2CHO = 0.04/2 = 0.02 (mol)
BT Cacbon :
3nC3H6 = 3nCH3CH2CHO + 3nCH3COCH3
=> nCH3COCH3 = 0.1 - 0.02 = 0.08 (mol)
\(\%m_{CH_3CH_2CHO}=\dfrac{0.02\cdot58}{0.02\cdot58+0.08\cdot58}\cdot100\%=20\%\)
C2H5CHO + 2AgNO3 + 3NH3 + H2O $\to$ C2H5COONH4 + 2Ag + 2NH4NO3
n Ag = 4,32/108 = 0,04(mol)
=> n C2H5CHO = 1/2 n Ag = 0,02 mol
n C3H6 = 2,24/22,4 = 0,1(mol)
Bảo toàn nguyên tố với C :
n C3H7OH(trong X) = 0,1 - 0,02 = 0,08(mol)
Vậy :
%m C2H5CHO = 0,02.58/(0,02.58 + 0,08.60) .100% =19,46%
Oxi hoá 2,3 gam ancol etylic bằng CuO đun nóng, thu được 3,3 gam hỗn hợp X gồm anđehit, axit, ancol dư và nước. Hỗn hợp này tác dụng hết với Na sinh ra 0,84 lít H 2 (đktc). Hiệu suất phản ứng oxi hoá ancol là :
A. 25%
B. 50%
C. 75%
D. 90%
Đáp án C
● Cách 1: Tính toán theo phương trình phản ứng
Khối lượng hỗn hợp X tăng lên so với khối lượng ancol ban đầu là do lượng O trong CuO phản ứng đã chuyển vào H 2 O và CH 3 COOH .
Theo giả thiết, suy ra :
n H 2 = 0 , 0375 n CuO phản ứng = n O phản ứng
= (3,3 - 2,3):16 = 0,0625
Gọi số mol của ancol tham gia phản ứng là x, y và số mol ancol dư là z.
Phương trình phản ứng :
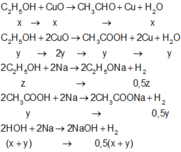
⇒ n C 2 H 5 OH bđ = x + y + z = 0 , 05 n H 2 = 0 , 5 y + 0 , 5 z + 0 , 5 x + 0 , 5 y = 0 , 0375 n CuO pư = x + 2 y = 0 , 0625 ⇒ x = 0 , 0125 ; y = 0 , 025 ; z = 0 , 0125 H = 0 , 05 - 0 , 0125 0 , 05 = 75 %
● Cách 2: Sử dụng phương pháp bảo toàn nguyên tố
Sơ đồ phản ứng :
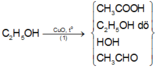
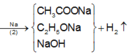
Bản chất phản ứng (1) là C 2 H 5 OH bị oxi hóa bởi CuO, khối lượng hỗn hợp sau phản ứng tăng lên là do O trong CuO chuyển vào H 2 O và CH 3 COOH . Ở phản ứng (2), CH 3 COOH , C 2 H 5 OH dư, HOH có nguyên tử H linh động trong nhóm –OH nên tham gia phản ứng thế Na giải phóng H 2 , CH 3 CHO không tham gia phản ứng này.
Sử dụng bảo toàn nguyên tố O trong phản ứng oxi hóa ancol và bảo toàn nguyên tố H của nhóm –OH trong phản ứng của X với Na, ta có :
n HOH = n CH 3 COOH = n O pư = 0 , 0625 n HOH + n CH 3 COOH + n C 2 H 5 OH dư = 2 n H 2 = 0 , 075 ⇒ n C 2 H 5 OH dư = 0 , 0125 H = 0 , 05 - 0 , 0125 0 , 05 = 75 %
Cho 12,20 gam hỗn hợp X gồm etanol và propan-1-ol tác dụng với Na (dư) thu được 2,80 lit khí đktc. Cho hỗn hợp X qua ống đựng CuO, đun nóng. Viết các phương trình hoá học của phản ứng xảy ra.
Phương trình phản ứng:
CH3-CH2OH + CuO 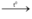 CH3-CHO + Cu + H2O
CH3-CHO + Cu + H2O
CH3-CH2-CH2OH + CuO  CH3-CH2-CHO + Cu + H2O
CH3-CH2-CHO + Cu + H2O
Oxi hoá 9,2 gam ancol etylic bằng CuO đun nóng thu được 13,2 gam hỗn hợp gồm anđehit, axit, ancol dư và nước. Hỗn hợp này tác dụng với Na sinh ra 3,36 lít H2 (ở đktc). Phần trăm ancol bị oxi hoá là:
A. 25%.
B. 50%.
C. 75%.
D. 90%.
Đáp án C
Hướng dẫn
Theo giả thiết ta có :
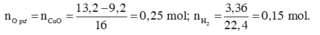
Phương trình phản ứng :

Theo các phương trình phản ứng và giả thiết ta có :
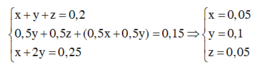
Theo các phương trình phản ứng và giả thiết ta có :
Vậy phần trăm khối lượng ancol bị oxi hóa là :
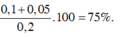
Cho 11g hỗn hợp A gồm metanol và etanol tác dụng với Na. Sau phản ứng thu được 3,36l khí H2 ở dktc. Õi hoá toàn bộ hỗn hợp A trên bằng CuO rồi cho sản phẩm vào AgNO3/NH3 dư được m g kết tủa. Tìm m
CH3OH + Na==>CH3ONa+ 1/2H2
C2H5OH + Na==> C2H5ONa+1/2H2
Gọi mol CH3Oh , C2H5OH lần lượt là a,b
tacó 1/2a+1/2b=0.15(mol)và 32a+46b=11
==>a=0.2(mol)và b=0.1(mol)
==>molCH3OH=0.2(mol),molC2H5OH=0,1(mol)
CH3OH + CuO==>HCHO +Cu+H20
C2H5OH + CuO==> Ch3CHO +Cu +H2O
molHCHO=molCH3OH=0.2(mol)
mol CH3CHO=0.1(mol)=molC2H5OH
có kết tủa là Ag
HCHO + 4AgNO3/Nh3==>HCOONh4 + 4Ag +7Nh3+2H2O
CH3CHO+2AgNo3/Nh3==>CH3COONH4 +2Ag +3Nh3+H20
tổng mol Ag=4molHCHO+2molCH3CHO=1(mol)
mAg=108(g)=m kết tủa![]()
Oxi hoá 1,2 gam CH3OH bằng CuO nung nóng, sau một thời gian thu được hỗn hợp X (gồm HCHO, H2O và CH3OH dư). Cho toàn bộ X tác dụng với lượng dư Ag2O (hoặc AgNO3) trong dung dịch NH3, được 12,96 gam Ag. Hiệu suất của phản ứng oxi hoá CH3OH là
A. 70,4%.
B. 76,6%.
C. 65,5%.
D. 80,0%.
Oxi hoá 1,2 gam CH3OH bằng CuO nung nóng, sau một thời gian thu được hỗn hợp sản phẩm X (gồm HCHO, H2O, CH3OH dư). Cho toàn bộ X tác dụng với lượng dư Ag2O (hoặc AgNO3) trong dung dịch NH3, được 12,96 gam Ag. Hiệu suất của phản ứng oxi hoá CH3OH là
A. 76,6%.
B. 80,0%.
C. 65,5%.
D. 70,4%.