Biết 5 gam hỗn hợp hai muối là CaCO 3 và CaSO 4 tác dụng vừa đủ với 200 ml dung dịch HCl, sinh ra được 448 ml khí (đktc). Tính nồng độ mol của dung dịch HCl đã dùng.

Những câu hỏi liên quan
Biết 5 gam hỗn hợp hai muối là CaCO 3 và CaSO 4 tác dụng vừa đủ với 200 ml dung dịch HCl, sinh ra được 448 ml khí (đktc). Tính thành phần phần trăm theo khối lượng của mỗi muối trong hỗn hợp ban đầu.
Thành phần của hỗn hợp muối :
Theo phương trình hoá học, số mol CaCO 3 có trong hỗn hợp là
n CaCO 3 = n CO 2 = 0,02 mol
Khối lượng CaCO 3 có trong hỗn hợp là :
m CaCO 3 = 0,02 x 100 = 2 gam
Thành phần các chất trong hỗn hợp :
% m CaCO 3 = 2x100%/5 = 40%
% m CaSO 4 = 100% - 40% = 60%
Đúng 0
Bình luận (0)
Câu 2:Có một hỗn hợp m gam gồm kim loại Al và Fe, hai dd NaOH và HCl chưa rõ nồng độ biết rằng: - 100ml dd HCl tác dụng vừa đủ với 3,71 gam Na2CO3 và 20 gam dd NaOH thu được 5,85g muối khan. - Cho m gam hỗn hợp Al, Fe tác dụng vừa đủ với 66,67 g dd NaOH hoặc 700ml dd HCl. a. Tính CM dd HCl và nồng độ % dd NaOH. b. Tính khối lượng mỗi kim loại trong hỗn hợp.
A là hỗn hợp 2 kim loại kiềm X và Y thuộc 2 chu kì kế tiếp. Nếu cho A tác dụng vừa đủ với dung dịch HCl thì thu được a gam 2 muối, còn nếu cho A tác dụng vừa đủ với dung dịch
H
2
S
O
4
thì thu được 1,2271a gam hai muối. X và Y là A. Li và Na B. Na và K C. K và Rb D. Rb và Cs
Đọc tiếp
A là hỗn hợp 2 kim loại kiềm X và Y thuộc 2 chu kì kế tiếp. Nếu cho A tác dụng vừa đủ với dung dịch HCl thì thu được a gam 2 muối, còn nếu cho A tác dụng vừa đủ với dung dịch H 2 S O 4 thì thu được 1,2271a gam hai muối. X và Y là
A. Li và Na
B. Na và K
C. K và Rb
D. Rb và Cs
A là hỗn hợp 2 kim loại kiềm X và Y thuộc 2 chu kì kế tiếp. Nếu cho A tác dụng vừa đủ với dung dịch HCl thì thu được a gam 2 muối, còn nếu cho A tác dụng vừa đủ với dung dịch
H
2
S
O
4
thì thu được 1,1807a gam hai muối. X và Y là A. Li và Na B. Na và K C. K và Rb D. Rb và Cs
Đọc tiếp
A là hỗn hợp 2 kim loại kiềm X và Y thuộc 2 chu kì kế tiếp. Nếu cho A tác dụng vừa đủ với dung dịch HCl thì thu được a gam 2 muối, còn nếu cho A tác dụng vừa đủ với dung dịch H 2 S O 4 thì thu được 1,1807a gam hai muối. X và Y là
A. Li và Na
B. Na và K
C. K và Rb
D. Rb và Cs
Cho 5g hỗn hợp muối CaCO3 và CaSO4 tác dụng vừa đủ với 200ml dung dịch HCl sinh ra 448ml khí( đktc)
a. tính nồng độ mol của dung dịch HCl đem dùng
b. Tính thành phần phần trăm theo khối lượng của mỗi muối trong hỗn hợp
CaCO3 + 2HCl -> CaCl2 + CO2 + H2O
nCO2=0,02(mol)
Theo PTHH ta có:
nHCl=2nCO2=0,04(mol)
nCaCO3=nCO2=0,02(mol)
CM dd HCl=\(\dfrac{0,04}{0,2}=0,2M\)
mCaCO3=100.0,02=2(g)
%mCaCO3=\(\dfrac{2}{5}.100\%=40\%\)
%mCaSO4=100-40=60%
Đúng 0
Bình luận (0)
Biết 5 gam hỗn hợp 2 muối là Na 2 CO 3 và NaCl tác dụng vừa đủ với 20 ml dung dịch HCl, thu được 448 ml khí (đktc). Tính thành phần phần trăm theo khối lượng của mỗi muối trong hỗn hợp ban đầu.
Na 2 CO 3 + 2HCl → 2NaCl + H 2 O + CO 2
n khi = n CO 2 = 0,448/22,4 = 0,02 mol; n HCl = 0,02.2/1 = 0,04 mol
n Na 2 CO 3 = 0,02.1/1 = 0,02 (mol) → m Na 2 CO 3 = 0,02 x 106 = 2,12g
% m Na 2 CO 3 = 2,12/5 . 100% = 42,4%
% m NaCl = 100% - 42,4% = 57,6%
Đúng 0
Bình luận (0)
Chia 64,42 gam hỗn hợp gồm FeO, Fe 3 O 4 , CuO, ZnO, Fe 2 O 3 thành hai phần bằng nhau.
Phần 1 tác dụng hết với axit HCl thu được 59,16 gam muối khan.
Phần 2 tác dụng vừa đủ với 1 lít dung dịch A chứa hỗn hợp HCl và H 2 SO 4 loãng thu được
65,41 gam muối khan.
Tính nồng độ mỗi axit trong dung dịch A.
Giả sử trong mỗi phần có: \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\\n_{Zn}=c\left(mol\right)\\n_O=d\left(mol\right)\end{matrix}\right.\)
=> 56a + 64b + 65c + 16d = 32,21
P1:
nO = nH2O = d (mol)
=> nHCl = 2d (mol)
Theo ĐLBTKL: mrắn bđ + mHCl = mmuối + mH2O
=> 32,21 + 73d = 59,16 + 18d
=> d = 0,49 (mol)
P2:
Gọi số mol HCl, H2SO4 là a, b (mol)
nH2O = nO = 0,49 (mol)
Bảo toàn H: a + 2b = 0,98 (1)
Theo ĐLBTKL: mrắn bđ + mHCl + mH2SO4 = mmuối + mH2O
=> 32,21 + 36,5a + 98b = 65,41 + 0,49.18
=> 36,5a + 98b = 42,02 (2)
(1)(2) => a = 0,48 (mol); b = 0,25 (mol)
=> \(\left\{{}\begin{matrix}C_{M\left(HCl\right)}=\dfrac{0,48}{1}=0,48M\\C_{M\left(H_2SO_4\right)}=\dfrac{0,25}{1}=0,25M\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Hỗn hợp E gồm chất X (CxHyO4N ) và Y (CxNtO5N2 ), trong đó X không chứa chức este, Y là muối củaα - amino axit no vớ axit nitric. Cho m gam E tác dụng vừa dủ với 100ml dung dịch NaOH 1,2M. Đun nóng nhẹ thấy thoát ra 0,672 lít (đktc) một amin bậc 3 thể khí điều kiện thường. Mặt khác m gam E tác dụng vừa đủ với a mol HCl trong dung dịch thu được hỗn hợp sản phẩm trong đó có 2,7 gam một axit cacboxylic. Giá trị m và a lần lượt là A. 9,87 và 0,03 B. 9,84 và 0,03 C. 9,84 và 0,06 D. 9,87 và 0,06
Đọc tiếp
Hỗn hợp E gồm chất X (CxHyO4N ) và Y (CxNtO5N2 ), trong đó X không chứa chức este, Y là muối củaα - amino axit no vớ axit nitric. Cho m gam E tác dụng vừa dủ với 100ml dung dịch NaOH 1,2M. Đun nóng nhẹ thấy thoát ra 0,672 lít (đktc) một amin bậc 3 thể khí điều kiện thường. Mặt khác m gam E tác dụng vừa đủ với a mol HCl trong dung dịch thu được hỗn hợp sản phẩm trong đó có 2,7 gam một axit cacboxylic. Giá trị m và a lần lượt là
A. 9,87 và 0,03
B. 9,84 và 0,03
C. 9,84 và 0,06
D. 9,87 và 0,06
Đáp án A
Amin bậc 3 thể khí ở điều kiện thường chỉ có thể là trimetyl amin (CH3)3N : 0,03 mol
X (CxHyO4N) không chứa chức este, chỉ có 1 nguyên tử N nên là muối amoni của axit 2 chức.
Y là muối của α− amino axit no với axit nitric nên phản ứng với NaOH không sinh khí.
TN1:
![]()
TN2:
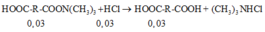
→ M a x i t c a c b o n x y l i c = 90 ⇒ R = O ( C O O H ) 2
→ X là: C5H11O4N → Y là C5H11O5N2
Mặt khác Y là muối của α− amino axit no với HNO3
→ α−aminoaxit là C5H11O2N
→ Y là C5H12O5N2(HOOC−C4H8−NH3NO3)
→ m = 9 , 87 g
→ a = nHCl = 0,03 mol
Đúng 0
Bình luận (0)
Hỗn hợp E gồm chất X (CxHyO4N ) và Y (CxNtO5N2 ), trong đó X không chứa chức este, Y là muối củaα - amino axit no vớ axit nitric. Cho m gam E tác dụng vừa dủ với 100ml dung dịch NaOH 1,2M. Đun nóng nhẹ thấy thoát ra 0,672 lít (đktc) một amin bậc 3 thể khí điều kiện thường. Mặt khác m gam E tác dụng vừa đủ với a mol HCl trong dung dịch thu được hỗn hợp sản phẩm trong đó có 2,7 gam một axit cacboxylic. Giá trị m và a lần lượt là A. 9,87 và 0,03 B. 9,84 và 0,03 C. 9,84 và 0,06 D. 9,87 và 0,06
Đọc tiếp
Hỗn hợp E gồm chất X (CxHyO4N ) và Y (CxNtO5N2 ), trong đó X không chứa chức este, Y là muối củaα - amino axit no vớ axit nitric. Cho m gam E tác dụng vừa dủ với 100ml dung dịch NaOH 1,2M. Đun nóng nhẹ thấy thoát ra 0,672 lít (đktc) một amin bậc 3 thể khí điều kiện thường. Mặt khác m gam E tác dụng vừa đủ với a mol HCl trong dung dịch thu được hỗn hợp sản phẩm trong đó có 2,7 gam một axit cacboxylic. Giá trị m và a lần lượt là
A. 9,87 và 0,03
B. 9,84 và 0,03
C. 9,84 và 0,06
D. 9,87 và 0,06
Đáp án A
Amin bậc 3 thể khí ở điều kiện thường chỉ có thể là trimetyl amin (CH3)3N : 0,03 mol
X (CxHyO4N) không chứa chức este, chỉ có 1 nguyên tử N nên là muối amoni của axit 2 chức.
Y là muối của α− amino axit no với axit nitric nên phản ứng với NaOH không sinh khí.

→ X là: C5H11O4N → Y là C5H11O5N2
Mặt khác Y là muối của α− amino axit no với HNO3 → α−aminoaxit là C5H11O2N
→ Y là C5H12O5N2(HOOC−C4H8−NH3NO3)
→ m=0,03.(149+180)=9,87 gam
→ a = nHCl = 0,03 mol
Đúng 0
Bình luận (0)










