Ion nào có tổng số proton bằng 48 ?
A. NH 4 + B. SO 3 2 -
C. SO 4 2 - D. K +
Ion nào có tổng số proton bằng 48 ?
A. NH4+
B. CO32-
C. SO42-
D. ClO3-
Đáp án C
Số proton của các nguyên tử N( p=7), H ( p=1), C (p = 6), O (p = 8), S (P = 16), Cl (P = 17)
NH4+ số proton = 7 + 1.4 = 11
Tương tự số proton trong CO32- = 30, SO42-= 48, ClO3- = 41.
Tổng số proton trong 2 ion XA32- và XA42- lần lượt là 40 và 48. Xđ các nguyên tố X,A và ct các ion
Vì Tổng số proton trong 2 ion XA32- và XA42- lần lượt là 40 và 48 nên
=> Ta có hệ phương trình
\(\left\{{}\begin{matrix}P_X+3P_A=40\\P_X+4P_A=48\end{matrix}\right.\) ----> \(\left\{{}\begin{matrix}P_X=16\\P_A=8\end{matrix}\right.\) (S và O)
Vì đây là cho proton k phải cho electron nên không phải cộng thêm 2
Mình nghĩ z sai đừng ném đá :)
Ba nguyên tử X, Y, Z có tổng số điện tích hạt nhân bằng 17, số proton của X nhiều hơn Y 2 proton. Tổng số electron trong ion (X3Y)2- là 32. Nhận xét nào sau đây không đúng.
A. X, Y, Z thuộc cùng một chu kì
B. X, Z thuộc cùng một nhóm
C. Z thuộc nhóm IA
D. Y thuộc nhóm IVA
Đáp án B
Giả sử số hiệu nguyên tử của X, Y lần lượt là ZX, ZY
Ta có hpt 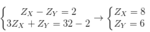
ZZ = 17 - ZX - ZY = 17 - 8 - 6 = 3.
Cấu hình electron của X, Y, Z là
8X: 1s22s22s4 → X thuộc chu kì 2, nhóm VIA.
6Y: 1s22s22p2 → Y thuộc chu kì 2, nhóm IVA.
3Z: 1s22s1 → Z thuộc chu kì 2, nhóm IA.
→ Chọn B.
Ba nguyên tử X, Y, Z có tổng số điện tích hạt nhân bằng 17, số proton của X nhiều hơn Y 2 proton. Tổng số electron trong ion ( X 3 Y ) 2 - là 32. Nhận xét nào sau đây không đúng.
A. X, Y, Z thuộc cùng một chu kì
B. X, Z thuộc cùng một nhóm
C. Z thuộc nhóm IA
D. Y thuộc nhóm IVA
Bài 1: Ion dương R3+. Có tổng số hạt e và n là 5 phần 7. Tính số electron, proton, notron.
Bài 2: x3- : 111, e=48% (p+n).
Ai giỏi giúp với...
Bài 1:
Bạn kham khảo nha
https://hoc24.vn/hoi-dap/tim-kiem?q=m%E1%BB%99t+ion+R3++c%C3%B3+t%E1%BB%95ng+s%E1%BB%91+h%E1%BA%A1t+37.+t%E1%BB%89+s%E1%BB%91+h%E1%BA%A1t+e+%C4%91%E1%BB%91i+v%E1%BB%9Bi+n+l%C3%A0+5/7.t%C3%ACm+p,e,n+trong+R3+&id=85045
Bài 2:
Bạn kham khảo nha
https://vn.answers.yahoo.com/question/index?qid=20100907055220AAODUMU
Hợp chất A được tạo thành từ ion M+ và ion X2-. Tổng số 3 loại hạt trong A là 140. Tổng số các hạt mang điện trong ion M+ lớn hơn tổng số hạt mang điện trong ion X2- là 19. Trong nguyên tử M, số hạt proton ít hơn số hạt nơtron 1 hạt; trong nguyên tử X, số hạt proton bằng số hạt nơtron. Số p trong M và X lần lượt là
A. 19 và 8
B. 11 và 16
C. 11 và 8
D. 19 và 16
Đáp án : A
A là M2X :
2.(2pM + nM) + (2pX + nX) = 140(1)
Số hạt mang điện trong M+ = 2pM – 1
Số hạt mang điện trong X2- = 2pX + 2
=> 2pM – 1 = (2pX + 2) + 19
=> pM – pX = 11(2)
Trong M : pM + 1 = nM(3)
Trong X : pX = nX (4)
Giải hệ (1,2,3,4) ta được :
pM = 19 và pX = 8
Câu 47: Một dung dịch không thể chứa đồng thời các ion sau:
A. NH 4 + , CO 3 2- , SO 4 2- , Na + .
B. K + , Zn 2+ , Cl - , Br - .
C. Ag + , Al 3+ , PO 4 3- , CO 3 2- .
D. Ba 2+ , Mg 2+ , Cl - , NO 3 - .
Câu 48: Các ion nào sau đây không cùng tồn tại trong một dung dịch?
A. Na + , Mg 2+ , OH - .
B. K + , Fe 2+ , NO 3 - .
C. Ca 2+ , Na + , Cl - .
D. Al 3+ , Cu 2+ , SO 4 2-
Câu 47: Một dung dịch không thể chứa đồng thời các ion sau:
A. NH 4 + , CO 3 2- , SO 4 2- , Na + .
B. K + , Zn 2+ , Cl - , Br - .
C. Ag + , Al 3+ , PO 4 3- , CO 3 2- .
D. Ba 2+ , Mg 2+ , Cl - , NO 3 - .
Câu 48: Các ion nào sau đây không cùng tồn tại trong một dung dịch?
A. Na + , Mg 2+ , OH - .
B. K + , Fe 2+ , NO 3 - .
C. Ca 2+ , Na + , Cl - .
D. Al 3+ , Cu 2+ , SO 4 2-
Câu 47: Một dung dịch không thể chứa đồng thời các ion sau:
A. NH 4 + , CO 3 2- , SO 4 2- , Na + .
B. K + , Zn 2+ , Cl - , Br - .
C. Ag + , Al 3+ , PO 4 3- , CO 3 2- .
D. Ba 2+ , Mg 2+ , Cl - , NO 3 - .
Câu 48: Các ion nào sau đây không cùng tồn tại trong một dung dịch?
A. Na + , Mg 2+ , OH - .
B. K + , Fe 2+ , NO 3 - .
C. Ca 2+ , Na + , Cl - .
D. Al 3+ , Cu 2+ , SO 4 2-
Hợp chất Y có công thức M4X3. Biết:
− Tổng số hạt trong phân tử Y là 214 hạt.
− Ion M3+ có số electron bằng số electron của ion X4 −
− Tổng số hạt proton, nơtron, electron của nguyên tử nguyên tố M nhiều hơn tổng số hạt của nguyên tử nguyên tố X trong Y là 106. Y là chất nào dưới đây?
A. Al4Si3
B. Fe4Si3
C. Al4C3
D. Fe4C3
Đáp án C.
Tổng số hạt trong phân tử Y là 214 hạt.
4(2pM + nM) + 3(2pX + nX) = 214 (1)
Ion M3+ có số electron bằng số electron của ion X4 −
pM - 3 = pX + 4 => pX = pM - 7 (2)
Tổng số hạt proton, nơtron, electron của nguyên tử nguyên tố M nhiều hơn tổng số hạt của nguyên tử nguyên tố X trong Y là 106
4(2pM + nM) - 3(2pX + nX) = 106 (3)
(1), (3) => 2pM + nM = 40 (4) và 2pX + nX = 18 (5)
(5),(2),(4) => pX = 6 ; pM = 13 => X là C (Carbon) và M là Al (Nhôm)
Y la Al4C3 (Nhôm carbua)
Trong phân tử M 2 X có tổng số hạt (proton, nơtron, electron) là 140 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion M + lớn hơn số khối của ion X 2 - là 23. Tổng số hạt proton, nơtron, electron trong ion M + nhiều hơn trong ion X 2 - là 31 hạt. Nhận xét nào sau đây không đúng?
A. M 2 X tan trong nước tạo thành dung dịch kiềm.
B. Trong các phản ứng hóa học, M chỉ thể hiện tính khử.
C. X vừa có tính oxi hóa vừa có tính khử.
D. M 2 X là hợp chất ion.