Hòa tan 15 gam hỗn hợp X gồm hai kim loại Mg và Al vào dung dịch Y gồm HNO3 và H2SO4 đặc thu được 0,1 molmỗikhí SO2,NO,NO2,N2O. Phầntrăm khối lượng của Al và Mg trong X lần lượt là
A. 63% và 37%.
B. 36% va 64%.
C. 50% và 50%.
D. 46% và 54%.
Câu 8: Hòa tan 15 gam hỗn hợp X gồm 2 kim loại Mg và Al vào dung dịch gồm HNo3 và H2SO4 đặc thu được 0,1 mol mỗi khí SO2, NO, NO2, N2O. Phần trăm khối lượng của Al và Mg trong X lần lượt là?
\(n_{Mg}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(24a+27b=15\left(1\right)\)
Bảo toàn e :
\(2a+3b=0.1\cdot\left(2+3+1+8\right)\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=0.4,b=0.2\)
\(\%Mg=64\%,\%Al=36\%\)
Gọi số mol Mg và Al lần lượt là a;b(mol)
$\Rightarrow 24a+27b=15$
Bảo toàn e ta có: $2a+3b=1,4$
Giải hệ ta được $a=0,4;b=0,2$
$\Rightarrow \%m_{Mg}=64\%;\%m_{Al}=36\%$
Hoà tan 15 gam hỗn hợp X gồm 2 kim loại Al và Mg vào dung dịch Y gồm HNO3 và H2SO4 đặc thu được 0,1 mol mỗi khí SO2, NO, NO2, N2O (không còn sản phẩm khử khác). % khối lượng Al trong hỗn hợp X là (Al=27, Mg=24)
A. 63%
B. 46%
C. 36%
D. 50%
Đáp án : C
Bảo toàn e :
3nAl + 2nMg= 2 n S O 2 + 3 n N O + n N O 2 + 8 n N 2 O = 1,4 mol
Và 27nAl + 24nMg = 15g
=> nAl = 0,2 mol
=> %mAl = 36%
Hòa tan hoàn toàn 12,84 gam hỗn hợp gồm Fe, Al và Mg có số mol bằng nhau trong dung dịch HNO3 loãng dư, thu được dung dịch X chứa 75,36 gam muối và hỗn hợp khí Y gồm N2, N2O, NO và NO2. Trong Y, số mol N2 bằng số mol NO2. Biết tỉ khối của Y so với H2 bằng 18,5. Số mol HNO3 đã tham gia phản ứng là bao nhiêu ?
Có : nFe = nAl = nMg = 0,12 mol
Y : N2 ; N2O ; NO và NO2( N2 và NO2 có số mol bằng nhau)
=> Qui đổi : NO2 +N2 -> NO + N2O
=> Y trở thành : NO và N2O với số mol lần lượt là x và y.
Có : MY = 37g => mY = 37(x + y) = 30x + 44y
=> x = y(1)
Giả sử có z mol NH4NO3 trong muối
Bảo toàn e : 3nFe + 3nAl + 2nMg = 3nNO + 8nN2O + 8nNH4NO3
=> 3x + 8y + 8z = 0,96 mol(2)
Và : nHNO3 = (4x + 10y + 10z)
=> nH2O = ½ (nHNO3 – 4nNH4NO3) = (2x + 5y + 3z) mol
Bảo toàn khối lượng :
mY = mKL + mHNO3 – mH2O - mmuối X = (216x + 540y + 576z) – 62,52 = 37(x + y)
=> 179x + 503y + 576z = 62,52(3)
Từ (1),(2),(3) => x = y = 0,06 ; z = 0,0375 mol
=> nHNO3 pứ = 4x + 10y + 10z = 1,215 mol
Hòa tan hết 11,54 gam hỗn hợp rắn X gồm Al, Mg, Al(NO3)3, Mg(NO3)2 trong dung dịch chứa H2SO4 và 0,1 mol NaNO3 (đun nhẹ), kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối sunfat (không chứa ion ) và hỗn hợp khí Z gồm NO, N2O và N2. Tỉ khối của Z so với He bằng 99 , 5 11 . Cho dung dịch NaOH 11,5M vào dung dịch Y đến khi kết tủa đạt cực đại thì đã dùng 480ml. Lấy kết tủa nung ngoài không khí đến khối lượng không đổi thu được 12,96 gam rắn. Biết rằng trong X phần trăm khối lượng của Mg chiếm 20,797%. Phần trăm khối lượng của N2O có trong hỗn hợp Z là
A. 66,3%
B. 49,7%
C. 55,3%
D. 44,2%
Đáp án C
![]()
Đặt số mol của Al, Al(NO3)3, Mg(NO3)2 lần lượt là a, b, c
=> 27a + 213b + 148c = 11,54 - 24.0,1 = 9,14 gam (1)
n NaOH = 2 n Mg 2 + + 3 n Al 3 + = 2 ( 0 , 1 + c ) + 3 ( a + b ) = 1 , 5 . 0 , 48 = 0 , 72 mol ( 2 )
Chất rắn thu được sau khi nung là MgO và Al2O3
=> 40.(0,1 + c) + 102 2 .(a+b) = 12,96 gam (3)
Từ (1), (2), (3) suy ra
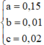
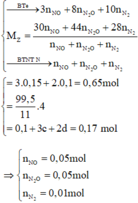
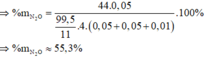
Hòa tan hoàn toàn 27,04 gam hỗn hợp X gồm Mg, Al, Al2O3, Mg(NO3)2 vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol H2SO4 (loãng). Sau khi kết thúc các phản ứng, thu được dung dịch Y chỉ chứa các muối và 0,28 mol hỗn hợp Z gồm N2O, H2. Tỷ khối của Z so với H2 bằng 10. Dung dịch Y tác dụng tối đa với dung dịch chứa 2,28 mol NaOH, thu được 27,84 gam kết tủa. Phần trăm khối lượng của nhôm kim loại có trong X là
A. 23,96%.
B. 31,95%.
C. 27,96%.
D. 15,09%.
Hòa tan hoàn toàn 31,25 gam hỗn hợp X gồm Mg, Al và Zn trong dung dịch HNO3, sau phản ứng hoàn toàn thu được dung dịch Y và hỗn hợp gồm 0,1 mol N2O và 0,1 mol NO. Cô cạn dung dịch sau phản ứng thu được 157,05 gam hỗn hợp muối. Vậy số mol HNO3 đã bị khử trong phản ứng trên là:
A. 0,40 mol
B. 0,5 mol
C. 0,45 mol
D. 0,30 mol
Chọn A
Giả sử sau phản ứng có x mol NH4NO3. Ta có:
Quá trình cho e:
Mg → Mg+2 +2e
Al → Al+3 +3e
Zn → Zn+2 +2e
Quá trình nhận e: N+5 → N+1 - 4e
N+5 → N+2 - 3e
N+5 → N-3 - 8e
DLBT e : 2nMg + 3nAl + 2nZn = 8nN2O + 3nNO + 8nNH4NO3
→ m muối = mKL + mNO3-(muối KL) + mNH4NO3
nNO3- (muối KL)= ne trao đổi
→157,05 = 31,25 + 62(8.0,1+3.0,1+8x) + 80x
x= 0,1 mol → nHNO3 đã bị khử = 2nN2O + nNO +nNH4NO3= 0,4 mol
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là:
A. 13,8;7,6;11,8
B. 11,8;9,6;11,8
C. 12,8;9,6;10,8
D. kết quả khác
Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)
Hòa tan hoàn toàn 12,84 gam hỗn hợp gồm Fe, Al và Mg có số mol bằng nhau trong dung dịch HNO3 loãng (dư), thu được dung dịch X chứa 75,36 gam muối và hỗn hợp khí Y gồm N2, N2O, NO và NO2. Trong Y, số mol N2 bằng số mol NO2. Biết tỉ khối của Y so với H2 bằng 18,5. Số mol HNO3 đã tham gia phản ứng là
A. 1,275 mol.
B. 1,080 mol.
C. 1,140 mol.
D. 1,215 mol.
Đáp án D
Có : nFe = nAl = nMg = 0,12 mol
Y : N2 ; N2O ; NO và NO2( N2 và NO2 có số mol bằng nhau)
=> Qui đổi : NO2 +N2 -> NO + N2O
=> Y trở thành : NO và N2O với số mol lần lượt là x và y.
Có : MY = 37g => mY = 37(x + y) = 30x + 44y
=> x = y(1)
Giả sử có z mol NH4NO3 trong muối
Bảo toàn e : 3nFe + 3nAl + 2nMg = 3nNO + 8nN2O + 8nNH4NO3
=> 3x + 8y + 8z = 0,96 mol(2)
Và : nHNO3 = (4x + 10y + 10z)
=> nH2O = ½ (nHNO3 – 4nNH4NO3) = (2x + 5y + 3z) mol
Bảo toàn khối lượng :
mY = mKL + mHNO3 – mH2O - mmuối X = (216x + 540y + 576z) – 62,52 = 37(x + y)
=> 179x + 503y + 576z = 62,52(3)
Từ (1),(2),(3) => x = y = 0,06 ; z = 0,0375 mol
=> nHNO3 pứ = 4x + 10y + 10z = 1,215 mol
Hòa tan hoàn toàn 12,84 gam hỗn hợp gồm Fe, Al và Mg có số mol bằng nhau trong dung dịch HNO3 loãng (dư), thu được dung dịch X chứa 75,36 gam muối và hỗn hợp khí Y gồm N2, N2O, NO và NO2. Trong Y, số mol N2 bằng số mol NO2. Biết tỉ khối của Y so với H2 bằng 18,5. Số mol HNO3 đã tham gia phản ứng là
A. 1,275 mol
B. 1,080 mol
C. 1,140 mol
D. 1,251 mol