Hòa tan hết 1,84 gam hỗn hợp Cu và Fe trong dung dịch H2SO4 dư, đặc, nóng, thu được 0,035 mol SO2. Số mol Fe và Cu trong hỗn hợp ban đầu lần lượt là:
A. 0,02 và 0,03
B. 0,01 và 0,02
C. 0,01 và 0,03
D. 0,02 và 0,04
Hòa tan hết 1,84 gam hỗn hợp Cu và Fe trong dung dịch HNO3 dư, thu được 0,01 mol NO và 0,04 mol NO2. Số mol Fe và Cu trong hỗn hợp ban đầu lần lượt là :
A. 0,02 và 0,03
B. 0,01 và 0,02
C. 0,01 và 0,03
D. 0,02 và 0,04
Đáp án B.
Gọi nCu = y, nFe = x mol

Áp dụng định luật bảo toàn e ta có: 3x+2y = 0,07 (1)
Khối lượng hai kim loại = 1,84 g: 56x+64y = 1,84 (2).
Giải 1,2 ta có: x = 0,01, y = 0,02 (mol)
Hòa tan hỗn hợp gồm 0,02 mol Cu, 0,03 mol Al và 0,01 mol Mg vào hỗn hợp dung dịch H2SO4 đặc, nóng + HNO3 đặc nóng dư thu đc 0,05 mol khí SO2 và a mol khí NO2 ( ko có khí nào khác ngoài 2 khí trên). Vậy a có trị là bao nhiêu ?
Hòa tan m gam Mg trong 500ml dung dịch chứa hỗn hợp H2SO4 0,4M và Cu(NO3)2 đến phản ứng hoàn toàn thu được dung dịch X; 2 gam hỗn hợp kim loại và hỗn hợp khí X gồm 0,03 mol H2 và 0,02 mol N2. Giá trị của m là
A. 5,08. .
B. 3,52.
C. 3,12.
D. 4,64
Đáp án A
Khí X có chứa H2 à dung dịch X không có muố nitrat;
Sau phản ứng thu được hỗn hợp kim loại à Mg dư à H+ đã phản ứng hết
Số mol H+ phản ứng = 0,4 (mol); Số mol H+ tạo ra H2 và N2 = 0,3 à có muối amoni trong dung dịch X
Số mol NH4+ = 0 , 4 - 0 , 3 10 = 0 , 01 (mol)à Số mol Cu(NO3)2 (bđ) = 0,025 (mol)
Theo bảo toàn e à số mol Mg phản ứng = 0,195 (mol); khố lượng Mg dư = 0,4 gam
à Khối lượng Mg (ban đầu) = 5,08 gam
Hòa tan hoàn toàn hỗn hợp gồm 0,02 mol FeS2 và 0,03 mol FeS vào dung dịch H2SO4 đặc nóng thu được Fe2(SO4)3, SO2 và H2O. Hấp thụ hết SO2 bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch Y trong suốt có pH =2. Thể tích dung dịch Y là
A. 11,4 l
B. 5,7 l
C. 17,1 l
D. 22,8 l
Đáp án D
Ta có :
Fe → Fe3+ + 3e
S → S+6 + 6e
S+6 + 2e → S+4
Do đó số mol SO2 là (0,05 . 3 + 0,07.6 ) / 2= 0,285 mol
5SO2 + 2H2O + 2KMnO4 → K2SO4 + 2 MnSO4 + 2H2SO4
Nên số mol H2SO4 tạo ra là 0,114 mol
=> [H+] = 0,228 : V =0,01 => V =22,8 l
Nung hỗn hợp A gồm x mol Fe và 0,15 mol Cu trong không khí một thời gian thu được 63,2 gam hỗn hợp chất rắn B. Hòa tan hết hỗn hợp B bằng dung dịch H2SO4 đặc nóng, dư thu được 6,72 lít khí SO2 (đktc). Giá trị của X là:
A. 0,4 mol.
B. 0,5 mol.
C. 0,6 mol.
D. 0,7 mol.
Đáp án C
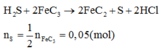
Chú ý: Không tồn tại muối sunfua của Al và Fe(III). H2S không phản ứng với AlCl3 nhưng nếu
![]()
Có sự khác nhau này do Fe3+ có tính oxi hóa mạnh còn Al3+ tính oxi hóa yếu
Nung hỗn hợp A gồm x mol Fe và 0,15 mol Cu trong không khí một thời gian thu được 63,2 gam hỗn hợp chất rắn B. Hòa tan hết hỗn hợp B bằng dung dịch H2SO4 đặc nóng, dư thu được 6,72 lít khí SO2 (đktc). Giá trị của X là:
A. 0,4 mol.
B. 0,5 mol.
C. 0,6 mol.
D. 0,7 mol.
Câu 17: Cho 8,9g hỗn hợp Zn, Mg tan hoàn toàn trong H2SO4 đặc nóng thu được dung dịch X và 0,15 mol SO2 ; 0,01 mol S ; 0,005 mol H2S. Tính khối lượng của mỗi kim loại trong hỗn hợp?
2 2. Hoà tan 37,1 g hh X gồm Fe, Zn, Cu trong dd H2SO4 đđ, nóng dư thu được dung dịch A và 15,68 lít khí SO2 (sản phẩm khử duy nhất). 37,1 g X tác dụng với dd HCl dư thì thu được 11,2 lít khí (đkc). Tính % khối lượng mỗi kim loại trong hh X.
Câu 23. Cho 7,6 gr hỗn hợp gồm Fe, Mg, Cu vào dung dịch H2SO4 đ, nguội dư thì thu được 3,08 lit khí SO2 (đkc). Phần không tan cho tác dụng với dung dịch HCl dư thu được 1,12 lit khí (đkc).Tính % khối lượng hỗn hợp đầu
Hòa tan hoàn toàn hỗn hợp X gồm Cu, Fe, Mg vào dung dịch HNO3 dư, sau phản ứng thu được dung dịch Y chỉ chứa muối của kim loại và hỗn hợp khí gồm 0,01 mol N2, 0,02 mol NO. Số mol HNO3 đã phản ứng là
A. 0,10
B. 0,12
C. 0,16
D. 0,20
Ở ví dụ 4, ta đã giải quyết câu hỏi này bằng bảo toàn nguyên tố, giờ với phương trình liên hệ mol H+ và sản phẩm khử, ta có ngay: nH+ = 12nN2 + 4nNO = 12.0,01 + 4.0,02 =0,2 mol
Chọn đáp án D
Hòa tan hoàn toàn hỗn hợp gồm 0,02 mol FeS2 và 0,03 mol FeS vào lượng dung dịch H2SO4 đặc nóng thu được Fe2(SO4)3, SO2 và H2O. Hấp thụ hết SO2 bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch Y không màu, trong suốt có pH = 2. Thể tích của dung dịch Y là
A. 11,4 lít
B. 5,7 lít
C. 17,1 lít
D. 22,8 lít
Bảo toàn electron: 15nFeS2 + 9nFeS = 2nSO2
⇒ nSO2 = 0,285 mol.
Phản ứng: 5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
∑nH+ = 0,285 × 2 ÷ 5 × 2 = 0,228 mol
⇒ VY = 0,228 ÷ 10 – 2 = 22,8 lít.
Đáp án D