cho hỗn hợp gồm đồng và sắt tác dụng một với một lượng dung dịch axit sunfuric loãng thu được 6,72 lít khí hidro ở điều kiện tiêu chuẩn và chất rắn a đem nung A trong trong không khí đến khối lượng không đổi cân được 4 g tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp cu

Những câu hỏi liên quan
cho 10.6g hỗn hợp gồm đồng và magie tác dụng với dung dịch axit sunfuric loãng dư sau phản ứng lọc lấy phần chất sắt ko tan cho tác dụng dung dịch axit sunfuric nóng thu được 0.112l khí ở điều khiện tiêu chuẩn tính khối lượng mỗi kim lọa trong hỗn hợp ban đầu
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
\(Cu+2H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}CuSO_4+SO_2\uparrow+2H_2O\)
Ta có: \(n_{SO_2}=\dfrac{0,112}{22,4}=0,005\left(mol\right)=n_{Cu}\)
\(\Rightarrow m_{Cu}=0,005\cdot64=0,32\left(g\right)\) \(\Rightarrow m_{Mg}=10,6-0,32=10,28\left(g\right)\)
Đúng 1
Bình luận (0)
Đun nóng hỗn hợp X gồm bột Fe và S trong điều kiện không có không khí, thu được hỗn hợp rắn A. Cho A tác dụng với một lượng dư dung dịch HCl thu được sản phẩm khí Y cñ tỉ khối so với H2 là 13. Lấy 2,24 lít (đo ở điều kiện tiêu chuẩn) khí Y đem đốt cháy rồi cho toàn bộ sản phẩm cháy đñ đi qua 100 ml dung dịch H2O2 5,1% (có khối lượng riêng bằng 1g/ml), sau phản ứng thu được dung dịch B. Các phản ứng xảy ra hoàn toàn.a. Tính thành phần % khối lượng các chất trong hỗn hợp X. (%Fe 70%; %S 30%)b. X...
Đọc tiếp
Đun nóng hỗn hợp X gồm bột Fe và S trong điều kiện không có không khí, thu được hỗn hợp rắn A. Cho A tác dụng với một lượng dư dung dịch HCl thu được sản phẩm khí Y cñ tỉ khối so với H2 là 13. Lấy 2,24 lít (đo ở điều kiện tiêu chuẩn) khí Y đem đốt cháy rồi cho toàn bộ sản phẩm cháy đñ đi qua 100 ml dung dịch H2O2 5,1% (có khối lượng riêng bằng 1g/ml), sau phản ứng thu được dung dịch B. Các phản ứng xảy ra hoàn toàn.
a. Tính thành phần % khối lượng các chất trong hỗn hợp X. (%Fe = 70%; %S = 30%)
b. Xác định nồng độ % các chất trong dung dịch B. (C%H2SO4 = 6,695%; C%H2O2 = 2,392%)Đun nóng hỗn hợp X gồm bột Fe và S trong điều kiện không có không khí, thu được hỗn hợp rắn A. Cho A tác dụng với một lượng dư dung dịch HCl thu được sản phẩm khí Y cñ tỉ khối so với H2 là 13. Lấy 2,24 lít (đo ở điều kiện tiêu chuẩn) khí Y đem đốt cháy rồi cho toàn bộ sản phẩm cháy đñ đi qua 100 ml dung dịch H2O2 5,1% (có khối lượng riêng bằng 1g/ml), sau phản ứng thu được dung dịch B. Các phản ứng xảy ra hoàn toàn.
a. Tính thành phần % khối lượng các chất trong hỗn hợp X. (%Fe = 70%; %S = 30%)
b. Xác định nồng độ % các chất trong dung dịch B. (C%H2SO4 = 6,695%; C%H2O2 = 2,392%)
a) PTHH : Fe + S \(\rightarrow\) FeS
=> A gồm : Fe , FeS
Fe + 2 HCl -> FeCl2 + H2
FeS + 2 HCL -> FeCl2 + H2S
=> Y gồm : H2 , H2S
nY = n H2 + n H2S = 0,1 mol (I)
dY/H2 = 13 -> m Y = 2.nH2 + 34.n H2S = 13.2.0,1 = 2,6 g (II)
Từ (I),(II) => n H2 = 0,025 mol ; n H2S = 0,075 mol
Fe + 2 HCl \(\rightarrow\) FeCl2 + H2
0,025<---------------------0,025 mol
FeS + 2 HCl \(\rightarrow\) FeCl2 + H2S
0,075<-------------------------0,075 mol
Ta có: n S = n Fe phản ứng = n FeS = 0,075 mol
=>m S =0,075.32 = 2,4 g
n Fe ban đầu = 0,075 + 0,025 = 0,1mol
=>m Fe=0,1.56 = 5,6 g
=> %m S = \(\dfrac{2,4}{2,4+5,6}.100=30\%\)
=> %m Fe = 100 - 70 = 30%
b ) 2 H2 + O2 \(\rightarrow\) 2 H2O
0,025-------------->0,025 mol
2 H2S + 3 O2 \(\rightarrow\) 2 SO2 + 2 H2O
0,075--------------->0,075--->0,075 mol
m H2O2 = 5,1 g -> n H2O2 = 0,15 mol
PTHH : SO2 + H2O2 \(\rightarrow\) H2SO4
Ban đầu :0,075---->0,15 mol
Phản ứng:0,075--->0,075------>0,075 mol
Sau phản ứng:0----->0,075----->0,075 mol
m dd sau phản ứng = 18.(0,025 + 0,075 ) + 64.0,075 + 100 = 106,6 g
m H2O2 dư = 0,075.34 =2,55g
\(\Rightarrow C\%_{H_2O_2dư}=\dfrac{2,55}{106,6}.100=2,392\%\)
m H2SO4 = 0,075.98 = 7,35g
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{7,35}{106,6}.100=6,895\%\)
Đúng 1
Bình luận (1)
Cho 10gam hỗn hợp đồng và đồng oxit tác dụng với dung dịch axit sunfuric loãng lọc lấy chất rắn không tan cho vào dung dịch axit sunfuric đặc nóng thì thu được khí A ở điều kiện tiêu chuẩn a) viết pt cho biết tên của khí A b) tính phần trăm khối lượng của mỗi chất hỗn hợp
a, \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\)
Khí A: SO2 - lưu huỳnh đioxit
b, Đề có cho thể tích khí A không bạn nhỉ?
Đúng 2
Bình luận (0)
Cho 19,2 gam hỗn hợp A gồm Mg, Fe vào 400 ml dung dịch B chứa AgNO3 1M và Cu(NO3)2 0,25M. Khuấy đều đến khi dung dịch B mất màu hoàn toàn thu được 55,2 gam hỗn hợp chất rắn C gồm 3 kim loại và dung dịch D. Hòa tan hoàn toàn C trong dung dịch HNO3 loãng dư thu được 6,72 lít khí E duy nhất. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc, rửa, sấy khô và nung kết tủa trong không khí đến khối lượng không đổi thu được m gam chất rắn khan. Xác định khí E và tính m biết các chất đo ở điều kiện tiê...
Đọc tiếp
Cho 19,2 gam hỗn hợp A gồm Mg, Fe vào 400 ml dung dịch B chứa AgNO3 1M và Cu(NO3)2 0,25M. Khuấy đều đến khi dung dịch B mất màu hoàn toàn thu được 55,2 gam hỗn hợp chất rắn C gồm 3 kim loại và dung dịch D. Hòa tan hoàn toàn C trong dung dịch HNO3 loãng dư thu được 6,72 lít khí E duy nhất. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc, rửa, sấy khô và nung kết tủa trong không khí đến khối lượng không đổi thu được m gam chất rắn khan. Xác định khí E và tính m biết các chất đo ở điều kiện tiêu chuẩn.
A. NO; 18,4 g
B. NO2; 20 g
C. N2O; 18,4 g
D. NO; 20 g
Đáp án D
Dung dịch B mất màu hoàn toàn => Cu2+ phản ứng hết
3 kim loại là Ag, Cu, Fe dư.
mFe dư =55,2-108.0,4-64.0,1=5,6 gam
Đặt số mol Mg và Fe phản ứng lần lượt là x, y
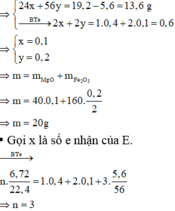
=> Khí E là NO
Đúng 0
Bình luận (0)
Trộn 21,6 gam bột Al với m gam hỗn hợp X gồm
FeO
,
Fe
2
O
3
và
Fe
3
O
4
được hỗn hợp Y. Nung Y ở nhiệt độ cao trong điều kiện không có không khí đến phản ứng hoàn toàn thu được chất rắn Z. Cho Z tác dụng vớii dung dịch NaOH dư thu được 6,72 lít khí. Nếu cho Z tác dụng với
HNO...
Đọc tiếp
Trộn 21,6 gam bột Al với m gam hỗn hợp X gồm FeO , Fe 2 O 3 và Fe 3 O 4 được hỗn hợp Y. Nung Y ở nhiệt độ cao trong điều kiện không có không khí đến phản ứng hoàn toàn thu được chất rắn Z. Cho Z tác dụng vớii dung dịch NaOH dư thu được 6,72 lít khí. Nếu cho Z tác dụng với HNO 3 , loãng dư thì thu được 19,04 lít khí NO là sản phẩm khử duy nhất. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
A. 50,8
B. 46,0
C. 58,6
D. 62,0
Cho 15,2g hỗn hợp 2 bột sắt và đồng vào 400ml đúng dịch axit sunfuaric loãng sau phản ứng thu được 4,48 lít khí ở điều kiện tiêu chuẩn và còn 1 chất rắn không tan
a,Tính khối lượng mỗi kim loại trong hỗn hợp bạn đầu
Xem chi tiết
Chất rắn không tan là Cu.
\(Fe + H_2SO_4 \to FeSO_4 + H_2\)
Ta có :
\(n_{Fe} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)\\ \Rightarrow m_{Fe} = 0,2.56 = 11,2(gam)\\ \Rightarrow m_{Cu} = 15,2 - 11,2 = 4(gam)\)
Đúng 2
Bình luận (2)
Cho 6,4 g hỗn hợp X gồm Mg,Al phản ứng với dung dịch axit sunfuric loãng dư thu được 7,28 lít khí ở điều kiện tiêu chuẩn a) Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp.b) nếu cho 12,9 g hỗn hợp X trên tác dụng với dung dịch axit sunfuric đặc nóng dư thì thu được bao nhiêu lít khí SO2 là sản phẩm khử duy nhất (đktc)
Sửa đề: 6,4 gam hh \(\rightarrow\) 6,45 gam hh
a) Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow24a+27b=6,45\) (1)
Ta có: \(n_{H_2}=\dfrac{7,28}{22,4}=0,325\left(mol\right)\)
Bảo toàn electron: \(2a+3b=0,65\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=n_{Mg}=0,1\left(mol\right)\\b=n_{Al}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1\cdot24}{6,4}\cdot100\%=37,5\%\\\%m_{Mg}=62,5\%\end{matrix}\right.\)
b) Ta thấy với 6,45 gam hh thì có 0,1 mol Mg và 0,15 mol Al
\(\Rightarrow\) Trong 12,9 gam hh thì chứa 0,2 mol Mg và 0,3 mol Al
Gọi \(n_{SO_2}=x\left(mol\right)\)
Bảo toàn electron: \(2\cdot0,2+3\cdot0,3=2x\) \(\Rightarrow x=n_{SO_2}=0,65\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,65\cdot22,4=14,56\left(l\right)\)
Đúng 2
Bình luận (0)
gọi số mol của Mg là x mol ; Al là y mol => 24x + 27y =6,4
n khí = 7,28/22,4=0,325 mol
bảo toàn e ta có
Mg + H2SO4 --> MgSO4 + H2
x x mol
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
y 3/2 y mol
=> x + 3/2y=0,325
=> x=11/120 mol ; y=7/45 mol
=> mMg11/120*24=2,2g => %mMg = 2,2*100/6,4=34,375%
=>%mAl=100-34,375=65,625%
Đúng 0
Bình luận (2)
Hỗn hợp X gồm Al, Fe2O3, Fe3O4 và CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít CO (điều kiện tiêu chuẩn) sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dung dịch HNO3 loãng dư thu được dung dịch T và 7,168 lít NO (điều kiện tiêu chuẩn, sản phẩm khử duy nhất). Cô cạn dung dịch T thu được 3,456m gam muối khan. Giá trị của m gần với giá trị nào sau đây nhất? A. 42,5 B. 35,0 C. 38,5 D...
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3, Fe3O4 và CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít CO (điều kiện tiêu chuẩn) sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dung dịch HNO3 loãng dư thu được dung dịch T và 7,168 lít NO (điều kiện tiêu chuẩn, sản phẩm khử duy nhất). Cô cạn dung dịch T thu được 3,456m gam muối khan. Giá trị của m gần với giá trị nào sau đây nhất?
A. 42,5
B. 35,0
C. 38,5
D. 40,5D. 40,5
Đáp án C
· X gồm 0,2539m (g) O và 0,7461m (g) kim loại.
· Hỗn hợp khí Z gồm CO dư và CO2
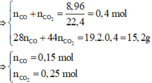
Þ Y gồm 0,7461m (g) kim loại và 0,2539m – 16.0,25 = 0,2539m – 4 (g) O
· Y + HNO3 → 0,32 mol NO + 3,456m g muối
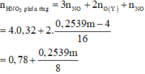
Þ Dung dịch T chứa
n NO 3 - = 0 , 78 + 0 , 2359 m 8 - 0 , 32 = 0 , 46 + 0 , 2359 m 8 ⇒ m muối = 0 , 7461 m + 62 . 0 , 46 + 0 , 2359 m 8 = 3 , 456 m ⇒ m = 38 , 43 g
Gần nhất với giá trị 38
Đúng 0
Bình luận (0)
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37%. B. 48,21% và 9,23%. C. 42,86% va 48,21%. D. 48,21% và 42,56%.
Đọc tiếp
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%.
B. 48,21% và 9,23%.
C. 42,86% va 48,21%.
D. 48,21% và 42,56%.
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n Cu = n SO 2 = 0 , 075 mol.
Đặt n Cr = x mol; n Fe = y mol → m X 52x + 56y + 0,075 × 64 = 18,2 gam.
x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
mCr trong X = 42,86% và %mCu trong X = 26,37%
Đáp án A
Đúng 0
Bình luận (0)

















