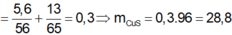Cho 2,8 gam bột sắt phản ứng hoàn toàn với khí Clo dư sau phản ứng khối lượng muối thu được là

Những câu hỏi liên quan
Cho 11,2 gam bột sắt tác dụng với khí clo dư. Sau phản ứng thu được 32,5 gam muối sắt. Khối lượng khí clo tham gia phản ứng là
A. 21,3 gam
B. 20,50 gam
C. 10,55 gam
D. 10,65 gam
Cho 5,6 gam bột sắt vào bình khí clo có dư. Sau phản ứng thu được 16,25 gam muối sắt. Tính khối lượng khí clo đã tham gia phản ứng.
Phương trình hoá học : 2Fe + 3 Cl 2 → t ° FeCl 3
Theo định luật bảo toàn khối lượng :
m Fe + m Cl 2 = m FeCl 3
m Cl 2 = m FeCl 3 - m Fe = 16,25 - 5,6 = 10,65g
Đúng 0
Bình luận (0)
Cho 4,6 gam hỗn hợp X gồm Al và Zn ở dạng bột phản ứng hoàn toàn với dung dịch NaOH đặc dư, sau phản ứng thu được 2,8 lít khí H2 (dktc). Phần trăm khối lượng của Zn trong X là?
Nung 5,6 gam bột sắt và 13 gam kẽm với một lượng dư bột lưu huỳnh, sau phản ứng thu được rắn X. Hòa tan hoàn toàn X trong dung dịch axit clohidric thu được khí Y. Dẫn khí Y vào V lit dung dịch CuSO4 dư, sau phản ứng hoàn toàn thu được m gam kết tủa. Gía trị của m là: A. 9,6 gam B. 19,2 gam C. 18,6 gam D. 28,8 gam
Đọc tiếp
Nung 5,6 gam bột sắt và 13 gam kẽm với một lượng dư bột lưu huỳnh, sau phản ứng thu được rắn X. Hòa tan hoàn toàn X trong dung dịch axit clohidric thu được khí Y. Dẫn khí Y vào V lit dung dịch CuSO4 dư, sau phản ứng hoàn toàn thu được m gam kết tủa. Gía trị của m là:
A. 9,6 gam
B. 19,2 gam
C. 18,6 gam
D. 28,8 gam
Cho 7,35 gam hỗn hợp hồn 2 kim loại kẽm,sắt tác dụng với khí Clo vừa đủ để phản ứng xảy ra hoàn toàn,sau phản ứng thu được 17,645 gam hỗn hợp muối X
a)Xác định % các chất có trong hỗn hợp X?
b)Cho hỗn hợp muối X tác dụng hoàn toàn với lượng dư dung dịch AgNO3.Thu được a gam kết tủa.Xác định giá trị của a?
Xem chi tiết
đốt cháy 16,8g bột sắt trog khí Cl dư, sau phản ứng hoàn toàn thu đc a gam muối. bt lượng khí Cl dùng dư 20% so vs lượng phản ứng. tính a và thể tích khí Cl
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
Theo PTHH :
$n_{FeCl_3} = n_{Fe} = \dfrac{16,8}{56} = 0,3(mol)$
$a = 0,3.162,5 = 48,75(gam)$
$n_{Cl_2\ pư} = \dfrac{3}{2}n_{Fe} = 0,45(mol)$
$n_{Cl_2\ dư} = 0,45.20\% = 0,09(mol)$
$V_{Cl_2} = (0,45 + 0,09).22,4 = 12,096(lít)$
Đúng 2
Bình luận (0)
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt), sau phản ứng thu được 16,38 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong thu được phần không tan Z và 3,36 lít khí (đktc). Cho Z tan hoàn toàn trong 40,5 gam dung dịch
H
2
S
O
4
98% (nóng, vừa đủ). Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al ban đầu và công thức oxit sắt là A. 6,12 gam và
F...
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt), sau phản ứng thu được 16,38 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong thu được phần không tan Z và 3,36 lít khí (đktc). Cho Z tan hoàn toàn trong 40,5 gam dung dịch H 2 S O 4 98% (nóng, vừa đủ). Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al ban đầu và công thức oxit sắt là
A. 6,12 gam và F e 3 O 4 .
B. 6,12 gam và F e 2 O 3 .
C. 5,94 gam và F e 2 O 3
D. 5,94 gam và F e 3 O 4
Đ á p á n D A l F e x O y → t o , H = 100 % Y → N a O H H 2 ⏟ o , 15 m o l ⇒ Y : A l , F e A l 2 O 3 Z c h ứ a F e V ớ i Y : B T e : 3 n A l = 2 n H 2 V ớ i Z : 3 n F e = 2 n S O 2 n S O 4 2 - t ạ o m u ố i = n S O 2 = x 2 x = n H 2 S O 4 = 0 , 405 ⇒ n A l = 0 , 1 x = 0 , 2025 n F e = 0 , 135 n A l 2 O 3 / Y = 0 , 06 ⇒ m A l / X = 27 0 , 1 + 0 , 06 . 2 = 5 , 92 g a m n F e n O = 0 , 135 0 , 06 . 3 = 3 4 ⇒ F e 3 O 4
Đúng 0
Bình luận (0)
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt) sau phản ứng thu được 16,38 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong thu được phần không tan Z và 3,36 lít khí (đktc). Cho Z tan hoàn toàn trong 40,5 gam dung dịch H2SO4 98% (nóng, vừa đủ). Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al ban đầu và công thức oxit sắt là A. 6,12 gam và Fe2O3 B. 5,94 gam và Fe2O3 C. 6,12 gam và Fe3O4 D. 5,94 gam và Fe3O4
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt) sau phản ứng thu được 16,38 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong thu được phần không tan Z và 3,36 lít khí (đktc). Cho Z tan hoàn toàn trong 40,5 gam dung dịch H2SO4 98% (nóng, vừa đủ). Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al ban đầu và công thức oxit sắt là
A. 6,12 gam và Fe2O3
B. 5,94 gam và Fe2O3
C. 6,12 gam và Fe3O4
D. 5,94 gam và Fe3O4
Đáp án : D
Vì các phản ứng hoàn toàn
Y + NaOH có H2 => Al dư
=> nAl dư = 2 3 n H 2 = 0,1 mol
=> Oxit chuyển hết thành Fe
n H 2 S O 4 = 0,405 mol => nFe = 0,135 mol
Y gồm 0,1 mol Al ; Al2O3 và 0,135 mol Fe
=> n A l 2 O 3 = 0,06 mol
Bảo toàn Al : nAl bđ = nAl dư + 2 n A l 2 O 3 = 0,22 mol
=> mAl bđ = 5,94g
Ta có : nFe : nO = 0,135 : 0,18 = 3 : 4
=> Oxit là Fe3O4
Đúng 0
Bình luận (0)
Cho bột sắt dư phản ứng hoàn toàn với 3,7185lit khí Cl2 (25 độ C, 1Bar). Sau phản ứng toàn bộ muối thu được hoà tan hoàn toàn trong 500ml nước cất. Nồng độ mol dung dịch thu được là:
0,3M
0,2M
0,15M
0,4M
\(n_{Cl_2}=\dfrac{0,99.3,7185}{0,082.\left(273+25\right)}=0,15\left(mol\right)\)
PTHH: 2Fe + 3Cl2 --to--> 2FeCl3
__________0,15-------->0,1________(mol)
=> \(C_{M\left(FeCl_3\right)}=\dfrac{0,1}{0,5}=0,2M\)
Đúng 0
Bình luận (0)