cho nổ 1 hỗn hợp gồm 1 mol hidro và 2 mol khí oxi <dktc> . Chất nào còn dư

Những câu hỏi liên quan
Đốt nóng hỗn hợp X gồm Fe2O3 và bột Al trong môi trường không có không khí. Nếu cho những chất còn lại sau phản ứng tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2; còn nếu cho tác dụng với dung dịch HCl dư thu được 0,4 mol H2. Vậy số mol Al trong hỗn hợp X là: A. 0,3 B. 0,4 C. 0,25 D. 0,6
Đọc tiếp
Đốt nóng hỗn hợp X gồm Fe2O3 và bột Al trong môi trường không có không khí. Nếu cho những chất còn lại sau phản ứng tác dụng với dung dịch NaOH dư sẽ thu được 0,3 mol H2; còn nếu cho tác dụng với dung dịch HCl dư thu được 0,4 mol H2. Vậy số mol Al trong hỗn hợp X là:
A. 0,3
B. 0,4
C. 0,25
D. 0,6
Đáp án A
Khi cho Al phản ứng với NaOH hoặc HCl thì số mol H2 thu được là như nhau:
nH2= 0,3 mol ⇒ nAl = 0,2 mol
Từ đó suy ra nH2 do Fe tạo ra = 0,4 - 0,3 = 0,1 mol
⇒nFe = 0,1 mol ⇒ nAl đã phản ứng tạo Fe là 0,1 mol vì:

⇒∑n Al trong X = 0,1 + 0,2 = 0,3mol
Đúng 0
Bình luận (0)
Nung nóng 1,26 mol hỗn hợp X gồm Mg, Fe(NO3)2 và FeCO3 trong một bình kín đến khới lượng không đổi thu được chất rắn Y và 13,44 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ chất rắn Y tác dụng với dung dịch hỗn hợp 2,7 mol HCl và 0,38 mol HNO3 đun nhẹ thu được dung dịch A và 7,168 lít hỗn hợp khí B (đktc) gồm NO và N2O. Cho toàn bộ dung dịch A tác dụng với một lượng dư dung dịch AgNO3, thu được 0,448 lít NO (đktc) l...
Đọc tiếp
Nung nóng 1,26 mol hỗn hợp X gồm Mg, Fe(NO3)2 và FeCO3 trong một bình kín đến khới lượng không đổi thu được chất rắn Y và 13,44 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ chất rắn Y tác dụng với dung dịch hỗn hợp 2,7 mol HCl và 0,38 mol HNO3 đun nhẹ thu được dung dịch A và 7,168 lít hỗn hợp khí B (đktc) gồm NO và N2O. Cho toàn bộ dung dịch A tác dụng với một lượng dư dung dịch AgNO3, thu được 0,448 lít NO (đktc) là sản phẩm khử duy nhất và m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây
A. 413
B. 415
C. 411
D. 414
Nung nóng 1,26 mol hỗn hợp X gồm Mg, Fe(NO3)2 và FeCO3 trong một bình kín đến khới lượng không đổi thu được chất rắn Y và 13,44 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ chất rắn Y tác dụng với dung dịch hỗn hợp 2,7 mol HCl và 0,38 mol HNO3 đun nhẹ thu được dung dịch A và 7,168 lít hỗn hợp khí B (đktc) gồm NO và N2O. Cho toàn bộ dung dịch A tác dụng với một lượng dư dung dịch AgNO3, thu được 0,448 lít NO (đktc) l...
Đọc tiếp
Nung nóng 1,26 mol hỗn hợp X gồm Mg, Fe(NO3)2 và FeCO3 trong một bình kín đến khới lượng không đổi thu được chất rắn Y và 13,44 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ chất rắn Y tác dụng với dung dịch hỗn hợp 2,7 mol HCl và 0,38 mol HNO3 đun nhẹ thu được dung dịch A và 7,168 lít hỗn hợp khí B (đktc) gồm NO và N2O. Cho toàn bộ dung dịch A tác dụng với một lượng dư dung dịch AgNO3, thu được 0,448 lít NO (đktc) là sản phẩm khử duy nhất và m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 413
B. 415
C. 411
D. 414
trộn 0.2 mol H2 và 0.08 mol O2 thu được hỗn hợp khí X ;nung nóng X để PƯ xảy ra với H =75% thì thu được hỗn hợp Y gồm khí và hơi . Tính khối lượng mỗi chất trong Y
2H2 + O2 --to--> 2H2O
Xét \(\dfrac{0,2}{2}>\dfrac{0,08}{1}\) => H2 dư, O2 hết
=> Hiệu suất phản ứng tính theo O2
\(n_{O_2\left(pư\right)}=\dfrac{0,08.75}{100}=0,06\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
____0,12<-0,06------>0,12
=> \(Y\left\{{}\begin{matrix}m_{O_2}=\left(0,08-0,06\right).32=0,64\left(g\right)\\m_{H_2}=\left(0,2-0,12\right).2=0,16\left(g\right)\\m_{H_2O}=0,12.18=2,16\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Hỗn hợp X gồm Cu và Fe có tỉ lệ khối lượng tương ứng là 7 : 3. Lấy m gam X phản ứng hoàn toàn với dung dịch chứa 0,7 mol HNO3. Sau phản ứng còn lại 0,75m gam chất rắn và có 0,25 mol khí Y gồm NO và NO2. Giá trị của m là:
A. 40,5
B. 50,4
C. 50,2
D. 50
Đáp án B
Ta có:
![]()
mCu = 0,7m (g)
Vì Fe phản ứng trước Cu và sau khi phản ứng còn 0,75m (g) chất rắn → Cu chưa phản ứng 0,7m
Fe dư 0,75m - 0,7m = 0,05m → mFe pư = 0,2m - 0,05m = 0,25m (g)
Fe dư → Chỉ tạo muối Fe(NO3)2
HNO3 hết (Lưu ý chỉ H+ hết, NO3- còn trong muối).
Quá trình nhường electron:

Quá trình nhận electron:
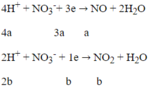
Áp dụng định luật bảo toàn electron:
![]()
→ m = 50,4
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm Na và Al có tỉ lệ mol tương ứng là 1 : 2 vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là:
A. 10,8
B. 5,4
C. 7,8
D. 43,2
Đáp án B
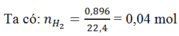
Gọi: nNa = x mol ⇒ nAl = 2x mol
Phản ứng:
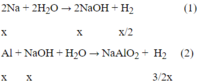
Sau các phản ứng còn m(g) chất rắn không tan, đó là khối lượng của Al dư.
Theo phản ứng (1), (2)
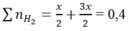
![]()
⇒mAl ban đầu = 2x = 0,2.2 = 0,4 mol
Mà: nAl phản ứng = nNaOH = x = 0,2 mol ⇒ nAl dư = 0,4 - 0,2 = 0,2 mol
⇒mAl = 0,2.27 = 5,4 (g)
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm Na và Al có tỉ lệ mol tương ứng là 1: 2 vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là: A.2,7g B.4,05g C.5,4g D.6,75g
Đọc tiếp
Cho hỗn hợp gồm Na và Al có tỉ lệ mol tương ứng là 1: 2 vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là:
A.2,7g
B.4,05g
C.5,4g
D.6,75g
Đáp án C
Ta có: nH2= 0,04 mol
Gọi: nNa = x mol " nAl = 2x mol
Phản ứng:
2Na + 2H2O → 2NaOH + H2 (1)
x x x 2
Al + NaOH + H2O → NaAlO2 + 3 2 H2 (2)
x x 3 2 x
Sau các phản ứng còn m(g) chất rắn không tan, đó là khối lượng của Al dư.
Theo phản ứng (1) ; (2)

⇒ mAl ban đầu = 2x = 0,2.2 = 0,4 mol
Mà: nAl phản ứng = nNaOH = x = 0,2 mol ⇒ nAl dư = 0,4 - 0,2 = 0,2 mol
⇒ mAl = 0,2.27 = 5,4 (g)
Đúng 0
Bình luận (0)
Một hỗn hợp A gồm Na2CO3 và Na2SO3 cho tác dụng với dung dịch HCl dư thu được hỗn hợp khí X có khối lượng mol trung bình là 56g/mol. Cho 0,224 lít khí X (đktc) đi qua 1 lít dung dịch Ba(OH)2. Sau thí nghiệm phải dùng 50ml dung dịch HCl 0,2M để trung hòa Ba(OH)2 dư a) Tính phần trăm số mol mỗi khí trong X và phần trăm khối lượng mỗi chất trong hỗn hợp Ab) Tính nồng độ mol/lít của dung dịch Ba(OH)2 ban đầu. Mình cần nhiều câu trả lời(lời giải...
Đọc tiếp
Một hỗn hợp A gồm Na2CO3 và Na2SO3 cho tác dụng với dung dịch HCl dư thu được hỗn hợp khí X có khối lượng mol trung bình là 56g/mol. Cho 0,224 lít khí X (đktc) đi qua 1 lít dung dịch Ba(OH)2. Sau thí nghiệm phải dùng 50ml dung dịch HCl 0,2M để trung hòa Ba(OH)2 dư
a) Tính phần trăm số mol mỗi khí trong X và phần trăm khối lượng mỗi chất trong hỗn hợp A
b) Tính nồng độ mol/lít của dung dịch Ba(OH)2 ban đầu.
Mình cần nhiều câu trả lời(lời giải) khác nhau nên các bạn giúp mình nha!!!!
a, Giả sử: \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{SO_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{0,224}{22,4}=0,01\left(1\right)\)
Mà: \(\overline{M}_A=56\Rightarrow44x+64y=56.0,01\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,004\left(mol\right)\\y=0,006\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%n_{CO_2}=\dfrac{0,004}{0,01}.100\%=40\%\\\%n_{SO_2}=60\%\end{matrix}\right.\)
BTNT C và S, có: \(\left\{{}\begin{matrix}n_{Na_2CO_3}=n_{CO_2}=0,004\left(mol\right)\\n_{Na_2SO_3}=n_{SO_2}=0,006\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na_2CO_3}=\dfrac{0,004.106}{0,004.106+0,006.126}.100\%\approx35,9\%\\\%m_{Na_2SO_3}\approx64,1\%\end{matrix}\right.\)
b, Ta có: \(n_{HCl}=0,05.0,2=0,01\left(mol\right)\)
PT: \(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
____0,005_______0,01 (mol)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
_0,004______0,004 (mol)
\(Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3+H_2O\)
_0,006_____0,006 (mol)
\(\Rightarrow n_{Ba\left(OH\right)_2}=0,015\left(mol\right)\)
\(\Rightarrow C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,015}{1}=0,015M\)
Bạn tham khảo nhé!
Đúng 4
Bình luận (4)
Hỗn hợp khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hỗn hợp X bằng một lượng oxi vừa đủ, thu được 550 ml hỗn hợp Y gồm khí và hơi nước. Nếu cho Y đi qua dung dịch axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân tử của hai hiđrocacbon là A. C2H6 và C3H8 B. C3H6 và C4H8 C. CH4 và C2H6 D. C2H4 và C3H6
Đọc tiếp
Hỗn hợp khí X gồm đimetylamin và hai hiđrocacbon đồng đẳng liên tiếp. Đốt cháy hoàn toàn 100 ml hỗn hợp X bằng một lượng oxi vừa đủ, thu được 550 ml hỗn hợp Y gồm khí và hơi nước. Nếu cho Y đi qua dung dịch axit sunfuric đặc (dư) thì còn lại 250 ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân tử của hai hiđrocacbon là
A. C2H6 và C3H8
B. C3H6 và C4H8
C. CH4 và C2H6
D. C2H4 và C3H6
















