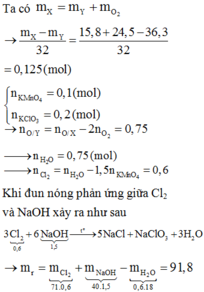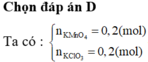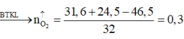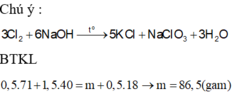Cho KMnO4 tác dụng với dung dịch HCl thu được chất khí màu vàng lục. Dẫn khí này vào dung dịch KOH đun nóng đến gần 100 C. Hãy viết pthh của các phản ứng xảy ra

Những câu hỏi liên quan
Cho 31,6 gam KMnO4 tác dụng hết với dung dịch HCl đặc, dư và đun nóng thu được một lượng khí X. Dẫn toàn bộ khí X vào 1 lít dung dịch KOH 2M trong điều kiện thích hợp để phản ứng xảy ra hoàn toàn, thu được dung dịch Y. Viết các phương trình phản ứng xảy ra và tính nồng độ mol các chất có trong dung dịch Y (giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể).
Đọc tiếp
Cho 31,6 gam KMnO4 tác dụng hết với dung dịch HCl đặc, dư và đun nóng thu được một lượng khí X. Dẫn toàn bộ khí X vào 1 lít dung dịch KOH 2M trong điều kiện thích hợp để phản ứng xảy ra hoàn toàn, thu được dung dịch Y. Viết các phương trình phản ứng xảy ra và tính nồng độ mol các chất có trong dung dịch Y (giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể).
– Số mol KMnO4 = 0,2 (mol); số mol KOH = 2 (mol)
– Phương trình phản ứng:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,2 0,5
* Ở điều kiện nhiệt độ thường:
Cl2 + 2KOH → KCl + KClO + H2O
0,5 1,0 0,5 0,5
– Dư 1,0 mol KOH
CM (KCl) = CM (KClO) = 0,5 (M); CM (KOH dư) = 1 (M)
* Ở điều kiện đun nóng trên 700C:
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
0,5 1,0 5/6 1/6
– Dư 1,0 mol KOH
CM (KCl) = 5/6 (M); CM (KClO3) = 1/6 (M); CM (KOH dư) = 1 (M).
Đúng 0
Bình luận (0)
Dẫn khí Cl 2 vào. Dung dịch KOH đun nóng tới gần 100 ° C.
Hãy viết PTHH của phản ứng xảy ra trong mỗi trường hợp. Cho biết vai trò của clo trong mỗi phản ứng oxi hoá - khử đó
3KCl + 6KOH → 5KCl + KCl O 3 + 4 H 2 O
Trong các phản ứng trên, clo vừa là chất oxi hoá, vừa là chất khử. Đó là các phản ứng tự oxi hoá, tự khử (hay còn gọi là phản ứng tự oxi hoá - khử).
Đúng 0
Bình luận (0)
Tiến hành thí nghiệm sau: – Thí nghiệm 1: cho 1,74 gam MnO2 tác dụng với HCl đặc, dư, đun nóng thu được khí A màu vàng lục. – Thí nghiệm 2: cho một lượng sắt vào dung dịch H2SO4 loãng đến khi khối lượng dung dịch tăng 167,4 gam thì thu được một lượng khí B. – Thí nghiệm 3: thêm 3 gam MnO2 vào 197 gam hỗn hợp KCl và KClO3 thu được hỗn hợp X. Trộn kĩ và đun nóng hỗn hợp X đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn nặng 152 gam và một lượng khí D. – Thí nghiệm 4: Nạp toàn bộ lượng khí...
Đọc tiếp
Tiến hành thí nghiệm sau:
– Thí nghiệm 1: cho 1,74 gam MnO2 tác dụng với HCl đặc, dư, đun nóng thu được khí A màu vàng lục.
– Thí nghiệm 2: cho một lượng sắt vào dung dịch H2SO4 loãng đến khi khối lượng dung dịch tăng 167,4 gam thì thu được một lượng khí B.
– Thí nghiệm 3: thêm 3 gam MnO2 vào 197 gam hỗn hợp KCl và KClO3 thu được hỗn hợp X. Trộn kĩ và đun nóng hỗn hợp X đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn nặng 152 gam và một lượng khí D.
– Thí nghiệm 4: Nạp toàn bộ lượng khí A, khí B và khí D thu được ở các thí nghiệm trên vào một bình kín, nâng nhiệt độ cao để thực hiện hoàn toàn các phản ứng rồi đưa nhiệt độ về 250C thu được dung dịch Y chỉ chứa một chất tan duy nhất.
Viết các phương trình hóa học xảy ra và tính nồng độ % của chất tan có trong dung dịch Y
Bài 8. a) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư KMnO4 thu được dung dịch A, V1 lít khí Cl2 (đktc). b) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư MnO2 thu được dung dịch B, V2 lít khí Cl2 (đktc). - Viết PTHH của phản ứng xảy ra. - Tính thể tích khí Cl2 thu được (V1, V2). Mọi người giúp mình với ạ mình thật sự rất cần
- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
Nung nóng hỗn hợp gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư, đun nóng, lượng khí clo sinh ra cho thụ vào 300ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z thu được m gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là: A. 12 gam B. 91,8 gam C. 111 gam D. 79,8 gam
Đọc tiếp
Nung nóng hỗn hợp gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư, đun nóng, lượng khí clo sinh ra cho thụ vào 300ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z thu được m gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 12 gam
B. 91,8 gam
C. 111 gam
D. 79,8 gam
Đáp án B
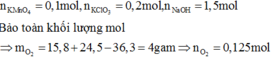
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()
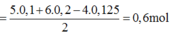

Đúng 0
Bình luận (0)
Nung nóng hỗn hợp X gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư đun nóng lượng khí clo sinh ra cho hấp thụ vào 300 ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z được chất rắn khan các phản ứng xảy ra hoàn toàn. Khối lượng chất rắn khan (gam) thu được là A. 111 B. 12 C. 79,8 D. 91,8
Đọc tiếp
Nung nóng hỗn hợp X gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư đun nóng lượng khí clo sinh ra cho hấp thụ vào 300 ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z được chất rắn khan các phản ứng xảy ra hoàn toàn. Khối lượng chất rắn khan (gam) thu được là
A. 111
B. 12
C. 79,8
D. 91,8
Nung nóng hỗn hợp gồm 31,6 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 46,5 gam hỗn hợp rắn Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư, đun nóng thu được khí clo. Hấp thụ khí sinh ra vào 300ml dung dịch NaOH 5M đung nóng thu được dug dịch Z. Cô cạn Z được m(gam) chất rắn khan. Các phản ứng xảy ra hoàn toàn. Giá trị m là: A. 79,8 g B. 91,8 g. C. 66,5 g. D. 86,5 g
Đọc tiếp
Nung nóng hỗn hợp gồm 31,6 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 46,5 gam hỗn hợp rắn Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư, đun nóng thu được khí clo. Hấp thụ khí sinh ra vào 300ml dung dịch NaOH 5M đung nóng thu được dug dịch Z. Cô cạn Z được m(gam) chất rắn khan. Các phản ứng xảy ra hoàn toàn. Giá trị m là:
A. 79,8 g
B. 91,8 g.
C. 66,5 g.
D. 86,5 g
Thực hiện các thí nghiệm sau: (a) Cho SiO2 tác dụng với axit HF. (b) Cho Si đơn chất tác dụng với dung dịch NaOH. (c) Cho dung dịch NH3 tác dụng với dung dịch AlCl3 đun nóng. (d) Dẫn khí CO2 vào dung dịch Na2SiO3. (e) Cho dung dịch HCl vào dung dịch Fe(NO3)2. Số thí nghiệm xảy ra phản ứng là A. 4 B. 3 C. 5 D. 2
Đọc tiếp
Thực hiện các thí nghiệm sau:
(a) Cho SiO2 tác dụng với axit HF.
(b) Cho Si đơn chất tác dụng với dung dịch NaOH.
(c) Cho dung dịch NH3 tác dụng với dung dịch AlCl3 đun nóng.
(d) Dẫn khí CO2 vào dung dịch Na2SiO3.
(e) Cho dung dịch HCl vào dung dịch Fe(NO3)2.
Số thí nghiệm xảy ra phản ứng là
A. 4
B. 3
C. 5
D. 2
Đáp án C
(a) SiO2 + 4HF ® SiF4 + 2H2O
(b) Si + 2NaOH + H2O ® Na2SiO3 + 2H2
(c) 3NH3 + AlCl3 + 3H2O ® Al(OH)3 + 3NH4Cl
(d) 2CO2 + Na2SiO3 + 2H2O ® H2SiO3 + 2NaHCO3
(e) 3Fe2+ + 4H+ + NO3- ® Fe3+ + NO + 2H2O
Đúng 0
Bình luận (0)
Thực hiện các thí nghiệm sau: (a) Cho SiO2 tác dụng với axit HF. (b) Cho Si đơn chất tác dụng với dung dịch NaOH. (c) Cho dung dịch NH3 tác dụng với dung dịch AlCl3 đun nóng. (d) Dẫn khí CO2 vào dung dịch Na2SiO3. (e) Cho dung dịch HCl vào dung dịch Fe(NO3)2. Số thí nghiệm xảy ra phản ứng là A. 4. B. 3. C. 5. D. 2.
Đọc tiếp
Thực hiện các thí nghiệm sau:
(a) Cho SiO2 tác dụng với axit HF.
(b) Cho Si đơn chất tác dụng với dung dịch NaOH.
(c) Cho dung dịch NH3 tác dụng với dung dịch AlCl3 đun nóng.
(d) Dẫn khí CO2 vào dung dịch Na2SiO3.
(e) Cho dung dịch HCl vào dung dịch Fe(NO3)2.
Số thí nghiệm xảy ra phản ứng là
A. 4.
B. 3.
C. 5.
D. 2.
Chọn C.
(a) SiO2 + 4HF ® SiF4 + 2H2O
(b) Si + 2NaOH + H2O ® Na2SiO3 + 2H2
(c) 3NH3 + AlCl3 + 3H2O ® Al(OH)3 + 3NH4Cl
(d) 2CO2 + Na2SiO3 + 2H2O ® H2SiO3 + 2NaHCO3
(e) 3Fe2+ + 4H+ + NO3- ® Fe3+ + NO + 2H2O
Đúng 0
Bình luận (0)