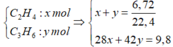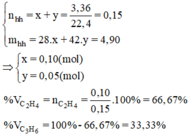1. Dẫn từ từ 5,6 lit (đktc) hỗn hợp X gồm etilen và propilen và dung dịch brom, dung dịch brom bị nhạt màu, và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tắng 8,4gam. Thành phần phần trăm theo thể tích của etilen trong X là:
2. Cho 10g hỗn hợp khí X gồm etilen và etan qua dung dịch Br2 25% có 128g dd Br2 phản ứng. % khối lượng của etan trong hỗn hợp là:
3. Hỗn hợp A gồm 2 anken đồng đẳng liên tiếp. Đốt cháy hoàn toàn V lít A thu được 15,2 lít CO2 ở đkc. Mặt khác A làm mất màu vừa hết 40g nước Br2. CTPT của 2 anken là:
4. Cho 6720 ml (đktc) anken X qua dung dịch brom dư. Sau phản ứng thấy khối lượng bình brom tăng 21 gam. Biết X có đồng phân hình học. CTCT của X là:
5. Để khử hoàn toàn 150 ml dung dịch KMnO4 0,1M tạo thành chất rắn màu đen cần V lít khí C2H4 (đktc). Giá trị tối thiểu của V là: