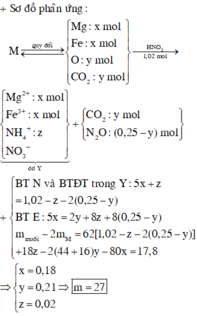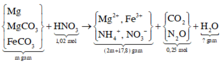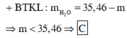Cho m gam hỗn hợp Mg và MgCO3 tác dụng với dung dịch HCl dư thu được 22,4 lít khí gồm h2 và co2 cho khí CO2 hấp thu hoàn toàn 500ml dd NaOH 2M dư sau phản ứng cô cạn dung dịch thu được 50,4 gam chất rắn khan Tính m

Những câu hỏi liên quan
Cho m gam hỗn hợp Mg, MgCO3 tác dụng với dung dịch HCl dư thu được 22,4 lít khí gồm H2 và co2 cho khí CO2 hấp thu hoàn toàn 500 ml dung dịch NaOH 2M dư sau phản ứng cô cạn dung dịch thu được 50,4 gam chất rắn khan Tính m
Cho m gam hỗn hợp Mg , MgCO3 tác dụng với dd HCL dư thu được 22,4 lít khí gồm H2 và CO2 cho khí CO2 hấp thu hoàn toàn 500 ml dd NaOH 2M dư ,sau phản ứng cô cạn dd thu được 50,4 gam chất rắn khan Tính m
\(n_{NaOH}=0,5.1\left(mol\right)\)
\(n_{hh\left(khi\right)}=1\left(mol\right)\Rightarrow n_{CO2}< 1\)
Vậy nNaOH/nCO2 < 1 vậy chất rắn khan gồm NaOH dư và Na2CO3
Gọi nCO2 = a mol
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
2a_________a ______ a _______ (mol)
\(\Rightarrow\left\{{}\begin{matrix}n_{Na2CO3}=a\left(mol\right)\\n_{NaOH\left(dư\right)}=1-2a\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{cr\left(khan\right)}=m_{NaOH}+m_{Na2CO3}=\left(1-2a\right).40+106a=50,4\)
\(\Rightarrow a=0,4\left(mol\right)\)
\(n_{H2}=n_{hh}-n_{CO2}=1-0,4=0,6\left(mol\right)\)
Ta có PTHH :
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,6 ____________________0,6 (mol)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
0,4______________________ 0,4 _____(mol)
\(\Rightarrow m=m_{Mg}+m_{MgCO3}=0,5.24+0,4.84=48\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 1,61 gam hỗn hợp X gồm Al , Mg , Fe tác dụng với 140ml HCl 1M dư sau khi phản ứng xảy ra hoàn toàn thu được dung dịch y và 1,456 lít khí H2 bay ra . Cô cạn dung dịch Y thu được m gam chất rắn . Tính m
\(n_{H_2}=\dfrac{1,456}{22,4}=0,065mol\\ BTNT\left(H\right):n_{HCl}=2n_{H_2}\\ \Leftrightarrow n_{HCl}=2.0,065=0,13mol\\ BTKL:m_{kl}+m_{HCl}=m_{muối}+m_{khí}\\ \Leftrightarrow1,61+0,13.36,5=m_{muối}+0,065.44\\ \Leftrightarrow m_{muối}=3,495g\)
Đúng 3
Bình luận (0)
Hỗn hợp X gồm RCO3 và R’CO3. Nung m gam hỗn hợp X một thời gian thu được 3,36 lít khí CO2 (đktc) và còn lại chất rắn Y. Cho Y tác dụng với dung dịch HCl dư thu được dung dịch B và V lít khí CO2. Cho V lít khí CO2 hấp thụ hoàn toàn vào dung dịch Ba(OH)2 thu được 9,85 gam gam kết tủa và dung dịch D. Đun nóng dung dịch D thu được tối đa 9,85 gam kết tủa nữa. Phần dung dịch B đem cô cạn thu được 38,15 gam muối khan. Tính m. A. 34,85 B. 31,75 C. 32,25 D. 33,15
Đọc tiếp
Hỗn hợp X gồm RCO3 và R’CO3. Nung m gam hỗn hợp X một thời gian thu được 3,36 lít khí CO2 (đktc) và còn lại chất rắn Y. Cho Y tác dụng với dung dịch HCl dư thu được dung dịch B và V lít khí CO2. Cho V lít khí CO2 hấp thụ hoàn toàn vào dung dịch Ba(OH)2 thu được 9,85 gam gam kết tủa và dung dịch D. Đun nóng dung dịch D thu được tối đa 9,85 gam kết tủa nữa. Phần dung dịch B đem cô cạn thu được 38,15 gam muối khan. Tính m.
A. 34,85
B. 31,75
C. 32,25
D. 33,15
Đáp án A
Gọi công thức TB của hai muối cacbonat là: M ¯ C O 3
M ¯ C O 3 → t 0 M O + C O 2 ( 1 )
Chất rắn Y ( M ¯ C O 3 ; M ¯ O )
n C O 2 ( 1 ) = 3 , 36 22 , 4 = 0 , 15 m o l
Y tác dụng với dung dịch HCl dư
M ¯ C O 3 + 2 H C l → t 0 M ¯ C l 2 + C O 2 + H 2 O ( 2 ) M ¯ O + H C l → t 0 M ¯ C l 2 + H 2 O ( 3 ) C O 2 + B a ( O H ) 2 → B a C O 3 + H 2 O ( 4 ) 2 C O 2 + B a ( O H ) 2 → B a ( H C O 3 ) 2 ( 5 ) B a ( H C O 3 ) 2 → t 0 B a C O 3 + C O 2 + H 2 O ( 6 ) n B a C O 3 ( 4 ) = 9 , 85 197 = 0 , 05 m o l n B a C O 3 ( 6 ) = 9 , 85 197 = 0 , 05 m o l
Theo PT (4,5,6): n C O 2 ( 3 ) = 0 , 15 m o l
Theo PT (1,2):
n M ¯ C O 3 = n C O 2 ( 2 ) + n C O 2 ( 1 ) = 0 , 15 + 0 , 15 = 0 , 3 m o l
Muối khan là: M ¯ C l 2
M ¯ C O 3 → M ¯ C l 2 M ¯ + 60 M ¯ + 71
0,3 mol muối cacbonat pư tạo 0,3 mol muối clorua tăng 3,3(g).
Khối lượng muối cacbonat ban đầu là: 38.15-3,3= 34,85(g)
Giá trị của m = 34,85(g)
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp A gồm: Al, Na, Mg tác dụng với nước dư thu được 2,24 lít khí H2. Nếu lấy 2m gam hỗn hợp A tác dụng với dung dịch NaOH dư thu được 8,96 lít khí H2. Nếu lấy 3m gam hỗn hợp A tác dụng với dung dịch HCl vừa đủ thu được 22,4 lít khí H2. Biết các thể tích khí đo ở đktc, tính m và phần trăm về khối lượng của từng kim loại trong A
Đặt x,y, z lần lượt là số mol của Na,Al,Mg trong m gam hỗn hợp A
m gam A + H2O dư
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
x--------------------x--------->0,5x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
x<------x-------------------------------------->1,5x
=> \(0,5x+1,5x=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) (1)
2m gam A + NaOH
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
2x------------------------------->x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
2y---------------------------------------------->3y
=> \(x+3y=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) (2)
3m gam A + HCl
\(Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\)
3x--------------------------->1,5x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
3y----------------------------->4,5y
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
3z----------------------------->3z
=> \(1,5x+4,5y+3z=\dfrac{22,4}{22,4}=1\left(mol\right)\) (3)
Từ (1), (2), (3) =>\(\left\{{}\begin{matrix}x=0,05\\y=\dfrac{7}{60}\\z=\dfrac{2}{15}\end{matrix}\right.\)
=> \(m_{Na}=0,05.23=1,15\left(g\right)\)
\(m_{Al}=\dfrac{7}{60}.27=3,15\left(g\right)\)
\(m_{Mg}=\dfrac{2}{15}.24=3,2\left(g\right)\)
=> \(m=1,15+3,15+3,2=7,5\left(g\right)\)
=> \(\%m_{Na}=\dfrac{1,15}{7,5}.100=15,33\%\)
\(\%m_{Al}=\dfrac{3,15}{7,5}.100=42\%\)
\(\%m_{Mg}=\dfrac{3,2}{7,5}.100=42,67\%\)
Đúng 2
Bình luận (0)
: Cho m gam hỗn hợp A gồm: Al, Na, Mg tác dụng với nước dư thu được 2,24 lít khí H2. Nếu lấy 2m gam hỗn hợp A tác dụng với dung dịch NaOH dư thu được 8,96 lít khí H2. Nếu lấy 3m gam hỗn hợp A tác dụng với dung dịch HCl vừa đủ thu được 22,4 lít khí H2. Biết các thể tích khí đo ở đktc, tính m và phần trăm về khối lượng của từng kim loại trong A
\(2Na+2H2O\rightarrow2NaOH+H2\left(1\right)\)
\(2Al+2NaOH+2H2O\rightarrow2NaAlO2+3H2\left(2\right)\)
\(2Al+6HCl\rightarrow2AlCl3+3H2\left(3\right)\)
\(2Na+2HCl\rightarrow2NaCl+H2\left(4\right)\)
\(Mg+2HCl\rightarrow MgCl2+H2\left(5\right)\)
\(n_{H2\left(1\right)}=0,1\left(mol\right)\rightarrow n_{Na}=0,2\left(mol\right)\rightarrow m_{Na}=4,6\left(g\right)\)
\(n_{H2\left(2\right)}=0,4\left(mol\right)\Rightarrow n_{Al}=\dfrac{4}{15}\left(mol\right)\Rightarrow m_{Al}=7,2\left(g\right)\)
\(\Rightarrow n_{H2\left(3\right)}=\dfrac{3}{2}n_{Al}=0,4\left(mol\right)\)
\(n_{H2\left(4\right)}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow n_{H2\left(5\right)}=1-0,4-0,1=0,5\left(mol\right)\)
\(\Rightarrow n_{Mg}=0,5\left(mol\right)\Rightarrow m_{Mg}=12\left(g\right)\)
\(\Rightarrow m=12+4,6+7,2=23,8\left(g\right)\)
\(\%m_{Na}=\dfrac{4,6}{23,8}.100\%=19,33\%\)
\(\%m_{Al}=\dfrac{7,2}{23,8}.100\%=30,25\%\)
\(\%m_{Mg}=100-19,33-30,25=50,42\%\)
Chúc bạn học tốt
Đúng 2
Bình luận (1)
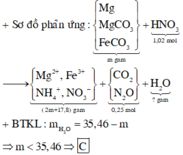
Hòa tan hết m gam hỗn hợp M chứa Mg, MgCO3 và FeCO3 trong dung dịch HCl loãng dư, thu được hỗn hợp khí X và dung dịch chứa các chất tan có cùng nồng độ mol. Mặt khác, m gam hỗn hợp trên phản ứng hoàn toàn với dung dịch chứa 1,02 mol HNO3, kết thúc phản ứng thu được dung dịch Y và 5,6 lít (đktc) hỗn hợp khí Z gồm 2 khí có tỉ khối so với H2 bằng 22. Cô cạn cẩn thận dung dịch Y thu được (2m + 17,8) gam muối khan. Giá trị m là A. 54,0 B. 40,5 C. 27,0 D. 39,15
Đọc tiếp
Hòa tan hết m gam hỗn hợp M chứa Mg, MgCO3 và FeCO3 trong dung dịch HCl loãng dư, thu được hỗn hợp khí X và dung dịch chứa các chất tan có cùng nồng độ mol. Mặt khác, m gam hỗn hợp trên phản ứng hoàn toàn với dung dịch chứa 1,02 mol HNO3, kết thúc phản ứng thu được dung dịch Y và 5,6 lít (đktc) hỗn hợp khí Z gồm 2 khí có tỉ khối so với H2 bằng 22. Cô cạn cẩn thận dung dịch Y thu được (2m + 17,8) gam muối khan. Giá trị m là
A. 54,0
B. 40,5
C. 27,0
D. 39,15
Hòa tan hết m gam hỗn hợp M chứa Mg, MgCO3 và FeCO3 trong dung dịch HCl loãng dư, thu được hỗn hợp khí X và dung dịch chứa các chất tan có cùng nồng độ mol. Mặt khác, m gam hỗn hợp trên phản ứng hoàn toàn với dung dịch chứa 1,02 mol HNO3, kết thúc phản ứng thu được dung dịch Y và 5,6 lít (đktc) hỗn hợp khí Z gồm 2 khí có tỉ khối so với H2 bằng 22. Cô cạn cẩn thận dung dịch Y thu được (2m + 17,8) gam muối khan. Giá trị m là A. 54,0. B. 40,5. C. 27,0. D. 39,15.
Đọc tiếp
Hòa tan hết m gam hỗn hợp M chứa Mg, MgCO3 và FeCO3 trong dung dịch HCl loãng dư, thu được hỗn hợp khí X và dung dịch chứa các chất tan có cùng nồng độ mol. Mặt khác, m gam hỗn hợp trên phản ứng hoàn toàn với dung dịch chứa 1,02 mol HNO3, kết thúc phản ứng thu được dung dịch Y và 5,6 lít (đktc) hỗn hợp khí Z gồm 2 khí có tỉ khối so với H2 bằng 22. Cô cạn cẩn thận dung dịch Y thu được (2m + 17,8) gam muối khan. Giá trị m là
A. 54,0.
B. 40,5.
C. 27,0.
D. 39,15.
Hòa tan hết m gam hỗn hợp M chứa Mg, MgCO3 và FeCO3 trong dung dịch HCl loãng dư, thu được hỗn hợp khí X và dung dịch chứa các chất tan có cùng nồng độ mol. Mặt khác, m gam hỗn hợp trên phản ứng hoàn toàn với dung dịch chứa 1,02 mol HNO3, kết thúc phản ứng thu được dung dịch Y và 5,6 lít (đktc) hỗn hợp khí Z gồm 2 khí có tỉ khối so với H2 bằng 22. Cô cạn cẩn thận dung dịch Y thu được (2m + 17,8) gam muối khan. Giá trị m là A. 54,0 B. 40,5. C. 27,0. D. 39,15
Đọc tiếp
Hòa tan hết m gam hỗn hợp M chứa Mg, MgCO3 và FeCO3 trong dung dịch HCl loãng dư, thu được hỗn hợp khí X và dung dịch chứa các chất tan có cùng nồng độ mol. Mặt khác, m gam hỗn hợp trên phản ứng hoàn toàn với dung dịch chứa 1,02 mol HNO3, kết thúc phản ứng thu được dung dịch Y và 5,6 lít (đktc) hỗn hợp khí Z gồm 2 khí có tỉ khối so với H2 bằng 22. Cô cạn cẩn thận dung dịch Y thu được (2m + 17,8) gam muối khan. Giá trị m là
A. 54,0
B. 40,5.
C. 27,0.
D. 39,15