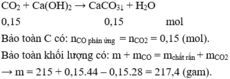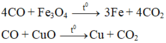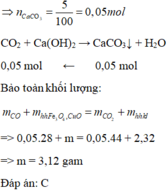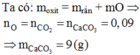Hỗn hợp A gồm MgO và Fe2O3 . Dần luồng khí CO qua 36 gam hỗn hợp A nung nóng thu được hỗn hợp B gồm 5 chất rắn và khí D thoát ra. Dẫn toàn bộ khí D qua bình đựng dung dịch nước vôi trong dư thì thu được 10 gam kết tủa. Để hòa tan hoàn toàn B thì cần một lượng vừa đủ một lượng dung dịch chứa 45,26 gam HCl, sau phản ứng có 0,448 lít khí thoát ra (đktc).
a. Viết các phương trình phản ứng xảy ra.
b. Tính thành phần % khối lượng các chất trong A.