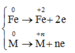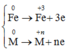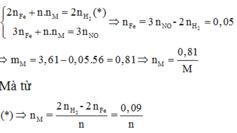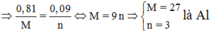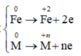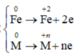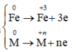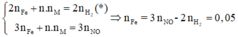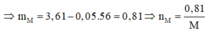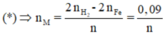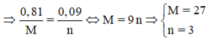Cho 7,22g hỗn hợp A gồm Fe và kim loại R có hóa trị không đổi . Chia hỗn hợp A thành 2 phần bằng nhau :-
- hòa tan hoàn toàn phần 1vào dd HCl thì thu được 2,128 lit H2(đktc)
-Đốt cháy hết phần 2 bằng khí Clo cần dùng 2,688lit khí (đktc).
Tìm R và tính % khối lượng các chất trong A.