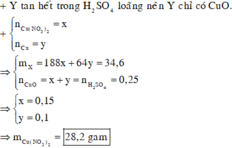ở 20độ C độ tan tronh nc của Cu(NO3)2 * 6H2O là 125g . tính khối lượng của Cu(NO3)2 * 6H2O cần lấy để pha chế 450g đ bão hòa tính khối lượng Cu(NO3)2 VÀ C % của dd đó ở 20 độ C

Những câu hỏi liên quan
ở 20độ C độ tan tronh nc của Cu(NO3)2 * 6H2O cần lấy để pha chế 450g đ bão hòa tính khối lượng Cu(NO3)2 VÀ C % của dd đó ở 20 độ C
Đề thiếu độ tan của Cu(NO3)2
Ở 20 độ C độ tan trong nc của Cu (NO3)2.6H2O là 125g. Tính khối lượng Cu (NO3)2.6H2O cần lấy để pha chế 450g dung dịch bão hòa và tính nồng độ % Cu (NO3)2 bão hòa ở nhiệt độ đó
Cứ 125g Cu(NO3)2.6H2O --> 100g nước --> 225g dung dịch
250g <-- 200g <-- 450g
=> \(m_{Cu\left(NO_3\right)_2}\) = \(\dfrac{250.188}{296}\) = 158,784(g)
=> C% = \(\dfrac{158,784}{450}.100\%\) = 35,285%
Đúng 0
Bình luận (3)
Độ tan của \(Cu\left(NO_3\right)_2.6H_2O\) là 125 g .Nghĩa là 100 g H20 hoà tan 125g muối do đó khối lượng dung dịch là 225 g
125g muối trong 225 g dung dịch
x ( g).........................450 g dung dịch
-> x = 250 g
Cứ 296 muối ngậm nước có 188 g Cu(NO3)2
Vậy 250 g...................................... y g
\(C_{\%}=\dfrac{157,78}{450}.100=35,29\%\)
Đúng 1
Bình luận (0)
Ơ 20 độ C thì cứ 125g chất tan thì có 100g nước và 225g d d
-----> Có 450g d d thì có 250g chất tan và 200g nước
Vậy là ta đã tính đc chất tan là 250g --->
C% chất tan = (250: 450).100=55,5%
Đúng 0
Bình luận (4)
Xem thêm câu trả lời
Ở 20 độ C, hòa tan m g Cu(NO3)2.6H2O vào 100g dd Cu(NO3)2 30% thu đc dung dịch bão hòa Cu(NO3)2. Tính m. Biết đọ tan của Cu(NO3)2 tại 20 độ C là 125g
Mong mn giúp :((
\(C\%_{bh}=\dfrac{125}{225}=\dfrac{\dfrac{m}{296}.188+100.0,3}{m+100}\\ m=321,132\left(g\right)\)
Đúng 1
Bình luận (1)
Điện phân 200ml một dung dịch có hoà tan Cu(NO3)2 và AgNO3 với cường độ dòng điện là 0,804A, đến khi bọt khí bắt đầu thoát ra ở cực âm thì mất thời gian là 2 giờ, khi đó khối lượng cực âm tăng 3,44g. Nồng độ mol của mỗi muối Cu(NO3)2 và AgNO3 trong dd ban đầu là A. 0,1M và 0,2M B. 0,1M và 0,1M C. 0,2M và 0,3M D. 0,1M và 0,4M
Đọc tiếp
Điện phân 200ml một dung dịch có hoà tan Cu(NO3)2 và AgNO3 với cường độ dòng điện là 0,804A, đến khi bọt khí bắt đầu thoát ra ở cực âm thì mất thời gian là 2 giờ, khi đó khối lượng cực âm tăng 3,44g. Nồng độ mol của mỗi muối Cu(NO3)2 và AgNO3 trong dd ban đầu là
A. 0,1M và 0,2M
B. 0,1M và 0,1M
C. 0,2M và 0,3M
D. 0,1M và 0,4M
Đáp án B
Khi bọt khí bắt đầu thoát ra ở catot là thời điểm Ag+ và Cu2+ đều bị điện phân hết.
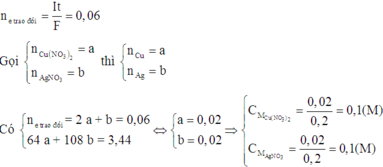
Đúng 0
Bình luận (0)
.1
Tính khối lượng BaCl2 có trong 200g dung dịch BaCl2 25%
2
Có 40g Cu(NO3)2 trong 200g dung dịch. Tính nồng độ phần trăm của dung dịch Cu(NO3)2
3
Biết SNaCl (25 0 C) = 36 gam. Hãy tính nồng độ phần trăm của dung dịch NaCl ở nhiệt độ này
1.\(m_{BaCl_2}\) = 200.25% = 50g
2.\(C\%_{Cu\left(NO_3\right)_2}\) = \(\dfrac{40}{200}.100\) = \(20\%\)
3.Ở 25\(^o\)C 100g nước hòa tan được 36 g NaCl để tạo dung dịch bão hòa
\(m_{dd}=m_{ct}+m_{dm}=36+100=136g\)
Nồng độ phần trăm của dung dịch NaCl:C% = \(\dfrac{36}{136}.100=26,47\%\)
Đúng 2
Bình luận (1)
\(1,m_{BaCl_2}=\dfrac{200.25}{100}=50\left(g\right)\\ 2,C\%_{Cu\left(NO_3\right)_2}=\dfrac{4}{200}.100\%=20\%\\ 3,C\%=\dfrac{36}{36+100}.100\%=26,47\%\)
Đúng 0
Bình luận (0)
Nung nóng 34,6 gam hỗn hợp X gồm Cu(NO3)2 và Cu trong bình kín đến khối lượng không đổi, thu được chất rắn Y. Để hòa tan hết Y cần vừa đủ 500 ml dung dịch H2SO4 loãng 0,5M. Khối lượng Cu(NO3)2 trong hỗn hợp là A. 18,8 gam. B. 23,5 gam. C. 28,2 gam. D. 14,1 gam.
Đọc tiếp
Nung nóng 34,6 gam hỗn hợp X gồm Cu(NO3)2 và Cu trong bình kín đến khối lượng không đổi, thu được chất rắn Y. Để hòa tan hết Y cần vừa đủ 500 ml dung dịch H2SO4 loãng 0,5M. Khối lượng Cu(NO3)2 trong hỗn hợp là
A. 18,8 gam.
B. 23,5 gam.
C. 28,2 gam.
D. 14,1 gam.
Cho hỗn hợp gồm Mg và Fe có khối lượng 8,64 gam được chia thành hai phần bằng nhau. Phần 1: Hòa tan hoàn toàn vào dung dịch HNO3 loãng, dư thoát ra 555ml hỗn hợp khí NO và NO2 đo ở 27,3° C và 2 atm và có tỉ khối hơi so với H2 bằng 18,8889. Phần 2: Đem hòa tan vào 400ml dung dịch chứa AgNO3 và Cu(NO3)2. Sau phản ứng thu được chất rắn gồm 3 kim loại có khối lượng 7,68g. Hòa tan chất rắn này trong dung dịch HCl dư thấy khối lượng chất rắn đã giảm đi 21,88%. Nồng độ của dung dịch AgNO3 và Cu(NO3)2 t...
Đọc tiếp
Cho hỗn hợp gồm Mg và Fe có khối lượng 8,64 gam được chia thành hai phần bằng nhau.
Phần 1: Hòa tan hoàn toàn vào dung dịch HNO3 loãng, dư thoát ra 555ml hỗn hợp khí NO và NO2 đo ở 27,3° C và 2 atm và có tỉ khối hơi so với H2 bằng 18,8889.
Phần 2: Đem hòa tan vào 400ml dung dịch chứa AgNO3 và Cu(NO3)2. Sau phản ứng thu được chất rắn gồm 3 kim loại có khối lượng 7,68g. Hòa tan chất rắn này trong dung dịch HCl dư thấy khối lượng chất rắn đã giảm đi 21,88%. Nồng độ của dung dịch AgNO3 và Cu(NO3)2 trong dung dịch lần lượt là
A.0,15M và 0,1M
B. 0,1M và 0,1M
C.0,05M và 0,15M
D. 0,125M và 0,215M
Đáp án C:
Gọi x, y là số mol Mg và Fe trong mỗi phần
=> 24x+56y = 4,32
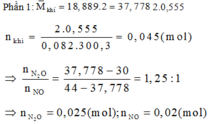

Phần 2: Gọi a, b lần lượt là số mol của AgNO3 và Cu(NO3)2
Sau phản ứng có 3 kim loại là Ag, Cu và Fe dư.
Gọi số mol Fe tham gia phản ứng là t (mol)
Bảo toàn electron ta có: nenhường= ne nhận
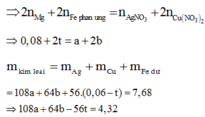
Chỉ có duy nhất Fe dư tan trong HCl
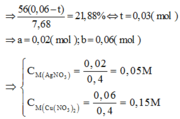
Đúng 0
Bình luận (0)
Hòa tan 32 g CuSO4 vào nước được 100ml dung dịch cuso4 bão hòa ở 60 độ c. Biết độ tan của CuSO4 ở nhiệt độ này là 40 gam.
a) Tính nồng độ mol và nồng độ phần trăm của dd CuSO4 bão hòa ở nhiệt độ trên
b)Tinh khối lượng H2O cần dùng pha vào dd trên để được dd CuSO4 10 phần trăm
GIÚP MÌNH LẸ VỚI. MÌNH ĐANG CẦN GẤP.
Giải thích các bước giải:
a Để tính nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ trên, ta dùng công thức:
Nồng độ % = (Khối lượng chất tan/Công thức phân tử chất tan) / Thể tích dung dịch x 100%
Với dung dịch CuSO4 bão hòa ở 60 độ C, ta có:
Khối lượng chất tan (CuSO4) = 40 kg = 40000 g
Thể tích dung dịch = 100 ml = 100 cm^3
Công thức phân tử CuSO4: 1 Cu + 1 S + 4 O = 63.5 + 32 + 4 x 16 = 159.5
Nồng độ % = (40000/159.5) / 100 = 25.08 %
Vậy, nồng độ % của dung dịch CuSO4 bão hòa ở nhiệt độ 60 độ C là khoảng 25.08 %.
b) Để tính khối lượng H2O cần dùng để pha vào dung dịch trên và có được dung dịch CuSO4 10%, ta dùng công thức:
Khối lượng H2O = Khối lượng chất tan ban đầu - Khối lượng chất tan sau pha / (Nồng độ sau pha - Nồng độ ban đầu)
Giả sử khối lượng chất tan sau khi pha là x g (= 10/100 x khối lượng dung dịch sau khi pha)
Vậy, ta có:
Khối lượng chất tan sau pha = 32 g + x g
Nồng độ sau pha = 10%
Nồng độ ban đầu = 25.08 %
Ứng dụng công thức, ta có:
x = (32 - 0.1 x (32 + x)) / (0.100 - 0.2508)
10000 x = 32 - 0.1 x (32 + x)
10000 x = 32 - 3.2 - 0.1x^2
0.1x^2 - 9967.2x + 3.2 = 0
Giải phương trình trên bằng phương pháp giải phương trình bậc hai ta có:
x ≈ 0.3145 hoặc x ≈ 9965.88
Với x ≈ 0.3145, ta được khối lượng H2O ≈ 32 - 0.3145 = 31.6855 g
Vậy, để có được dung dịch CuSO4 10%, ta cần dùng khoảng 31.6855 g nước.
Đúng 1
Bình luận (0)
Câu 1: Hòa tan 20g K2SO4 vào 150ml H2O đem điện phân cực trơ khi nồng độ dd là 14,925% thì dừng. V khí thoát ra ở anot trong điềi kiện 20C 1atm là bao nhiu?
Câu2: Đpdd chứa NaCl và Cu(NO3)2 đến khi hết màu xanh thì thu đc 6,72 lit hỗn hợp khí A có tỉ khối so với H2 là 29. tính m của Cu(NO3)2
1)khối lượng dd sau điện phân \(=\frac{20\cdot100}{14,925}=134\)
=>khối lượng dd giảm sau điện phân= tổng khối lượng khí thoát ra =20+150-134=36
2H−−−−−>H2+2e
____________a___2a
2O−−+4e−−>O2
_________4b_____b
Ta có các hệ phương trình
\(\begin{cases}2a+32b=36\\2a-4b=0\end{cases}\)\(\Rightarrow\)\(\begin{cases}a=2\\b=1\end{cases}\)
sử dụng CT
\(n=\frac{PV}{RT}\Rightarrow V=\frac{4688}{65}\left(l\right)\)
Đúng 0
Bình luận (1)
2)
BTklg=>mO2=mhht-mhhs
ppe:6*nKClO3+5*nKMnO4-4nO2=nCl2*2
BTng tử ng tố =>nAgCl=nCl2*2
=>mAg=mh***AgCl
ppe:nFe*3=nAg+nCl2*2
=>m=nM
Đúng 0
Bình luận (0)