Cho m gam gồm Fe, FeO, Fe2O3, Fe3O4 vào 400ml dd HCl 2M, sau phản ứng thu được 2,24 lít H2, ddY và 2,8 gam Fe không tan. Tìm m

Những câu hỏi liên quan
Câu 2 : Cho m gam gồm Fe, FeO, Fe2O3, Fe3O4 vào 400ml dd HCl 2M, sau phản ứng thu được 2,24 lít H2, ddY và 2,8 gam Fe không tan. Tìm m
Quy hỗn hợp ban đầu chỉ có Fe và O
Bảo toàn nguyên tố với clo
DD sau phản ứng chỉ có FeCl2 0,4 mol
=> m Fe ban đầu=0,4*56+2,8=25,2g
n O=1/2 n H+ =0,4
=> m=m Fe + m O=25,2+0,4*16=31,6g
Đúng 0
Bình luận (0)
Cho m gam X gồm Fe, FeO, Fe3O4, Fe2O3 vào 400 ml dung dịch HCl 2M, sau phản ứng, thu được 2,24 lít H2 (đktc), dung dịch Y và 2,8 gam Fe không tan. Giá trị m là A. 27,2. B. 30,0. C. 25,2. D. 22,4.
Đọc tiếp
Cho m gam X gồm Fe, FeO, Fe3O4, Fe2O3 vào 400 ml dung dịch HCl 2M, sau phản ứng, thu được 2,24 lít H2 (đktc), dung dịch Y và 2,8 gam Fe không tan. Giá trị m là
A. 27,2.
B. 30,0.
C. 25,2.
D. 22,4.
Cho m gam X gồm Fe, FeO, Fe3O4, Fe2O3 vào 400 ml dung dịch HCl 2M, sau phản ứng thu được 2,24 lít H2 (ở đktc), dung dịch Y, và 2,8 gam Fe không tan. Giá trị m là A. 27,2. B. 30,0. C. 25,2. D. 22,4
Đọc tiếp
Cho m gam X gồm Fe, FeO, Fe3O4, Fe2O3 vào 400 ml dung dịch HCl 2M, sau phản ứng thu được 2,24 lít H2 (ở đktc), dung dịch Y, và 2,8 gam Fe không tan. Giá trị m là
A. 27,2.
B. 30,0.
C. 25,2.
D. 22,4
Sau phản ứng còn 2,8g Fe nên dd Y chỉ chứa FeCl2
nHCl=0,8 mol
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Đáp án B
Đúng 0
Bình luận (0)
Cho m gam X gồm Fe, FeO, Fe3O4, Fe2O3 vào 400 ml dung dịch HCl 2M, sau phản ứng thu được 2,24 lít H2 (ở đktc), dung dịch Y, và 2,8 gam Fe không tan. Giá trị m là
A. 27,2
B. 30,0
C. 25,2
D. 22,4
Đáp án : B
Vì có Fe dư => trong dung dịch chỉ chứa muối FeCl2
Bảo toàn nguyên tố Cl : nFeCl2 = ½ nHCl = 0,4 mol
Lại có nH2 = nFe + HCl = 0,1 mol
Coi hỗn hợp đầu gồm có Fe và O
Dựa vào phản ứng : 2H+ + O -> H2O
=> nHCl = 2nH2 + 2nO
=> nO = ½ [0,8 – 0,1.2 ] = 0,3 mol
=> m = mFe + mO = 56.0,4 + 2,8 + 16.0,3 = 30g
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 vào 400 ml dd HCl 2M, sau phản ứng thi được 2,24l khí H2 (đktc), dd Y và 2,8g Fe khong tan. Tính m ???
\(n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\)
\(n_{H^+} = n_{HCl} = 0,8(mol)\)
Coi X gồm Fe,O
2H+ + 2e → H2
0,2...........0,2......0,1..................(mol)
2H+ + O2- → H2O
0,6..........0,3.............................(mol)
Bảo toàn electron :
\(2n_{Fe} = 2n_{H_2} + 2n_O\\ \Rightarrow n_{Fe\ pư} = \dfrac{0,3.2+0,1.2}{2} = 0,4(mol)\)
Suy ra :
mX = mFe phản ứng + mO + mFe dư = 0,4.56 + 0,3.16 + 2,8 = 30 gam
Đúng 2
Bình luận (0)
Cho m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 vào 400 ml dung dịch HCl 2M thấy thoát ra 2,24 lít khí (ở đktc) và còn lại 2,8 gam Fe (duy nhất) chưa tan. Mặt khác nếu cho m gam X trên vào dung dịch HNO3 đặc nóng dư thu được V lít NO2 ( ở đktc). Giá trị m và V lần lượt là: A. 32,6 gam và 10,08 lít. B. 24,8 gam và 4,48 lít. C. 30,0 gam và 16,8 lít. D. 14,8 gam và 20,16 lít.
Đọc tiếp
Cho m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 vào 400 ml dung dịch HCl 2M thấy thoát ra 2,24 lít khí (ở đktc) và còn lại 2,8 gam Fe (duy nhất) chưa tan. Mặt khác nếu cho m gam X trên vào dung dịch HNO3 đặc nóng dư thu được V lít NO2 ( ở đktc). Giá trị m và V lần lượt là:
A. 32,6 gam và 10,08 lít.
B. 24,8 gam và 4,48 lít.
C. 30,0 gam và 16,8 lít.
D. 14,8 gam và 20,16 lít.
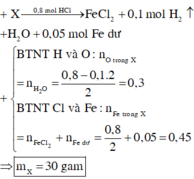
Fe dư ⇒ HCl hết. nHCl = 0,8 mol; nH2 = 0,1 mol.
Bảo toàn nguyên tố Hidro:
nH2O = (0,8 - 0,1 × 2) ÷ 2 = 0,3 mol
Bảo toàn nguyên tố Clo: nFeCl2 = 0,4 mol.
Quy X về Fe và O
⇒ ∑nFe = 0,4 + 2,8 ÷ 56 = 0,45 mol;
nO = nH2O = 0,3 mol.
⇒ m = 0,45 × 56 + 0,3 × 16 = 30(g).
Do HNO3 dư, bảo toàn electron:
3nFe = 2nO + nNO2 ⇒ nNO2 = 0,75 mol ⇒ V = 16,8 lít
Đáp án C
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 vào 400 ml dung dịch HCl 2M thấy thoát ra 2,24 lít khí (ở đktc) và còn lại 2,8 gam Fe (duy nhất) chưa tan. Mặt khác nếu cho m gam X trên vào dung dịch HNO3 đặc nóng dư thu được V lít NO2 ( ở đktc). Giá trị m và V lần lượt là: A. 32,6 gam và 10,08 lít. B. 24,8 gam và 4,48 lít. C. 30,0 gam và 16,8 lít. D. 14,8 gam và 20,16 lít.
Đọc tiếp
Cho m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 vào 400 ml dung dịch HCl 2M thấy thoát ra 2,24 lít khí (ở đktc) và còn lại 2,8 gam Fe (duy nhất) chưa tan. Mặt khác nếu cho m gam X trên vào dung dịch HNO3 đặc nóng dư thu được V lít NO2 ( ở đktc). Giá trị m và V lần lượt là:
A. 32,6 gam và 10,08 lít.
B. 24,8 gam và 4,48 lít.
C. 30,0 gam và 16,8 lít.
D. 14,8 gam và 20,16 lít.
Chọn đáp án C
Fe dư ⇒ HCl hết. nHCl = 0,8 mol; nH2 = 0,1 mol. Bảo toàn nguyên tố Hidro:
nH2O = (0,8 - 0,1 × 2) ÷ 2 = 0,3 mol || Bảo toàn nguyên tố Clo: nFeCl2 = 0,4 mol.
Quy X về Fe và O ⇒ ∑nFe = 0,4 + 2,8 ÷ 56 = 0,45 mol; nO = nH2O = 0,3 mol.
⇒ m = 0,45 × 56 + 0,3 × 16 = 30(g). Do HNO3 dư, bảo toàn electron:
3nFe = 2nO + nNO2 ⇒ nNO2 = 0,75 mol ⇒ V = 16,8 lít ⇒ chọn C.
Đúng 0
Bình luận (0)
Nung 8,4 gam Fe trong không khí, sau phản ứng thu được m gam X gồm Fe, FeO,
Fe
2
O
3
và
Fe
3
O
4
. Hoà tan m gam hỗn hợp X bằng
HNO
3
dư, thu được 2,24 lít khí
NO
2
(đktc) là sản phẩm khử duy nhất. Giá trị m là A. 11,2 gam B. 25,2 gam...
Đọc tiếp
Nung 8,4 gam Fe trong không khí, sau phản ứng thu được m gam X gồm Fe, FeO, Fe 2 O 3 và Fe 3 O 4 . Hoà tan m gam hỗn hợp X bằng HNO 3 dư, thu được 2,24 lít khí NO 2 (đktc) là sản phẩm khử duy nhất. Giá trị m là
A. 11,2 gam
B. 25,2 gam
B. 25,2 gam
D. 6,8 gam.
Hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4. Hòa tan X trong 400 ml dung dịch HCl 2M, thấy thoát ra 2,24 lít H2 (đktc) và còn lại 2,8 gam sắt chưa tan. Nếu cho toàn bộ hỗn hợp X vào dung dịch HNO3 đặc nóng (dư) thì thu được bao nhiêu lít khí NO2 (đktc)? A. 4,48 lít. B. 10,08 lít. C. 16,8 lít. D. 20,16 lít.
Đọc tiếp
Hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4. Hòa tan X trong 400 ml dung dịch HCl 2M, thấy thoát ra 2,24 lít H2 (đktc) và còn lại 2,8 gam sắt chưa tan. Nếu cho toàn bộ hỗn hợp X vào dung dịch HNO3 đặc nóng (dư) thì thu được bao nhiêu lít khí NO2 (đktc)?
A. 4,48 lít.
B. 10,08 lít.
C. 16,8 lít.
D. 20,16 lít.