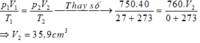một bình kim loại có chứa chất khí ở 27 độ C và áp suất 760 mmHg. khi áp suất tăng gấp đôi thì nhiệt độ của lượng khí

Những câu hỏi liên quan
Trong phòng thí nghiệm người ta điều chế được 40
cm
3
khí hiđrô ở áp suất 750 mmHg và nhiệt độ 27
°
C
. Thể tích của lượng khí trên ở điều kiện tiêu chuẩn (áp suất 760 mmHg và nhiệt độ 0
°
C
) bằng A. 23
cm
3
. B. 32,5
cm
3...
Đọc tiếp
Trong phòng thí nghiệm người ta điều chế được 40 cm 3 khí hiđrô ở áp suất 750 mmHg và nhiệt độ 27 ° C . Thể tích của lượng khí trên ở điều kiện tiêu chuẩn (áp suất 760 mmHg và nhiệt độ 0 ° C ) bằng
A. 23 cm 3 .
B. 32,5 cm 3
C. 35,9 cm 3
D. 25,9 cm 3
Trong phòng thí nghiệm, người ta điều chế được
40
c
m
3
khí hidro ở áp suất 750 mmHg và nhiệt độ
27
°
C
. Thể tích của lượng khí trên ở điều kiện chuẩn (áp suất 760 mmHg và nhiệt độ
0
°
C
) có giá trị gần nhất với giá trị nào sau đây? A.
36
c
m
3
B.
400
c...
Đọc tiếp
Trong phòng thí nghiệm, người ta điều chế được 40 c m 3 khí hidro ở áp suất 750 mmHg và nhiệt độ 27 ° C . Thể tích của lượng khí trên ở điều kiện chuẩn (áp suất 760 mmHg và nhiệt độ 0 ° C ) có giá trị gần nhất với giá trị nào sau đây?
A. 36 c m 3
B. 400 c m 3
C. 43 c m 3
D. 2 c m 3
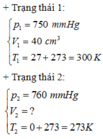
+ Áp dụng phương trình trạng thái của khí lí tưởng ta có:
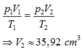
=> Chọn A.
Đúng 0
Bình luận (0)
Tính khối lượng riêng của không khí ở đỉnh núi Phăng-xi-păng cao 3 140 m. Biết rằng mỗi khi lên cao thêm 10m thì áp suất khí quyển giảm 1 mmHg và nhiệt độ trên đỉnh núi là 2o C. Khối lượng riêng của không khí ở điều kiện tiêu chuẩn (áp suất 760 mmHg và nhiệt độ 0o C) là 1,29 kg/m3. - Trạng thái 1 (chuẩn) Po 760 mmHg To 0 + 273 273 K Vo ? - Trạng thái 2 (ở đỉnh núi) P (760 – 314) mmHg T 275 K V ?
Đọc tiếp
Tính khối lượng riêng của không khí ở đỉnh núi Phăng-xi-păng cao 3 140 m. Biết rằng mỗi khi lên cao thêm 10m thì áp suất khí quyển giảm 1 mmHg và nhiệt độ trên đỉnh núi là 2o C. Khối lượng riêng của không khí ở điều kiện tiêu chuẩn (áp suất 760 mmHg và nhiệt độ 0o C) là 1,29 kg/m3.
- Trạng thái 1 (chuẩn)
Po = 760 mmHg
To = 0 + 273 = 273 K
Vo = ?
- Trạng thái 2 (ở đỉnh núi)
P = (760 – 314) mmHg
T = 275 K
V = ?
Khi lên cao thêm 10m thì áp suất khí quyển giảm 1 mmHg. Do đó lên cao 3140m, áp suất không khí giảm: 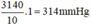
→ Áp suất không khí ở trên đỉnh núi Phăng-xi-păng: p1 = 760 – 314 = 446 mmHg
Khối lượng riêng của không khí:
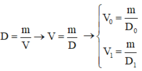
Áp dụng phương trình trạng thái ta được:
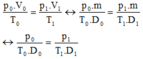
Khối lượng riêng của không khí ở đỉnh núi Phăng-xi-păng cao 3 140 m:
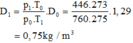
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm, người ta điều chế được 40 cm3 khí hidro ở áp suất 750 mmHg và nhiệt độ 27oC. Tính thể tích của lượng khí trên ở điều kiện chuẩn (áp suất 760 mmHg và nhiệt độ 0oC)
Bài giải.
+ Trạng thái 1:
p1 = 750 mmHg
T1 = 300 K
V1 = 40 cm3
+ Trạng thái 2 :
P0 = 760 mmHg
T0 = 273 K
V0 = ?
+ Phương trình trạng thái :
\(\dfrac{p_0V_0}{T_0}=\dfrac{p_1V_1}{T_1}\Rightarrow V_0=\dfrac{p_1V_1}{T_1}.\dfrac{T_0}{p_0}\)
\(V_0=\dfrac{750.40.273}{760.300}=36cm^3\)
Đúng 0
Bình luận (0)
trong phòng thí nghiệm , người ta điều chế được 40 cm3 khí hidro ở áp suất 750 mmHg và nhiệt độ 27oC . Tính thể tích của lượng khí trên ở điều kiện chuẩn (áp suất 760 mmHg và nhiệt độ 0oC ).
Áp dụng pt trạng thái: (P1.V1):T1= (P2.V2):T2
<=> (750x40):300= (760.V2):273
Giải pt tìm được V2
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm, người ta điều chế được 40 cm3 khí hidro ở áp suất 750 mmHg và nhiệt độ 27o C. Tính thể tích của lượng khí trên ở điều kiện chuẩn (áp suất 760 mmHg và nhiệt độ 0o C)
Trạng thái 1:
P1 = 750 mmHg
T1 = 27 + 273 = 300 K
V1 = 40 cm3
Trạng thái 2:
Po = 760 mmHg
To = 0 + 273 = 273 K
Vo = ?
Áp dụng phương trình trạng thái của khí lí tưởng:
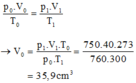
Đúng 0
Bình luận (0)
Một bình chứa một lượng khí ở nhiệt độ 30o C và áp suất 2 bar. (1 bar = 105 Pa). Hỏi phải tăng nhiệt độ lên tới bao nhiêu độ để áp suất tăng gấp đôi?
Trạng thái 1: T1 = t1 + 273 = 303 K; P1 = 2 bar
Trạng thái 2: P2 = 4 bar ; T2 = ?
Áp dụng định luật Sác-lơ cho quá trình biến đổi đẳng tích, ta có:
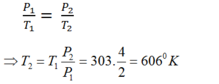
Đúng 1
Bình luận (0)
Một bình thép chứa khí ở nhiệt độ 27 ° C và áp suất 40atm. Nếu tăng áp suất thêm 10atm thì nhiệt độ của khí trong binh là:
A. 102 ° C
B. 375 ° C
C. 34 ° C
D. 402 ° C
Đáp án: A
Vì thể tích của bóng đèn không đổi nên ta có:
p 1 T 1 = p 2 T 2 → T 2 = P 2 P 1 T 1 = 40 + 10 40 . ( 27 + 273 ) = 375 − 273 = 102 0 C
Đúng 0
Bình luận (0)
trong phòng thí nghiệm , điều chế được 40 cm3 khí hidro ở áp suất 750 mmHg và ở nhiệt độ 27oC . Thể tích của lượng khí trên ở áp suất 760 mmHg và ở nhiệt độ 0oC gần bằng bao nhiêu ?
+ Trạng thái 1:
p1 = 750 mmHg
T1 = 300 K
V1 = 40 cm3
+ Trạng thái 2 :
P0 = 760 mmHg
T0 = 273 K
V0 = ?
+ Phương trình trạng thái :
=
=> V0 =
.
V0= = 36 cm3
Đúng 0
Bình luận (0)