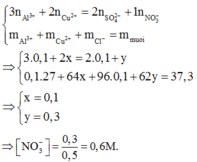Cho 300 ml dung dịch NH3 1M vào 200 ml dung dịch HCI 1M. Tinh CM của các ion NH4+, Cl- và muối NH4Cl trong dung dịch thu được

Những câu hỏi liên quan
Trộn 200 mL dung dịch BaCl2 1M với 100 mL dung dịch KCl 2M thu được dung dịch X. Nồng độ mol/L của ion Cl- trong X là
`n_{BaCl_2}=200.10^{-3}.1=0,2(mol)`
`n_{KCl}=100.10^{-3}.2=0,2(mol)`
`->n_{Cl^-}=2n_{BaCl_2}+n_{KCl}=0,6(mol)`
`->[Cl^-]={0,6}/{(200+100).10^{-3}}=2M`
Đúng 3
Bình luận (0)
cho 200 ml dung dịch AgNO3 1M vào 300 ml dung dịch HCL 1M. a) tính CM của dung dịch thu được sau phản ứng. b) trung hòa dung dịch sau phản ứng cần dùng bao nhiêu gam dung dịch KOH 5,6% và hiệu suất phản ứng là 85%
Dung dịch X chứa các ion sau: Al3+, Cu2+, SO42- và NO3-. Để kết tủa hết ion SO42- có trong 250 ml dung dịch X cần 50 ml dung dịch BaCl2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NH3 dư thì thu được 7,8 gam kết tủa Làm bay hơi hết nước có trong 500 ml dung dịch X được 37,3 gam hỗn hợp muối khan. Nồng độ mol của NO3- trong dung dịch X là A. 0,3M. B. 0,6M C. 0,2M D. 0,4M
Đọc tiếp
Dung dịch X chứa các ion sau: Al3+, Cu2+, SO42- và NO3-. Để kết tủa hết ion SO42- có trong 250 ml dung dịch X cần 50 ml dung dịch BaCl2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NH3 dư thì thu được 7,8 gam kết tủa Làm bay hơi hết nước có trong 500 ml dung dịch X được 37,3 gam hỗn hợp muối khan. Nồng độ mol của NO3- trong dung dịch X là
A. 0,3M.
B. 0,6M
C. 0,2M
D. 0,4M
Dung dịch X chứa các ion sau: Al3+, Cu2+,
S
O
4
2
-
và
N
O
3
-
. Để kết tủa hết ion có trong 250 ml dung dịch X cần 50 ml dung dịch BaC2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NH3 dư thì được 7,8 gam kết tủa. Cô cạn 500 ml dung dịch X được 37,3 gam hỗn hợp muối khan. Nồng độ mol/l của
N
O...
Đọc tiếp
Dung dịch X chứa các ion sau: Al3+, Cu2+, S O 4 2 - và N O 3 - . Để kết tủa hết ion có trong 250 ml dung dịch X cần 50 ml dung dịch BaC2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NH3 dư thì được 7,8 gam kết tủa. Cô cạn 500 ml dung dịch X được 37,3 gam hỗn hợp muối khan. Nồng độ mol/l của N O 3 - là:
A. 0,2M.
B. 0,3M.
C. 0,6M.
D. 0,4M.
Cho 200 ml dung dịch X có chứa các ion NH4+, K+, SO42- và Cl- với các nồng độ sau: [NH4+] 0,5M; [K+] 0,1M; [SO42-] 0,25M. Khối lượng của chất rắn thu được sau khi cô cạn 200 ml dung dịch X là: A. 8,09 gam B. 7,38 gam C. 12,18 gam D. 36,9 gam
Đọc tiếp
Cho 200 ml dung dịch X có chứa các ion NH4+, K+, SO42- và Cl- với các nồng độ sau: [NH4+] = 0,5M; [K+]= 0,1M; [SO42-]= 0,25M. Khối lượng của chất rắn thu được sau khi cô cạn 200 ml dung dịch X là:
A. 8,09 gam
B. 7,38 gam
C. 12,18 gam
D. 36,9 gam
Đáp án A
Áp dụng ĐLBT ĐT: Tổng số mol điện tích dương bằng tổng số mol điện tích âm ta có: 0,1.1+ 0,02.1=0,05.2+ nCl-
Suy ra nCl-= 0,02 mol
Khối lượng chất rắn thu được khi cô cạn dung dịch là:
0,1.18+ 0,02.39+ 96.0,05+ 0,02.35,5= 8,09 gam
Đúng 0
Bình luận (0)
Trong 200 ml dung dịch A có chứa 0,2 mol ion Na+; 0,6 mol NH4+; 0,4 mol H+; 0,2mol Cl-; 0,5 mol SO42-. Dung dịch B chứa hh 2 hiđroxit KOH 1M và Ba(OH)2 2M .Cho 300ml dung dịch B vào dung dịch A , đun nnh. Tính khối lượng giảm sau phản ứng .
Đọc tiếp
Trong 200 ml dung dịch A có chứa 0,2 mol ion Na+; 0,6 mol NH4+; 0,4 mol H+; 0,2mol Cl-; 0,5 mol SO42-. Dung dịch B chứa hh 2 hiđroxit KOH 1M và Ba(OH)2 2M .Cho 300ml dung dịch B vào dung dịch A , đun nnh. Tính khối lượng giảm sau phản ứng .
Cho 300 ml dung dịch
Ba
OH
2
1M vào 200 ml dung dịch
NaHCO
3
2,5M, thu được dung dịch X và kết tủa Y. Cho từ từ dung dịch HCl 1M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V là A. 300 B. 150 C. 200 D. 250
Đọc tiếp
Cho 300 ml dung dịch Ba OH 2 1M vào 200 ml dung dịch NaHCO 3 2,5M, thu được dung dịch X và kết tủa Y. Cho từ từ dung dịch HCl 1M vào X đến khi bắt đầu có khí sinh ra thì hết V ml. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V là
A. 300
B. 150
C. 200
D. 250
Đổ từ từ 200ml dung dịch A (Na2CO3 1M và K2CO3) vào 200 ml dung dịch (Na+ 1M, Ba2+ 1M, Ca2+ 1M, Cl- 2,5 M và HCO3-) thu được m gam kết tủa và dung dịch B. Đổ thêm 100 ml dung dịch A vào B, sau phản ứng thấy nồng độ CO32- trong dung dịch bằng ¼ nồng độ của HCO3-. Hãy tìm nồng độ của K2CO3 trong A. A. 0,75 M B. 1,125M C. 2,625M D. 2,5M
Đọc tiếp
Đổ từ từ 200ml dung dịch A (Na2CO3 1M và K2CO3) vào 200 ml dung dịch (Na+ 1M, Ba2+ 1M, Ca2+ 1M, Cl- 2,5 M và HCO3-) thu được m gam kết tủa và dung dịch B. Đổ thêm 100 ml dung dịch A vào B, sau phản ứng thấy nồng độ CO32- trong dung dịch bằng ¼ nồng độ của HCO3-. Hãy tìm nồng độ của K2CO3 trong A.
A. 0,75 M
B. 1,125M
C. 2,625M
D. 2,5M
Đáp án A
Bảo toàn điện tích : CHCO3 trong 200 ml dung dịch là 2,5M
Xét tổng thể : đổ 300 ml dung dịch A và 200 ml dung dịch
Sau khi trộn :
=> nHCO3 = 2,5.0,2 = 0,5 mol => nCO32- = 0,125 mol
Gọi nồng độ K2CO3 trong A là x => nCO3 tổng = 0,3.(1 + x)
Sau trộn sẽ phản ứng với Ca2+ , Ba2+ => còn lại : 0,3(1 + x) – 0,2 – 0,2 = 0,125
=> x = 0,75M
Đúng 0
Bình luận (0)
Dung dịch X chứa các ion sau: Al3+, Cu2+, SO42- và NO3-. Để kết tủa hết ion SO42- có trong 250 ml dung dịch X cần 50 ml dung dịch BaCl2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NH3 dư thì được 7,8 gam kết tủa. Làm bay hơi hết nước có trong 500 ml dung dịch X được 37,3 gam hỗn hợp muối khan. Nồng độ mol của NO3- trong dung dịch X là A. 0,3M B. 0,6M C. 0,2M D. 0,4M
Đọc tiếp
Dung dịch X chứa các ion sau: Al3+, Cu2+, SO42- và NO3-. Để kết tủa hết ion SO42- có trong 250 ml dung dịch X cần 50 ml dung dịch BaCl2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NH3 dư thì được 7,8 gam kết tủa. Làm bay hơi hết nước có trong 500 ml dung dịch X được 37,3 gam hỗn hợp muối khan. Nồng độ mol của NO3- trong dung dịch X là
A. 0,3M
B. 0,6M
C. 0,2M
D. 0,4M
Đáp án : B
250 ml X phản ứng với 50 ml BaCl2
=> 500 ml X phản ứng với 100 ml BaCl2 => nSO4 = nBa2+ = 0,1 mol
X phản ứng với NH3 => tạo kết tủa Al(OH)3 ( Cu(OH)2 tan trong NH3)
=> nAl3+ = nAl(OH)3 = 0,1 mol
Trong X : Bảo toàn điện tích : 3nAl3+ + 2nCu2+ = nNO3- + 2nSO42-
Laij cos : mmuối X = 27.nAl3+ + 64nCu2+ + 62nNO3 + 96nSO4 = 37,3g
=> nNO3- = 0,3 mol
=> CM(NO3-) = 0,6M
Đúng 0
Bình luận (0)