Đốt cháy hoàn toàn 6,72 lít hỗn hợp X (đktc) gồm 2 hidrocacbon A và B thì thu được 8,98 lít CO2 và 9 g H2O
a , Xác định công thức phân tử của A , B
b,Tính thành phần phần trăm theo thể tích của các chất trong hỗn hợp A
Đốt cháy hoàn toàn hh X gồm 2 hidrocacbon A (CnH2n-2) và B (CmH2m) thu được 15,68 lít CO2 ở đktc và 14,4 gam H2O. Biết X chiếm thể tích là 6,72 lít ở đktc. Xác định tp % thể tích của hỗn hợp X, xác định CTPT của A,B
Đốt cháy hoàn toàn 8,7 gam hỗn hợp X gồm 2 Ankin đồng đẳng kế tiếp nhau, thu được 14,56 lít khí CO2 (đktc) a) Xác định công thức phân tử của 2 Ankin b) Tính phần trăm theo thể tích mỗi Ankin trong hỗn hợp.
Đốt cháy hoàn toàn 6,72 lít hỗn hợp khí X gồm một hiđrocacbon CxHy và các bon oxit thì cần dùng vừa đủ 13,44 lít khí O2 thu được 22 g CO2 và 72 g hơi nước tìm công thức phân tử của cxhy và phần trăm theo thể tích của mỗi khí trong hỗn hợp X
\(\left\{{}\begin{matrix}C_xH_y:a\left(mol\right)\\CO:b\left(mol\right)\end{matrix}\right.=>a+b=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CO_2}=\dfrac{22}{44}=0,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Bảo toàn C: ax + b = 0,5
Bảo toàn H: ay = 0,8
Bảo toàn O: b + 0,6.2 = 0,5.2 + 0,4
=> b = 0,2 (mol)
=> a = 0,1 (mol)
=> x = 3 ; y = 8 => CTPT: C3H8
\(\left\{{}\begin{matrix}\%V_{C_3H_8}=\dfrac{0,1}{0,3}.100\%=33,33\%\\\%V_{CO}=\dfrac{0,2}{0,3}.100\%=66,67\%\end{matrix}\right.\)
Cho hốn hợp 2 hidrocacbon A,B với MB-MA=24 và DB/A=1.8.Đốt cháy hoàn toàn V(lít) hỗn hợp trên thu được 11.2(lít) CO2 (ĐKTC) và 8.1(g) H2O
a, xác định công thức phân tử của A ,B
b,Tính V(các khí đo ở đktc)
ai giải giúp e vs
Mb - Ma = 24 và Mb = 1,8Ma. Thu được Ma = 30 và Mb = 54
A là C2H6 và B là C4H6
Gọi x,y tương ứng là số mol A và B.
2x + 4y = 0,5 và 3x + 3y = 0,45
x = 0,05; y = 0,1
Va = 0,05.22,4 = 0,112 lít; Vb = 2,24 lít.
Hỗn hợp khí A chứa một ankan và một anken, Khối lượng hỗn hợp A là 9 gam và thể tích là 8,96 lít. Đốt cháy hoàn toàn A, thu được 13,44 lít C O 2 . Các thể tích được đo ở đktc.
Xác định công thức phân tử và phần trăm thể tích từng chất trong A.
Khối lượng trung bình của 1 mol A :
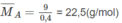
Trong hỗn hợp A phải có chất có M < 22,5 ; chất đó chỉ có thể là C H 4 .
Sau đó giải hệ 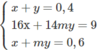
Ta tìm được m = 3; x = 0,3; y = 0,1.
HH khí A gồm CO và một hidro cacbon. Để đốt cháy hoàn toàn 6,72 lít khí A, phải dùng vừa hết 39,2 lít không khí. Phản ứng tạo thành 8,96 lít CO2 và 1,8 g H2O.
Xác định công thức phân tử của hidro cacbon và thành phần % theo thể tích các khí trong hh A. Biết oxi chiếm 20% thể tích không khí, các khí đều đo ở đktc
Gọi số mol CO, CxHy trong A là a, b
=> \(a+b=\dfrac{6,72}{22,4}=0,3\)
\(n_{O_2}=\dfrac{39,2}{22,4}.20\%=0,35\left(mol\right)\)
\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
Bảo toàn C: a + bx = 0,4
Bảo toàn H: by = 0,2
Bảo toàn O: a + 0,7 = 0,8 + 0,1 => a = 0,2 (mol) => b = 0,1 (mol)
=> bx = 0,2 (mol)
\(\left\{{}\begin{matrix}x=\dfrac{0,2}{b}=\dfrac{0,2}{0,1}=2\\y=\dfrac{0,2}{b}=\dfrac{0,2}{0,1}=2\end{matrix}\right.\)
=> CTPT: C2H2
\(\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,2}{0,3}.100\%=66,67\%\\\%V_{C_2H_2}=\dfrac{0,1}{0,3}.100\%=33,33\%\end{matrix}\right.\)
Hỗn hợp M ở thể lỏng, chứa hai hợp chất hữu cơ kế tiếp nhau trong một dãy đồng đẳng. Nếu làm bay hơi 2,58 g M thì thể tích hơi thu được đúng bằng thể tích của 1,40 g khí N 2 ở cùng điều kiện.
Đốt cháy hoàn toàn 6,45 g M thì thu được 7,65 g H 2 O và 6,72 lít C O 2 (đktc).
Xác định công thức phân tử và phần trăm khối lượng của từng chất trong hỗn hợp M.
Số mol 2 chất trong 2,58 g M: 
Số mol 2 chất trong 6,45 g M: 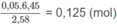
Khi đốt hỗn hợp M, thu được C O 2 và H 2 O ; vậy các chất trong hỗn hợp phải chứa C và H, có thể có O. Hai chất lại kế tiếp nhau trong một dãy đồng đẳng (nghĩa là hom nhau 1 nhóm CH2) nên công thức phân tử hai chất đó là C x H y O z và C x + 1 H y + 2 O z (x, y nguyên và > 0; z nguyên và > 0).
Giả sử trong 6,45 g M có a moi C x H y O z và b mol C x + 1 H y + 2 O z :
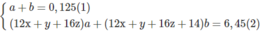
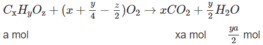
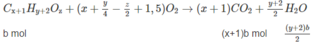
Số mol C O 2 :
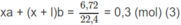
Số mol H 2 O :
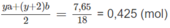
⇒ ya + (y + 2)b = 0,85 (4)
Giải hệ phương trình :
Biến đổi (3) ta có x(a + b) + b = 0,300
b = 0,300-0,125x
0 < b < 0,125 ⇒ 0 < 0,300 - 0,125x < 0,125
1,40 < x < 2,40
⇒ x = 2; b = 0,300 - 0,125.2 = 0,05.
⇒ a = 0,125 - 0,05 = 0,075.
Thay giá trị của a và b vào (4) ta có :
0,0750y + 0,0500(y + 2) = 0,85
⇒ y = 6.
Thay giá trị của a, b, x, y vào (2) ta tìm được z = 1.
Thành phần hỗn hợp M :
Khối lượng
C
2
H
6
O
chiếm 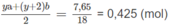
Khối lượng
C
3
H
g
O
chiếm 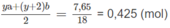
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm hiđrocacbon A và hợp chất hữu cơ B có công thức CxHyOz ( x ≥ 2 ), cần dùng vừa đủ 14,56 lít O2 (đktc), thu được 8,96 lít CO2 (đktc) và 9,9 gam H2O. Xác định công thức phân tử của A và B
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).
a. Xác định thành phần % về thể tích các khí trong hỗn hợp?
b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)
Một hỗn hợp X gồm ankan A và anken B được chia thành 2 phần
- Phần 1: có thể tích là 11,2 lít, đem trộn với 6,72 lít H2 (có xúc tác Ni) đến khi phản ứng hoàn toàn rồi đưa về nhiệt độ ban đầu thì thấy hỗn hợp khí sau phản ứng có thể tích giảm 25% so với ban đầu
- Phần 2: nặng 8 gam, đem đốt cháy hoàn toàn thu được 24,2 gam CO2. Công thức phân tử của A và B là
A. C4H10 và C3H6
B. C3H8 và C2H4
C. C2H6 và C3H6
D. CH4 và C4H8