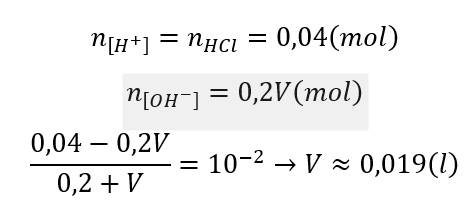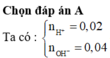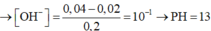ính pH của dung dịch sau HNO3 0,05M; KOH 0,2M; H2SO4 0,1M.

Những câu hỏi liên quan
Trộn 100 ml dung dịch gồm H2SO4 0,05M vào HCl 0,1M với 100 ml dung dịch gồm NaOH 0,2M và Ba(OH)2 0,1M. Tìm pH của dung dịch thu được sau phản ứng là:
A. 12,8
B. 13
C. 1
D. 1,2
Đáp án B
nH+ = 0,1 .2.0,05 + 0,1.0,1 =0,02
nOH- = 0,1.0,2 + 0,1.0,1.2 = 0,04
⇒ Trong dung dịch sau phản ứng có nOH- dư = 0,04 – 0,02 = 0,02 mol
V dd thu = 100 + 100 = 200ml
⇒ [OH-] = 0,1 ⇒ pH = 13
Đáp án B.
Đúng 1
Bình luận (0)
Cho dung dịch A chứa H2SO4 0,1M; HNO3 0,2M và HCl 0,3M. Trộn 300 ml dung dịch A với V lít dung dịch B gồm NaOH 0,2M và KOH 0,29M thu được dung dịch C có pH = 2. Giá trị của V là
A. 0,134
B. 0,424
C. 0,441
D. 0,414
Đáp án : D
Trong A :
n H + = 2 n H 2 S O 4 + n H N O 3 + n H C l = 0,21 mol
Trong B :
n O H - = nNaOH + nKOH = 0,49V mol
Để C có pH = 2 (axit) => H+ dư
=> nH+(C) = 10-pH .(0,3 + V) = 0,21 – 0,49V
=> V = 0,414 lit
Đúng 0
Bình luận (0)
Tính pH của các dung dịch
HNO3 0.04 M
NaOH 10^-3 M
100ml H2SO4 0,01 M + 100ml HCl 0,05M
100ml KOH 0,1M + 100ml HCL 0,05M
Trộn 100ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Tính pH của dung dịch X? A. 8 B. 14 C. 12 D. 13
Đọc tiếp
Trộn 100ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Tính pH của dung dịch X?
A. 8
B. 14
C. 12
D. 13
Đáp án C
nH+ = 0,02 mol; nOH-= 0,04 mol
H+ + OH- → H2O
0,02 0,04
nOH- dư = 0,02 mol; [OH-] dư = 0,02/0,2 = 0,1M suy ra [H+] = 10-13 M suy ra pH = 13
Đúng 0
Bình luận (0)
trộn 200ml dung dịch HCl 0,2M với V lít dung dịch Y gồm KOH 0,1M và Ba(OH)2 0,05M . Dung dịch có pH=2 . Tính V?
Trộn ba dung dịch: HCl 0,2M;
H
2
SO
4
0,1M và
HNO
3
0,08M với thể tích bằng nhau thu được dung dịch X. Cho 150 ml X tác dụng với 150 ml dung dịch hỗn hợp NaOH 0,1M và KOH 0,058M thu được dung dịch Y có pH x. Giá trị của x là A. 4 B. 1 C. 2 D. 3
Đọc tiếp
Trộn ba dung dịch: HCl 0,2M; H 2 SO 4 0,1M và HNO 3 0,08M với thể tích bằng nhau thu được dung dịch X. Cho 150 ml X tác dụng với 150 ml dung dịch hỗn hợp NaOH 0,1M và KOH 0,058M thu được dung dịch Y có pH = x. Giá trị của x là
A. 4
B. 1
C. 2
D. 3
Chọn D
Trộn 3 dung dịch với thể tích bằng nhau thu được 150 ml dung dịch X → mỗi dung dịch lấy 50ml.
→ n H + = 0,05.0,2 + 0,05.2.0,1 + 0,05.0,08 = 0,024 mol.
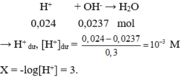
Đúng 0
Bình luận (0)
Trộn 200ml dung dịch axit H2SO4 0,05M với 100ml dung dịch KOH 0,2M. Viết phương trình phân tử và ion rút gọn của phản ứng và tính pH của dung dịch sau phản ứng .
\(2KOH+H_2SO_4->K_2SO_4+2H_2O\)
\(OH^-+H^+->H_2O\)
\(n_{H_2SO_4}=0,05.0,2=0,01\left(mol\right);n_{KOH}=0,2.0,1=0,02\left(mol\right)\)
PTHH: \(2KOH+H_2SO_4->K_2SO_4+2H_2O\)
_____0,02------->0,01
=> KOH, H2SO4 phản ứng vừa đủ, tạo ra dd K2SO4
=> pH = 7
Đúng 3
Bình luận (0)
Trộn 3 dung dịch H2SO4 0,1M; HNO3 0,2M; HCl 0,3M với những thể tích bằng nhau thu được dung dịch A. Lấy 300ml dung dịch A cho phản ứng với V lít dung dịch B gồm NaOH 0,2M và KOH 0,29M thu được dung dịch C có pH 2. Giá trị V là A.0,214 lít B. 0,424 lít C. 0,134 lít D. 0,414 lít
Đọc tiếp
Trộn 3 dung dịch H2SO4 0,1M; HNO3 0,2M; HCl 0,3M với những thể tích bằng nhau thu được dung dịch A. Lấy 300ml dung dịch A cho phản ứng với V lít dung dịch B gồm NaOH 0,2M và KOH 0,29M thu được dung dịch C có pH= 2. Giá trị V là
A.0,214 lít
B. 0,424 lít
C. 0,134 lít
D. 0,414 lít
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là: A. 13,0 B. 1,2 C. 1,0 D. 12,8
Đọc tiếp
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch X có pH là:
A. 13,0
B. 1,2
C. 1,0
D. 12,8
Đáp án A
nH+ = 0,02 mol; nOH-= 0,04 mol
H+ + OH- → H2O
0,02 0,04
nOH- dư = 0,02 mol; [OH-] dư = 0,02/0,2 = 0,1M suy ra [H+] = 10-13 M suy ra pH = 13
Đúng 0
Bình luận (0)