đốt cháy hoàn toàn 5,04g hidrocacbon A.Sản phẩm sau phản ứng cho qua bình 1 đựng CaCl2 khan và bình 2 đựng KOH dư thấy khổi lượng bình 1 tăng 6,48g và bình 2 tăng 15,84g .Biết 1 lít khí hơi A ở đktc có khối lượng là 3,57g . Tìm CTHH của A

Những câu hỏi liên quan
Đốt cháy 8,52 hợp chất hữu cơ X, cho sản phẩm đi qua các bình đựng CaCl2 khan và KOH dư. Thấy bình CaCl2 tăng thêm 9,72 gam còn bình đựng KOH tăng thêm 21,12 gam. Mặt khác nếu đốt cháy 1,42 gam chất X thì thu được 0,224 lít khí N2 (ở đktc). Biết rằng hợp chất X chỉ chứa một nguyên tử nito. Xác định CTPT của hợp chất X
Ta có: \(n_{H_2O}=\dfrac{9,72}{18}=0,54\left(mol\right)\Rightarrow n_H=0,54.2=1,08\left(mol\right)\)
\(n_{CO_2}=\dfrac{21,12}{44}=0,48\left(mol\right)=n_C\)
\(n_{N_2}=\dfrac{0,224}{22,4}=0,01\left(mol\right)\Rightarrow n_{N\left(1,42\left(g\right)X\right)}=0,01.2=0,02\left(mol\right)\)
\(\Rightarrow n_{N\left(8,52\left(g\right)X\right)}=0,02.\dfrac{8,52}{1,42}=0,12\left(mol\right)\)
⇒ mC + mH + mN = 0,48.12 + 1,08.1 + 0,12.14 = 8,52 (g) = mX
→ X chứa C, H và N.
Gọi CTPT của X là CxHyNt.
⇒ x:y:t = 0,48:1,08:0,12 = 4:9:1
Mà: X chỉ chứa 1 nguyên tử N.
→ CTPT của X là C4H9N.
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn a gam hỗn hợp các hidrocacbon trong oxi dư, sau phản ứng dẫn hỗn hợp sản phẩm qua lần lượt bình 1 đựng CuSO4 khan dư; bình 2 đựng dung dịch NaOH dư. Biết khối lượng bình 1 và bình 2 tăng lên lần lượt 6,3 gam và 17,6 gam. Xác định giá trị của a
Ta có: \(n_{H_2O}=\dfrac{6,3}{18}=0,35\left(mol\right)\Rightarrow n_H=0,35.2=0,7\left(mol\right)\)
\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
⇒ a = mC + mH = 0,4.12 + 0,7.1 = 5,5 (g)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 3,075 g hỗn hợp 2 ancol no, đơn chức và cho sản phẩm lần lượt đi qua bình 1 đựng H2SO4 đặc và bình 2 đựng KOH rắn. Tính khối lượng các bình tăng lên biết rằng nếu cho lượng rượu trên tác dụng với Na dư thấy bay ra 0,672 lít khí H2 ở đktc. A. Bình 1 tăng 3,645 g; bình 2 tăng 6,27 g B. Bình 1 tăng 6,27 g; bình 2 tăng 3,645 g C. Bình 1 tăng 3,645 g: bình 2 tăng 5,27 g D. Bình 1 tăng 3,645 g; bình 2 tăng 7,27 g
Đọc tiếp
Đốt cháy hoàn toàn 3,075 g hỗn hợp 2 ancol no, đơn chức và cho sản phẩm lần lượt đi qua bình 1 đựng H2SO4 đặc và bình 2 đựng KOH rắn. Tính khối lượng các bình tăng lên biết rằng nếu cho lượng rượu trên tác dụng với Na dư thấy bay ra 0,672 lít khí H2 ở đktc.
A. Bình 1 tăng 3,645 g; bình 2 tăng 6,27 g
B. Bình 1 tăng 6,27 g; bình 2 tăng 3,645 g
C. Bình 1 tăng 3,645 g: bình 2 tăng 5,27 g
D. Bình 1 tăng 3,645 g; bình 2 tăng 7,27 g
Đốt cháy 3g HCHC X ,dẫn toàn bộ sản phẩm cháy qua bình 1 đựng H2SO4 đặc, bình 2 đựng dung dịch KOH dư, thấy bình 1 tăng thêm 1,8g, bình 2 tăng thêm 3,52g và còn lại 448 ml khí N2 ở đktc. Tỉ khối hơi của X đối với không khí là 2,586. Tìm CTPT của X.
\(m_{b1\uparrow}=m_{H_2O}=1,8\left(g\right)\Rightarrow n_{H_2O}=0,1\left(mol\right)\)
=> \(n_H=0,2\left(mol\right)\)
\(m_{b2\uparrow}=m_{CO_2}=3,52\left(g\right)\Rightarrow n_{CO_2}=0,08\left(mol\right)\)
=> \(n_C=0,08\left(mol\right)\)
\(n_{N_2}=0,02\left(mol\right)\Rightarrow n_N=0,04\left(mol\right)\)
Ta có : \(m_O=3-\left(0,08.12+0,2+0,04.14\right)=1,28\left(g\right)\)
=> \(n_O=0,08\left(mol\right)\)
\(M_X=2,586.29=75\)
Đặt CT của X là CxHyOzNt (x,y,z,t >0)
Ta có : \(x:y:z:t=0,08:0,2:0,08:0,04=2:5:2:1\)
=> CTĐGN : \(\left(C_2H_5O_2N\right)_n\)
Ta có : 75n=75
=> n=1
Vậy CTPT của X là C2H5O2N
Đúng 2
Bình luận (1)
Đốt cháy hết 6,72 lít hỗn hợp khí (đktc) X gồm 2 amin đơn chức, bậc một A và B là đồng đẳng kế tiếp. Cho hỗn hợp khí và hơi sau khi đốt cháy lần lượt qua bình 1 đựng
H
2
S
O
4
đặc, bình 2 đựng KOH dư, thấy khối lượng bình 2 tăng 21,12 gam. Tên gọi của 2 amin là: A. metylamin và etylamin. B. etylamin và n-propylamin. C. n-propylamin và n-butylamin. D. iso-propylamin và iso-butylamin.
Đọc tiếp
Đốt cháy hết 6,72 lít hỗn hợp khí (đktc) X gồm 2 amin đơn chức, bậc một A và B là đồng đẳng kế tiếp. Cho hỗn hợp khí và hơi sau khi đốt cháy lần lượt qua bình 1 đựng H 2 S O 4 đặc, bình 2 đựng KOH dư, thấy khối lượng bình 2 tăng 21,12 gam. Tên gọi của 2 amin là:
A. metylamin và etylamin.
B. etylamin và n-propylamin.
C. n-propylamin và n-butylamin.
D. iso-propylamin và iso-butylamin.
Khối lượng bình 2 tăng 21 , 12 g a m → m C O 2 = 21 , 12 g a m → n C O 2 = 0 , 48 m o l
namin = 0,3 mol
→ C ¯ = n C O 2 n a m i n = 0 , 48 0 , 3 = 1 , 6
Vậy 2 amin là C H 3 N H 2 v à C 2 H 5 N H 2
Đáp án cần chọn là: A
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 1 hidrocacbon A ( là chất khí, đkc) rồi dẫn sản phẩm lần lượt qua bình 1 đựng H2SO4 đặc và bình 2 chứa NaOH dư người ta thấy khối lượng bình I tăng 1,8g và khối lượng bình 2 tăng 3,52 gam. XĐ CTPT của A. A. C4H10 B. C3H8 C. C5H12 D. C6H14
Đọc tiếp
Đốt cháy hoàn toàn 1 hidrocacbon A ( là chất khí, đkc) rồi dẫn sản phẩm lần lượt qua bình 1 đựng H2SO4 đặc và bình 2 chứa NaOH dư người ta thấy khối lượng bình I tăng 1,8g và khối lượng bình 2 tăng 3,52 gam. XĐ CTPT của A.
A. C4H10
B. C3H8
C. C5H12
D. C6H14
Đáp án A
Khối lượng bình 1 tăng là khối lượng của H2O => nH2O = 1,8/18 = 0,1 mol
Khối lượng bình 2 tăng là khối lượng của CO2 => nCO2 = 3,52/44 = 0,08 mol
Nhận thấy: nCO2 < nH2O => hidrocacbon là ankan;
Số mol ankan là nankan = 0,1 – 0,08 = 0,02 mol
Phương trình phản ứng:
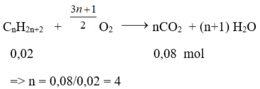
CTPT của A là C4H10
Đúng 0
Bình luận (0)
Hỗn hợp khí A gồm 1 ankan và 1 Ankadien . Đốt cháy hoàn toàn 0,3 mol A cần dùng 28 lít O2( đktc) . Dẫn sản phẩm cháy lần lượt qua bình (1) đựng H2SO4 đặc dư và bình (2) đựng dd NaOH dư thấy khối lượng bình (2) tăng thêm 35,2g. Xác định phần trăm thể tích Ankadien trong A?
Xem chi tiết
34. Hỗn hợp khí A gồm 1 ankan và 1 Ankadien . Đốt cháy hoàn toàn 0,3mol A cần dùng 28 lít O2(đktc) . Dẫn sản phẩm cháy lần lượt qua bình (1) đựng H2SO4 đặc dư và bình(2) đựng dd NaOH dư thấy khối lượng bình(2) tăng thêm 35,2g. Xác định % thể tích Ankadien trong A
Xem chi tiết
Khối lượng bình 2 tăng = mCO2 = 35,2 gam
=> nCO2 = \(\dfrac{35,2}{44}\) = 0,8 mol , nO2 = \(\dfrac{28}{22,4}\) = 1,25 mol
A + O2 → CO2 + H2O
Áp dụng định luật BTNT O => 2nO2 = 2nCO2 + nH2O
=> nH2O = 1,25.2 - 0,8.2 = 0,9 mol
Ankan có CTPT CnH2n+2: x mol
Ankađien có CTPT CmH2m-2 : y mol
CnH2n+2 + O2 → nCO2 + (n+1)H2O
x x.n x.(n+1)
CmH2m-2 + O2 → mCO2 + (m-1)H2O
y y.m y(m-1)
Ta có nH2O - nCO2 = y(m-1) + x.(n+1) - x.n - y.m = x - y = 0,1 (1)
Mà x + y = 0,3 (2)
Từ (1), (2) => x = 0,2 và y = 0,1
%V Ankađien = \(\dfrac{0,1}{0,3}.100\%\)= 33,34%
Đúng 0
Bình luận (0)
Đốt cháy 0,282 gam hợp chất hữu cơ X, cho sản phẩm đi qua các bình đựng CaCl2 khan và KOH dư. Thấy bình đựng CaCl2 tăng thêm 0,194 gam còn bình đựng KOH tăng thêm 0,8 gam. Mặt khác nếu đốt cháy 0,186 gam chất X thì thu được 22,4 ml khí N2 (ở đktc). Biết rằng hợp chất X chỉ chứa một nguyên tử nitơ. Công thức phân tử của hợp chất X là: A. C6H6N2 B. C6H7N C. C6H9N D. C5H7N
Đọc tiếp
Đốt cháy 0,282 gam hợp chất hữu cơ X, cho sản phẩm đi qua các bình đựng CaCl2 khan và KOH dư. Thấy bình đựng CaCl2 tăng thêm 0,194 gam còn bình đựng KOH tăng thêm 0,8 gam. Mặt khác nếu đốt cháy 0,186 gam chất X thì thu được 22,4 ml khí N2 (ở đktc). Biết rằng hợp chất X chỉ chứa một nguyên tử nitơ. Công thức phân tử của hợp chất X là:
A. C6H6N2
B. C6H7N
C. C6H9N
D. C5H7N
Đáp án : B
Từ dữ kiện đề bài ta tính được %H = 7,64% ; %C = 77.37%; %N = 15.05%
=> Công thức phân tử C6H7N
Đúng 0
Bình luận (0)










