Nung x gam H2 BaCO3,CaCO2 đến khi phản ứng xảy ra hoàn toàn thu được 36,2g chất rắn ,khối lượng x gồm số với ban đầu là 13,2g
a,viết phương thức hóa học
b,tính x
giúp mình với mình cần gấp
Nung x gam H2 BaCO3,CaCO2 đến khi phản ứng xảy ra hoàn toàn thu được 36,2g chất rắn ,khối lượng x gồm số với ban đầu là 13,2g
a,viết phương thức hóa học
b,tính x =
giúp mình với mình cần gấp
Nung x gam \(H_2,BaCO_3,CaCO_3\) đến khi phản ứng xảy ra hoàn toàn thu được 36,2g chất rắn ,khối lượng x gồm số với ban đầu là 13,2g
a,viết phương thức hóa học
b,tính x
ý bạn là đề vậy phải ko
Bạn có thể ghi đề lại ko vậy đọc mình ko hiểu
Giúp mình nhé mấy bạn mình cần gấp nhak
Cho dòng khí H2 dư đi qua 3,54 gam hỗn hợp gồm Fe,FeO,Fe2O3 được đốt nóng sau khi phản ứng xong còn lại 2,94 gam Fe nếu cho 3,54 gam hỗn hợp ban đầu trên tác dụng với dung dịch CuSO4 cho đến khi phản ứng xảy ra hoàn toàn lọc lấy chất rắn sau khi làm khô chất rắn cân nặng 3,72 gam tính khối lượng của mỗi chất trong hỗn hợp ban đầu
FeO + CO -> Fe + CO2
mol: x -> x
pt2: Fe2O3 + CO ->2 Fe + CO2
mol: y -> 2y
theo gt thu được 2.94 g
Fe trong đó có Fe tạo thành và Fe ban đầu và gọi Z là số mol Fe ban đầu
=> ta có Pt : 72x + 160y +56z=3.54 (1)
và x + 2y + z =3.92/56=0.0525 (2)
hh trên vào CuSO4 thì chỉ có Fe phản ứng
pt: Fe + CuSO4 -> FeSO4 + Cu
mol: z -> z
thu được 3.72g rắn gồm Cu , FeO, Fe2O3
=> ta có pt: 72x + 160y + 64Z=3.72 (3)
từ (1),(2),(3) ta có x=0.015= nFeO , y=0.0075 mol =nFe2O3 , z=0.0225 mol=nFe
Có số mol áp dụng công thức m=n*M em tự tính khối lượng các chất nha
Số ko đẹp lắm nên số mol hơi dài,cứ giữ nguyên để tính để tránh sai số
CHÚC EM HỌC TỐT !!!!!!(nhớ hậu tạ nha hi hi.....)
Ở nhiệt độ phòng, hỗn hợp khí X gồm hiđrocacbon A và lượng dư hiđro có tỉ khối so với H2 là 3,375. Khi cho X qua Ni đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y có tỉ khối so với H2 là 4,5.
a) Xác định công thức phân tử của A.
b) Tính thành phần phần trăm theo thể tích của các chất có trong X.
Nếu cho X qua Pd/BaSO4 đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z. Trong Z chỉ có hai chất khí là B và hiđro.
c) Viết phương trình phản ứng tạo thành B trên. Tính tỉ khối của Z so với hiđro.
d) B có thể cho phản ứng polime hóa. Viết phương trình phản ứng này.
Hợp chất B cho phản ứng với Cl2 ở 500 tạo thành C (có chứa 46,4% khối lượng Cl). C phản ứng với dung dịch NaOH loãng thu được D. Cho D phản ứng với nước và Cl2 thu được E (có chứa 32,1% khối lượng Cl). Sau cùng E phản ứng với dung dịch NaOH loãng thu được F.
e) Viết công thức cấu tạo của các chất từ B đến F và viết các phương trình hóa học xảy ra
a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
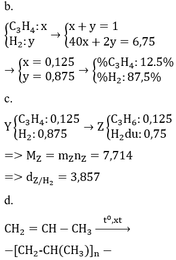

Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được chất rắn. Mặt khác, khi cho hỗn hợp X vào dung dịch CuCl2, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được muối khan. Biết các phản ứng hóa học xảy ra hoàn toàn.
Hãy viết các phương trình phản ứng xảy ra.
M + 2HCl → MCl2 + H2↑
MO + 2HCl → MCl2 + H2O
MCl2 + 2NaOH → M(OH)2↓ + 2NaCl
M(OH)2 → MO + H2O
M + CuCl2 → MCl2 + Cu↓
Thủy phân hoàn toàn m gam hỗn hợp hai este đơn chức mạch hở A, B ( M A < M B ) trong 700 ml dung dịch KOH 1M thu được dung dịch X và hỗn hợp Y gồm 2 ancol là đồng đẳng liên tiếp. Thực hiện tách nước Y trong H2SO4 đặc lượng của các ete là 8,04 gam (Hiệu suất ete hóa của các ancol đều là 60%). Cô cạn dung dịch X được 54,4 gam chất rắn. Nung chất rắn này với CaO cho đến khi phản ứng xảy ra hoàn toàn, thu được 6,72 lít hỗn hợp khí T (đktc). Thêm NaOH vào chất rắn nung tiếp thấy có thêm khí thoát ra. Phần trăm khối lượng của A trong hỗn hợp ban đầu là:
A. 66,89%
B. 48,96%
C. 49,68%
D. 68,94%
Chọn đáp án D.
Có n K O H = 0 , 7 m o l n T = 6 , 72 22 , 4 = 0 , 3 m o l
Thêm NaOH vào chất rắn nung tiếp thấy có thêm khí thoát ra
⇒ Chứng tỏ muối RCOOK chưa phản ứng hết khi nung chất rắn.
⇒ n e s t e = n K O H − n T = 0 , 7 − 0 , 3 = 0 , 4 m o l ⇒ n Y = 0 , 4 m o l
Số mol H2O tạo thành trong phản ứng tạo ete = 60 % . 1 2 .0 , 4 = 0 , 12 m o l
⇒ M ¯ e t e = 8 , 04 0 , 12 = 67 ⇒ 2 ancol là C2H5OH và CH3OH
⇒ n C 2 H 5 O H + n C H 3 O H = 0 , 4 m o l 46 n C 2 H 5 O H + 32 n C H 3 O H 0 , 4 = 8 , 04 + 18.0 , 12 0 , 24 ⇒ n C 2 H 5 O H = 0 , 3 n C H 3 O H = 0 , 1
m c h a t r a n = m R C O O K + m K O H d u = R + 83 .0 , 4 + 56.0 , 3 = 54 , 4 g
⇒ R = 11 ⇒ Có 1 gốc axit là H, gốc axit còn lại kí hiệu là
Trường hợp 1: H C O O K : 0 , 1 m o l R ' C O O K : 0 , 3 m o l ⇒ R ' = 37 , 6 − 84.0 , 3 0 , 1 − 83 = 41
⇒ Loại.
Trường hợp 2: H C O O K : 0 , 3 m o l R ' C O O K : 0 , 1 m o l ⇒ R ' = 37 , 6 − 84.0 , 3 0 , 1 − 83 = 41
⇒ R ' là C3H5-, A là HCOOC2H5, B là C3H5COOCH3
% m A = 74.0 , 3 74.0 , 3 + 100.0 , 1 .100 % = 68 , 94 %
Cho 11g hỗn hợp Al, Fe tác dụng với một lượng dư dung dịch axit Clohidric. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít H2 (đktc). Dẫn toàn bộ lượng khí H2 này đi chậm qua ống sứ đựng 32g CuO nung nóng. Sau một thời gian, thấy trong ống sứ còn lại 26,88g chất rắn và chỉ có 80% H2 đã phản ứng.
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)
Nung nóng hoàn toàn 6,06 gam hỗn hợp Cu(OH)2 và Fe(OH)3 thu được 4,8 gam chất rắn.
a. Viết phương trình hóa học của phản ứng xảy ra? Vì sao khối lượng chất rắn giảm?
b. Tính % theo khối lượng mỗi chất trong hỗn hợp đầu
a)
$Cu(OH)_2 \xrightarrow{t^o} CuO + H_2O$
$2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
Vì theo bảo toàn khối lượng :
$m_{hh} = m_{oxit} + m_{H_2O}$
mà $m_{H_2O} > 0$ nên $m_{hh} > m_{oxit}$
Do đó khối lượng rắn giảm.
b)
Gọi $n_{Cu(OH)_2} = a ; n_{Fe(OH)_3} = b$
$\Rightarrow 98a + 107b = 6,06(1)$
Theo PTHH :
$m_{cr} = 80a + 80b = 4,8(2)$
Từ (1)(2) suy ra a = 0,04; b = 0,02
Suy ra :
$\%m_{Cu(OH)_2} = \dfrac{0,04.98}{6,06}.100\% = 64,67\%$
$\%m_{Fe(OH)_3} = 35,33\%$
\(n_{Cu\left(OH\right)_2}=a\left(mol\right),n_{Fe\left(OH\right)_3}=b\left(mol\right)\)
\(m_{hh}=98a+107b=6.06\left(g\right)\left(1\right)\)
\(Cu\left(OH\right)_2\underrightarrow{^{^{t^0}}}CuO+H_2O\)
\(a............a\)
\(2Fe\left(OH\right)_3\underrightarrow{^{^{t^0}}}Fe_2O_3+3H_2O\)
\(b............0.5b\)
\(m_{Cr}=80a+0.5b\cdot160=4.8\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.04,b=0.02\)
\(\%Cu\left(OH\right)_2=\dfrac{0.04\cdot98}{6.06}\cdot100\%=64.68\%\)
\(\%Fe\left(OH\right)_3=35.32\%\)
Nung nóng hoàn toàn 6,06 gam hỗn hợp Cu(OH)2 và Fe(OH)3 thu được 4,8 gam chất rắn.
a. Viết phương trình hóa học của phản ứng xảy ra? Vì sao khối lượng chất rắn giảm?
b. Tính % theo khối lượng mỗi chất trong hỗn hợp đầu
Câu 7. Hòa tan 10 gam NaOH vào 160(g) CuSO4 20%. Sau khi phản ứng xẩy ra hoàn toàn, lọc lấy kết tủa rồi nung đến khối lượng không đổi.
1. Viết phương trình hóa học xảy ra.
2. Tính khối lượng chất rắn thu được sau khi nung.
3. Tính nồng độ % các chất tan trong nước lọc
\(1,PTHH:2NaOH+CuSO_4\to Na_2SO_4+Cu(OH)_2\downarrow\\ 2,n_{NaOH}=\dfrac{10}{40}=0,25(mol)\\ m_{CuSO_4}=\dfrac{160.20\%}{100\%}=32(g)\\ \Rightarrow n_{CuSO_4}=\dfrac{32}{160}=0,2(mol)\)
Vì \(\dfrac{n_{NaOH}}{2}<\dfrac{n_{CuSO_4}}{1}\) nên \(CuSO_4\) dư
\(\Rightarrow n_{Cu(OH)_2}=0,125(mol)\\ \Rightarrow m_{Cu(OH)_2}=0,125.98=12,25(g)\\ 3,n_{Na_2SO_4}=0,125(mol)\\ \Rightarrow m_{CT_{Na_2SO_4}}=0,125.142=17,75(g)\\ m_{dd_{Na_2SO_4}}=10+160-12,25=157,75(g)\\ \Rightarrow C{\%}_{Na_2SO_4}=\dfrac{17,75}{157,75}.100\% \approx 11,25\%\)