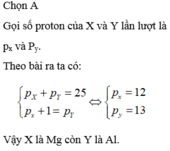Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì có tổng số proton trong hai hạt nhân nguyên tử là 25.Viết cấu hình e và xác định vị trí X và Y trong BTH

Những câu hỏi liên quan
Hai nguyên tố x và y đứng kế tiếp nhau trong cùng một chu kì của bảng hệ thống tuần hoàn và có tổng số điện tích hạt nhân bằng 25. a xác định số hiệu của x y b viết cấu hình electron nguyên tử X,Y Cho biết vị trí X,Y trong bảng hệ thống tuần hoàn
Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kỳ của BTH các nguyên tố có tổng số điện tích hạt nhân là 25 . Xác định số hiệu của A,B . Viết cấu hình electron nguyên tử của A,B và cho biết vị trí của A,B trong BTH . So sánh tính chất hóa học của chúng
Xem chi tiết
\(\left\{{}\begin{matrix}P_A+P_B=25\\P_B-P_A=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P_A=12\\P_B=13\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z_A=P_A=12\\Z_B=P_B=13\end{matrix}\right.\)
=> A là magie (ZMg=12); B là nhôm (ZAl=13)
Cấu hình e của magie: 1s22s22p63s2
=> Chu kì 3, nhóm IIA, ô 12.
Cấu hình e của nhôm: 1s22s22p63s23p1
=> Chu kì 3, nhóm IIIA, ô 13
=> Magie có tính khử, tính kim loại mạnh hơn nhôm.
Nhôm có tính oxi hoá và tính kim loại mạnh hơn magie.
Đúng 1
Bình luận (0)
Câu 1. Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì có tổng số proton trong hai hạt nhân nguyên tử là 25. X và Y thuộc chu kì và các nhóm nào?
Giả sử X đứng trước Y
Ta có : \(\left\{{}\begin{matrix}P_X+P_Y=25\\P_X+1=P_Y\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}P_X=12\left(Mg\right)\\P_Y=13\left(Al\right)\end{matrix}\right.\)
=> X và Y thuộc chu kì 3
X thuộc nhóm IIA và Y thuộc nhóm IIIA
Đúng 1
Bình luận (0)
Gọi số hạt proton của một nguyên tử nguyên tố là a
Suy ra số hạt proton của nguyên tử nguyên tố còn lại là a + 1
Ta có : $a + a + 1 = 25 \Rightarrow a = 12$
Vậy X là Magie, Y là Nhôm
Do đó, X thuộc nhóm IIA, Y thuộc nhóm IIIA
Đúng 1
Bình luận (0)
Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì và có tổng số proton trong hai hạt nhân là 25, trong đó X có số proton nhở hơn Y. Hai nguyên tố X và Y lần lượt là
A. Mg và Al.
B. Al và Mg.
C. F và Cl.
D. Cl và F.
X và Y là hai nguyên tố thuộc hai chu kì liên tiếp nhau và cùng thuộc một nhóm A, trong đó X có điện tích hạt nhân nhỏ hơn Y. Tổng số proton trong hạt nhân nguyên tử của X và Y là 22. Xác định hai nguyên tố X, Y A. P và C B. O và S C. N và P D. F và Cl
Đọc tiếp
X và Y là hai nguyên tố thuộc hai chu kì liên tiếp nhau và cùng thuộc một nhóm A, trong đó X có điện tích hạt nhân nhỏ hơn Y. Tổng số proton trong hạt nhân nguyên tử của X và Y là 22. Xác định hai nguyên tố X, Y
A. P và C
B. O và S
C. N và P
D. F và Cl
Đáp án C
Theo đề bài, ta có: ZX + ZY = 22 (1)
- Nếu X, Y thuộc hai chu kì nhỏ thì (ZX < ZY): ZY = ZX + 8 (2)
Từ (1) và (2) => ZX =7; ZY = 15.
Vậy X là N, Y là P
- Nếu X thuộc chu kì nhỏ và Y thuộc chu kì lớn thì: ZY = ZX + 18 (3)
Từ (1) và (3) => ZX = 2; ZY = 20 (loại vì không thảo mãn đề bài)
- Nếu X, Y thuộc hai chu kì lớn: ZY = ZX + 32 (4)
Từ (1) và (4) => ZX <0 (loại)
Đúng 0
Bình luận (0)
A và B là hai nguyên tố đứng kế tiếp nhau ở một chu kì trong hệ thống tuần hoàn. Tổng số proton của chúng là 25. Xác định số hiệu nguyên tử và viết cấu hình electron của A, B
$12 <$ Số proton trung bình là $25 : 2 = 12,5 < 13$
Vậy hai nguyên tố A và B là $Mg$ và $Al$
Cấu hình e của Mg : $1s^22s^22p^63s^2$
Cấu hình e của Al : $1s^22s^22p^63s^23p^1$
Đúng 0
Bình luận (0)
X và Y là hai nguyền tố thuộc hai chu kì liên tiếp nhau và cùng thuộc một nhóm A, trong đó X có điện tích hạt nhân nhỏ hơn Y. Tổng số proton trong hạt nhân nguyên tử của X và Y là 22. Xác định hai nguyên tố X, Y.
A. P và C.
B. O và S.
C. N và P.
D. F và Cl.
Hai nguyên tố X và Y thuộc 2 nhóm chính kế tiếp nhau trong cùng 1 chu kì có tổng số proton là 27.
Viết CHe và xác định vị trí của chúng trong HTTH
Số hạt proton trung bình $ = \dfrac{27}{2} = 13,5$
Vậy hai nguyên tố cần tìm là :
Aluminium - Ô 13, nhóm IIIA, chu kì 3
Silicon - Ô 14, nhóm IVA, chu kì 3
Đúng 0
Bình luận (0)
Hai nguyên tố X,Y đứng kế tiếp nhau trong một chu kì thuộc bảng tuần hoàn có tổng điện tích dương trong hạt nhân là 25. Vị trí của X và Y trong bảng tuần hoàn là (biết
Z
x
Z
y
) A. X chu kì 3, nhóm IIA, Y chu kì 2, nhóm IIIA. B. X chu kì 3, nhóm IIA, Y chu kì 3, nhóm IIIA. C. X chu kì 2, nhóm IIIA, Y chu kì 3 nhóm IIIA. D. tất cả đều sai.
Đọc tiếp
Hai nguyên tố X,Y đứng kế tiếp nhau trong một chu kì thuộc bảng tuần hoàn có tổng điện tích dương trong hạt nhân là 25. Vị trí của X và Y trong bảng tuần hoàn là (biết Z x < Z y )
A. X chu kì 3, nhóm IIA, Y chu kì 2, nhóm IIIA.
B. X chu kì 3, nhóm IIA, Y chu kì 3, nhóm IIIA.
C. X chu kì 2, nhóm IIIA, Y chu kì 3 nhóm IIIA.
D. tất cả đều sai.