cho a gam Zn vào dd H2SO4 dư,thu được V ml khí H2(đktc).Dẫn toàn bộ khí này đi qua ống đựng bột CuO nung nóng,thu được 14,4gam Cu.Tìm giá trị của a,V
giúp mk với sắp thi rồi ae ơi
Dẫn V lít khí NH3 đi qua ống sứ đựng lượng dư bột CuO (m gam) nung nóng thu được (m-4,8) gam chất rắn X và V’ lít khí Y (đktc). Giá trị của V’ là:
A. 4,48
B. 2,24
C. 1,12
D. 3,36
Đáp án B
2NH3+ 3CuO → t o N2+ 3Cu + 3H2O (1)
2x 3x x 3x 3x mol
Theo ĐL bảo toàn khối lượng:
mNH3+ mCuO= mchất rắn X+ mN2+ mH2O
→17.2x+m=m-4,8+ 28x+18.3x
→ x= 0,1 mol→V’= VN2= 22,4.x= 2,24 lít
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hơp khí X, Cho toàn bộ khí X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 10
B. 8
C. 12
D. 5
Cho bột kẽm dư vào 200ml dd Hcl 1M ta thu được khí H2 bay lên a. Tính thể tích khí sinh ra (đktc) b. dẫn toàn bộ khí hidro bay ra ống đựng CuO dư nung nóng thu được Cu. Tính khối lượng Cu em cần gấp ạ=(((
\(a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{HCl}=1\cdot0,2=0,2\left(mol\right)\\ \Rightarrow n_{H_2}=\dfrac{1}{2}n_{HCl}=0,1\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=0,1\cdot22,4=2,24\left(l\right)\\ b,PTHH:CuO+H_2\rightarrow^{t^o}Cu+H_2O\\ \Rightarrow n_{Cu}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow m_{Cu}=0,1\cdot64=6,4\left(g\right)\)
`a)`
PTHH : `Zn + 2HCl -> ZnCl_2 + H_2`
`200ml = 0,2l`
`n_{HCl} = 0,2 . 1 = 0,2` `mol`
`n_{H_2} = 1/2 . n_{HCl} = 0,1` `mol`
`V_{H_2} = 0,1 . 22,4 = 2,24` `l`
`b)`
`CuO + H_2 -> Cu + H_2O`
Ta có : `n_{H_2} = 0,1` `mol`
`-> n_{Cu} = n_{H_2} = 0,1` `mol`
`-> m_{Cu} = 0,1 . 64 = 6,4` `gam`
Bài 5.Cho 6,5 g Zn tác dụng vừa đủ với dd axit H2SO4 thu được V l khí H2 dktc. Dẫn toàn bộ lượng khí H2 này qua bột CuO nung nóng cho đến khi hết khí H2.Tính khối lượng Cu tạo thành.
Ta có: \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH:
Zn + H2SO4 ---> ZnSO4 + H2 (1)
H2 + CuO ---to---> Cu + H2O (2)
Theo PT(1): \(n_{H_2}=n_{Zn}=0,1\left(mol\right)\)
Theo PT(2): \(n_{Cu}=n_{H_2}=0,1\left(mol\right)\)
=> \(m_{Cu}=0,1.64=6,4\left(g\right)\)
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 10
B. 5
C. 12
D. 8
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 8.
B. 12.
C. 10.
D. 5.
Dẫn khí CO dư qua ống sứ đựng 8 gam bột CuO nung nóng, thu được hỗn hợp khí X. Cho toàn bộ X vào nước vôi trong dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 8.
B. 5.
C. 12.
D. 10
Cho 0,448 lít khí NH3 (đktc) đi qua ống sứ đựng 16 gam CuO nung nóng, sau khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Cho X vào dung dịch HNO3 đặc, nóng (dư) thu được V lít khí (đktc). Giá trị của V là
A. 8,960.
B. 0,448.
C. 0,672.
D. 1,344.
Đáp án D
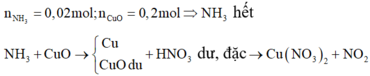
Ta thấy Cu không bị thay đổi số oxi hóa trong cả quá trình.
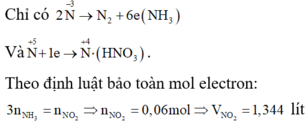
Bài 3: Cho một lượng mạt sắt dư vào 400 ml dung dịch HCl 1M, thu được khí H2.
a) Viết PTHH
b) Tính thể tích khí H2 thoát ra (đktc) và khối lượng Fe phản ứng.
c) Dẫn hết toàn bộ lượng khí H2 ở trên qua ống đựng CuO nung nóng dư, thu được 10,24 gam Cu. Tính hiệu suất của phản ứng.
a) \(n_{HCl}=0,4.1=0,4\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,4 0,2
b, \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
c, \(n_{Cu\left(tt\right)}=\dfrac{10,24}{64}=0,16\left(mol\right)\)
PTHH: H2 + CuO → Cu + H2O
Mol: 0,2 0,2
\(\Rightarrow H=\dfrac{n_{Cu\left(tt\right)}}{n_{Cu\left(lt\right)}}=\dfrac{0,16}{0,2}.100\%=80\%\)