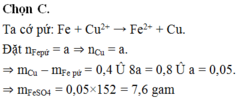Một thỏi sắt nặng 100g nhúng trong dung dịch CuSO4, sau một thời gian lọc thỏi kim loại rửa sạch , làm khô cân được 101,3g. Hỏi thỏi kim loại lúc đầu có bao nhiêu gam sắt và bao nhiêu g đồng?

Những câu hỏi liên quan
Nhúng một thanh sắt nặng 100 gam vào 100 ml dung dịch hỗn hợp gồm
C
u
N
O
3
2
0,2M và
A
g
N
O
3
0,2M. Sau một thời gian lấy thanh kim loại ra, rửa sạch làm khô cân được 101,72 gam (giả thiết các kim loại tạo thành đều bám hết vào thanh sắt). Tính khối lượng sắt đã phản ứng.
Đọc tiếp
Nhúng một thanh sắt nặng 100 gam vào 100 ml dung dịch hỗn hợp gồm C u N O 3 2 0,2M và A g N O 3 0,2M. Sau một thời gian lấy thanh kim loại ra, rửa sạch làm khô cân được 101,72 gam (giả thiết các kim loại tạo thành đều bám hết vào thanh sắt). Tính khối lượng sắt đã phản ứng.
Nhúng một thanh sắt nặng 100 gam vào 100 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và AgNO3 0,2M. Sau một thời gian lấy thanh kim loại ra, rửa sạch làm khô cân được 101,72 gam (giả thiết các kim loại tạo thành đều bám hết vào thanh sắt). Tính khối lượng sắt đã phản ứng.
Nhúng một thanh sắt nặng 100 gam vào 100 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và AgNO3 0,2M. Sau một thời gian lấy thanh kim loại ra, rửa sạch làm khô cân được 101,72 gam (giả thiết các kim loại tạo thành đều bám hết vào thanh sắt). Tính khối lượng sắt đã phản ứng.
\(\left\{{}\begin{matrix}n_{Cu\left(NO_3\right)_2}=0,2.0,1=0,02\left(mol\right)\\n_{AgNO_3}=0,2.0,1=0,02\left(mol\right)\end{matrix}\right.\)
PTHH: Fe + 2AgNO3 --> Fe(NO3)2 + 2Ag
0,01<---0,02--------->0,01---->0,02
Fe + Cu(NO3)2 --> Fe(NO3)2 + Cu
a<--------a------------->a----->a
=> 100 - 56(0,01+a) + 0,02.108 + 64a = 101,72
=> a = 0,015
=> nFe = 0,015 + 0,01 = 0,025 (mol)
=> mFe = 0,025.56 = 1,4(g)
Đúng 4
Bình luận (0)
Bài 1: Cho 28 gam bột sắt vào dung dịch CuSO4. Sau một thời gian phản ứng, lọc lấy toàn bộ lượng kim loại, rửa nhẹ, làm khô và cân nặng thì thấy khối lượng tăng 2,4 gam so với khối lượng sắt ban đầu. Đốt cháy toàn bộ lượng chất rắn trong oxi (sắt lên hóa trị III). Sản phẩm thu được tác dụng với dung dịch HCl 2M. Tính thể tích dung dịch HCl đã tham gia phản ứng.Bài 2: Để 19,6 gam sắt trong không khí thì thu được hỗn hợp A gồm Fe và 3 oxit sắt. Hòa tan hoàn toàn A trong dung dịch HNO3 loãng dư đượ...
Đọc tiếp
Bài 1: Cho 28 gam bột sắt vào dung dịch CuSO4. Sau một thời gian phản ứng, lọc lấy toàn bộ lượng kim loại, rửa nhẹ, làm khô và cân nặng thì thấy khối lượng tăng 2,4 gam so với khối lượng sắt ban đầu. Đốt cháy toàn bộ lượng chất rắn trong oxi (sắt lên hóa trị III). Sản phẩm thu được tác dụng với dung dịch HCl 2M. Tính thể tích dung dịch HCl đã tham gia phản ứng.
Bài 2: Để 19,6 gam sắt trong không khí thì thu được hỗn hợp A gồm Fe và 3 oxit sắt. Hòa tan hoàn toàn A trong dung dịch HNO3 loãng dư được 3,36 lít khi NO (đktc) và dung dich B chứa 1 muối duy nhất. Cô cạn B thì thu được 141,4 gam muối T. Xác định công thức của T và thể tích khí oxi đã tham gia phản ứng với sắt.
Ngâm một lá sắt nặng 10g vào dung dịch CuSO4, sau một thời gian lấy sắt ra khỏi dung dịch, rửa nhẹ, làm khô cân lại được 10,4g Hỏi có bao nhiêu gam đồng bám trên lá sắt biết rằng toàn bộ lượng đồng sinh ra để bám trên lá sắt Giúp mình với ạ
\(n_{CuSO_4}=x\left(mol\right)\)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
\(x.......x...................x\)
\(m_{tăng}=m_{Cu}-m_{Fe}=10.4-10=0.4\left(g\right)\)
\(\Leftrightarrow64x-56x=0.4\)
\(\Leftrightarrow x=0.05\)
\(m_{Cu}=0.05\cdot64=3.2\left(g\right)\)
Đúng 2
Bình luận (0)
Ngâm một lá Fe có khối lượng 100 gam trong 200 ml dung dịch CuSO4 0,5M một thời gian lấy lá Fe rửa sạch, sấy khô cân lại thấy nặng 100,4 gam, Giả sử toàn bộ kim loại sinh ra đều bám vào sắt. Khối lượng FeSO4 có trong dung dịch sau phản ứng là: A. 3,2 gam . B. 6,4 gam. C. 7,6 gam D. 14,2 gam.
Đọc tiếp
Ngâm một lá Fe có khối lượng 100 gam trong 200 ml dung dịch CuSO4 0,5M một thời gian lấy lá Fe rửa sạch, sấy khô cân lại thấy nặng 100,4 gam, Giả sử toàn bộ kim loại sinh ra đều bám vào sắt. Khối lượng FeSO4 có trong dung dịch sau phản ứng là:
A. 3,2 gam .
B. 6,4 gam.
C. 7,6 gam
D. 14,2 gam.
Đáp án C
nCuSO4 = 0,2. 0,5 = 0,1 (mol) ; Gọi nFe phản ứng = x (mol)
PTHH: Fe + CuSO4 → FeSO4 + Cu ↓
Theo PTHH 56x 64x
Khối lượng kim loại tăng ∆ = (64x -56x)= 8x (g)
Theo đề bài ∆m tăng = ( 100,4 -100) = 0,4 (g)
=> 8x = 0,4
=> x = 0,05 (mol)
=> mFeSO4 = 0,05. 152 = 7,6 (g)
Đúng 0
Bình luận (0)
nhúng 1 lá sắt nặng 10g vào dung dịch CuSO4 5% . Sau 1 thời gian lấy lá sắt ra rửa,sấy khô cân nặng 10,24g a) tính khối lượng của kim loại tan ra và loại bám vào b) tính khối lượng của CuSO4 cần dùng c) tính C% của dung dịch thu được
\(n_{CuSO_4}=x\left(mol\right)\)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
\(x.....x...........x........x\)
\(m_{tăng}=m_{Cu}-m_{Fe}=10.24-10=0.24\left(g\right)\)
\(\Leftrightarrow64x-56x=0.24\)
\(\Leftrightarrow x=0.03\)
\(m_{Fe\left(pư\right)}=0.03\cdot56=1.68\left(g\right)\)
\(m_{Cu}=0.03\cdot64=1.92\left(g\right)\)
\(m_{CuSO_4}=0.03\cdot160=4.8\left(g\right)\)
\(m_{dd_{CuSO_4}}=\dfrac{4.8\cdot100}{5}=96\left(g\right)\)
\(m_{\text{dung dịch sau phản ứng}}=1.68+96-1.92=95.76\left(g\right)\)
\(C\%_{FeSO_4}=\dfrac{0.03\cdot152}{95.76}\cdot100\%=4.76\%\)
Đúng 2
Bình luận (0)
Ngâm một lá Fe có khối lượng 100 gam trong 200 ml dung dịch CuSO4 0,5M một thời gian lấy lá Fe ra rửa sạch, sấy khô cân lại thấy nặng 100,4 gam. Giả sử toàn bộ kim loại sinh ra đều bám vào thanh sắt. Khối lượng FeSO4 có trong dung dịch sau phản ứng là A. 3,2 gam B. 6,4 gam C. 7,6 gam D. 14,2 gam
Đọc tiếp
Ngâm một lá Fe có khối lượng 100 gam trong 200 ml dung dịch CuSO4 0,5M một thời gian lấy lá Fe ra rửa sạch, sấy khô cân lại thấy nặng 100,4 gam. Giả sử toàn bộ kim loại sinh ra đều bám vào thanh sắt. Khối lượng FeSO4 có trong dung dịch sau phản ứng là
A. 3,2 gam
B. 6,4 gam
C. 7,6 gam
D. 14,2 gam
Đáp án C
Ta cớ pứ: Fe + Cu2+ → Fe2+ + Cu.
Đặt nFepứ = a ⇒ nCu = a.
⇒ mCu – mFe pứ = 0,4 Û 8a = 0,8 Û a = 0,05.
⇒ mFeSO4 = 0,05×152 = 7,6 gam
Đúng 0
Bình luận (0)
Ngâm một lá Fe có khối lượng 100 gam trong 200 ml dung dịch CuSO4 0,5M một thời gian lấy lá Fe ra rửa sạch, sấy khô cân lại thấy nặng 100,4 gam. Giả sử toàn bộ kim loại sinh ra đều bám vào thanh sắt. Khối lượng FeSO4 có trong dung dịch sau phản ứng là
Đọc tiếp
Ngâm một lá Fe có khối lượng 100 gam trong 200 ml dung dịch CuSO4 0,5M một thời gian lấy lá Fe ra rửa sạch, sấy khô cân lại thấy nặng 100,4 gam. Giả sử toàn bộ kim loại sinh ra đều bám vào thanh sắt. Khối lượng FeSO4 có trong dung dịch sau phản ứng là
![]()
![]()
![]()
![]()