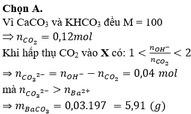Hòa tan hoàn toàn 30 gam muối CaCO3 bằng axit HCl. Hấp thụ hoàn toàn lượng khí sinh ra vào 100 ml dung dịch Ba(OH)2 aM, thu được 14,95 gam muối axit Ba(HCO3)2. Tính giá trị của a.

Những câu hỏi liên quan
Hòa tan 12 gam hỗn hợp gồm CaCO3 và KHCO3 trong dung dịch HCl dư, hấp thụ toàn bộ khí sinh ra vào 100 ml dung dịch X chứa KOH 1,2M, Ba(OH)2 0,2M và BaCl2 0,1M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là A. 5,91 B. 7,88 C. 3,94 D. 9,85
Đọc tiếp
Hòa tan 12 gam hỗn hợp gồm CaCO3 và KHCO3 trong dung dịch HCl dư, hấp thụ toàn bộ khí sinh ra vào 100 ml dung dịch X chứa KOH 1,2M, Ba(OH)2 0,2M và BaCl2 0,1M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là
A. 5,91
B. 7,88
C. 3,94
D. 9,85
Hòa tan hoàn toàn m gam hỗn hợp gồm Na2CO3, K2CO3, BaCO3 bằng dung dịch HCl dư thu được khí X và dung dịch Y. Để hấp thụ hoàn toàn khí X cần lượng tối thiểu 150 ml dung dịch Ba(OH)2 1M. Cô cạn dung dịch Y thu được 51,15 gam muối khan. Giá trị của m là A. 49,50 gam B. 58,80 gam C. 47,85 gam D. 54,825 gam
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp gồm Na2CO3, K2CO3, BaCO3 bằng dung dịch HCl dư thu được khí X và dung dịch Y. Để hấp thụ hoàn toàn khí X cần lượng tối thiểu 150 ml dung dịch Ba(OH)2 1M. Cô cạn dung dịch Y thu được 51,15 gam muối khan. Giá trị của m là
A. 49,50 gam
B. 58,80 gam
C. 47,85 gam
D. 54,825 gam
Hòa tan 12,6 gam hỗn hợp hai kim loại M (hóa trị II) và M’ (hóa trị III) bằng axit HCl dư, thu được dung dịch A và khí B. Đốt cháy hoàn toàn ½ lượng khí B trên thu được 2,79 gam H2O. a) Cô cạn dung dịch A thu được m gam hỗn hợp muối khan. Tính giá trị m. b) Cho lượng khí B còn lại phản ứng hoàn toàn với khí Cl2 vừa đủ (t0C) rồi cho sản phẩm thu được hấp thụ vào 0,2 lít dung dịch NaOH 16% (d 1,20g/ml). Tính nồng độ % các chất trong dung dịch thu được.
Đọc tiếp
Hòa tan 12,6 gam hỗn hợp hai kim loại M (hóa trị II) và M’ (hóa trị III) bằng axit HCl dư, thu được dung dịch A và khí B. Đốt cháy hoàn toàn ½ lượng khí B trên thu được 2,79 gam H2O.
a) Cô cạn dung dịch A thu được m gam hỗn hợp muối khan. Tính giá trị m.
b) Cho lượng khí B còn lại phản ứng hoàn toàn với khí Cl2 vừa đủ (t0C) rồi cho sản phẩm thu được hấp thụ vào 0,2 lít dung dịch NaOH 16% (d = 1,20g/ml). Tính nồng độ % các chất trong dung dịch thu được.
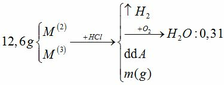
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
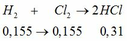
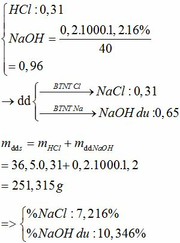
Đúng 0
Bình luận (0)
: Nung hoàn toàn 15 gam một muối cacbonat của một kim loại hóa trị II không đổi. Toàn bộ khí thoát ra cho hấp thụ hết vào 100 ml dung dịch Ba(OH)2 1M thấy thu được 9,85 gam kết tủa. Xác định công thức hóa học của muối cacbonat?
Giả sử kim loại hóa trị II là A.
Ta có: nBa(OH)2 = 0,1 (mol)
nBaCO3 = 0,05 (mol)
\(ACO_3\underrightarrow{t^o}AO+CO_2\)
- TH1: Ba(OH)2 dư.
PT: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
Theo PT: \(n_{ACO_3}=n_{CO_2}=n_{BaCO_3}=0,05\left(mol\right)\)
\(\Rightarrow M_{ACO_3}=\dfrac{15}{0,05}=300\left(g/mol\right)\Rightarrow M_A=240\left(g/mol\right)\)
→ Không có chất nào thỏa mãn.
- TH2: Ba(OH)2 hết.
PT: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
______0,05_____0,05_____0,05 (mol)
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
___0,05_____0,1 (mol)
⇒ nCO2 = 0,05 + 0,1 = 0,15 (mol)
Theo PT: \(n_{ACO_3}=n_{CO_2}=0,15\left(mol\right)\Rightarrow M_A=\dfrac{15}{0,15}=100\left(g/mol\right)\)
\(\Rightarrow M_A=40\left(g/mol\right)\)
→ A là Ca.
Vậy: CTHH cần tìm là CaCO3
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp gồm
N
a
2
C
O
3
;
K
2
C
O
3
;
B
a
C
O
3
bằng dung dịch HCl dư thu được khí X và dung dịch Y. Để hấp thụ hoàn toàn khí X cần lượng tối thiểu 150 ml dung dịch
B
a...
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp gồm N a 2 C O 3 ; K 2 C O 3 ; B a C O 3 bằng dung dịch HCl dư thu được khí X và dung dịch Y. Để hấp thụ hoàn toàn khí X cần lượng tối thiểu 150 ml dung dịch B a O H 2 1M. Cô cạn dung dịch Y thu được 51,15g muối khan. Giá trị của m là
A. 47,85
B. 58,50
C. 44,55
D. 33,80
Nung 23,2 gam hỗn hợp X gồm FeCO3 và FexOy trong không khí tới phản ứng hoàn toàn thu được khí A và 22,4 gam Fe2O3 duy nhất. Cho khí A hấp thụ hoàn toàn vào dung dịch Ba(OH)2 dư thu được 7,88 gam kết tủa. Mặt khác, để hòa tan hết 23,2 gam X cần vừa đủ V ml dung dịch HCl 2M. Công thức FexOy và giá trị của V là A. Fe3O4 và 360 B. Fe3O4 và 250 C. FeO và 200 C. FeO và 200
Đọc tiếp
Nung 23,2 gam hỗn hợp X gồm FeCO3 và FexOy trong không khí tới phản ứng hoàn toàn thu được
khí A và 22,4 gam Fe2O3 duy nhất. Cho khí A hấp thụ hoàn toàn vào dung dịch Ba(OH)2 dư thu được
7,88 gam kết tủa. Mặt khác, để hòa tan hết 23,2 gam X cần vừa đủ V ml dung dịch HCl 2M. Công thức FexOy và giá trị của V là
A. Fe3O4 và 360
B. Fe3O4 và 250
C. FeO và 200
C. FeO và 200
Đáp án A
Số mol CO2 = 0.04 -> Số mol CO3- = 0.04
=> Số mol Fe trong FeCO3=0.04
Số mol Fe2O3=0.14
=> Số mol Fe3+ = 0.28 => Số mol Fe trong FexOy = 0.24 => Số mol FexOy = 0.24/x
Từ khối lượng hỗn hợp X ta có PT: 23.2 - 0.04*116 = (56x + 16y)*0.24/x Từ đó => x/y = 3/4Thể tích
HCL = n/CM = (0.04*2 + 0.08*8)/2 = 0.36l = 360 ml
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 30g muối CaCO3 bằng axit HCl. Hấp thụ hoàn toàn lượng khí sinh ra vào 100ml dd Ba(OH)2 aM, thu được 14,95g muối axit Ba(HCO3)2. Tính giá trị của a?
TH1 : \(CO_2\left(d\text{ư}\right)\) như Azue đã làm nhé !
TH2 \(CO_2\) hết nhưng hoà tan 1 phần \(Ca\left(OH\right)_2\)
\(CO_2\left(0,3-0,06\right)+Ba\left(OH\right)_2\left(0,3-0,06\right)-->BaCO_3\left(0,06\right)+H_2O\)
\(CO_2\left(0,05\right)+BaCO_3\left(0,05\right)+H_2O-->Ba\left(HCO_3\right)_2\)
\(=>C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,24}{0,1}=2,4M\)
Đúng 0
Bình luận (3)
Theo đề bài ta có : nCaCO3 = \(\dfrac{30}{1000}=0,3\left(mol\right)\)
PTHH :
\(CaCO3+2HCl->CaCl2+CO2\uparrow+H2O\)
0,3mol.............................................0,3mol
Theo đề ta thấy : Khi cho sp khí CO2 thu được khi hòa tan CaCO3 vào dd HCl thì thu được muối axit
=> Chứng tỏ nCO2 dư sau PƯ
theo đề bài ta có : \(nBa\left(HCO3\right)2=\dfrac{14,95}{259}\approx0,06\left(mol\right)\)
PTHH :
\(2CO2+Ba\left(OH\right)2->Ba\left(HCO3\right)2\)
0,12mol.....0,06mol..............0,06mol
=> a = CMddBa(OH)2 = \(\dfrac{0,06}{0,1}=0,6\left(M\right)\)
Vậy...
Đúng 0
Bình luận (7)
Theo đề bài ta có : nCaCO3 = \(\dfrac{30}{100}=0,3\left(mol\right)\)
PTHH :
\(CaCO3+2HCl->CaCl2+CO2\uparrow+H2O\)
0,3mol..........0,6mol.............................0,3mol
Ta thấy sau khi co sp khí CO2 ở PƯ hòa tan CaCO3 tác dụng với Ba(OH)2 thì thu được muối axit
=> nCO2(dư)
Theo đề bài ta có : nBa(HCO3)2 = \(\dfrac{14,95}{259}\approx0,06\left(mol\right)\)
PTHH :
\(2CO2+Ba\left(OH\right)2->Ba\left(HCo3\right)2\)
0,12mol...........0,06mol...........0,06mol
=> a = CMddBa(HCO3)2 = \(\dfrac{0,06}{0,1}=0,6\left(l\right)\)
Đúng 0
Bình luận (10)
Cho CO dư đi qua 3,2 gam một oxit kim loại nung nóng, toàn bộ khí CO2 sinh ra hấp thụ vào 50 ml dung dịch Ba(OH)2 1M thu được 7,88 gam kết tủa. Lấy toàn bộ lượng kim loại tạo thành cho tác dụng vừa đủ với dung dịch HCl 2,99425% thu được 0,896 lít khí (đktc) và dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Thành phần % khối lượng của muối trong X gần nhất với giá trị nào sau đây? A. 4,65. B. 5,4. C. 5,65. D. 5,05.
Đọc tiếp
Cho CO dư đi qua 3,2 gam một oxit kim loại nung nóng, toàn bộ khí CO2 sinh ra hấp thụ vào 50 ml dung dịch Ba(OH)2 1M thu được 7,88 gam kết tủa. Lấy toàn bộ lượng kim loại tạo thành cho tác dụng vừa đủ với dung dịch HCl 2,99425% thu được 0,896 lít khí (đktc) và dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Thành phần % khối lượng của muối trong X gần nhất với giá trị nào sau đây?
A. 4,65.
B. 5,4.
C. 5,65.
D. 5,05.
Chọn D.
Ta có: ![]()
![]()
Khi cho Fe tác dụng với HCl thì: ![]()
![]()
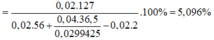
Đúng 0
Bình luận (0)
Hấp thụ hết a mol khí CO2 vào 200 ml dung dịch NaOH 1M và Ba(OH)2 0,6M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 21,67 gam kết tủa và dung dịch chứa hai muối. Giá trị của a là A. 0,33 B. 0,22 C. 0,44 D. 0,11
Đọc tiếp
Hấp thụ hết a mol khí CO2 vào 200 ml dung dịch NaOH 1M và Ba(OH)2 0,6M. Sau khi các phản ứng xảy ra hoàn toàn, thu được 21,67 gam kết tủa và dung dịch chứa hai muối. Giá trị của a là
A. 0,33
B. 0,22
C. 0,44
D. 0,11