Những câu hỏi liên quan
Một hợp chất ion tạo ra từ ion M+ và ion X2−. Trong phân tử M2X có tổng số các hạt là 140, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44. Số khối của M+ lớn hơn số khối của X2− là 23. Tổng số hạt trong M+ nhiều hơn trong X2− là 31. Tìm điện tích hạt nhân, số khối của M và X. viết công thức phân tử của hợp chất. A. K2O. B. Na2O. C. Na2S. D. Li2S.
Đọc tiếp
Một hợp chất ion tạo ra từ ion M+ và ion X2−. Trong phân tử M2X có tổng số các hạt là 140, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44. Số khối của M+ lớn hơn số khối của X2− là 23. Tổng số hạt trong M+ nhiều hơn trong X2− là 31. Tìm điện tích hạt nhân, số khối của M và X. viết công thức phân tử của hợp chất.
A. K2O.
B. Na2O.
C. Na2S.
D. Li2S.
Tổng số các hạt trong phân tử là 140 → 2ZX + NX + 2.( 2ZM + NM ) = 140 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt → 2ZX+ 2. 2ZM - NX- 2. NM = 44 (2)
Giải hệ (1), (2) → 4ZM+ 2ZX= 92, 2NM+ NX = 48
Số khối của M+ lớn hơn số khối của X2- là 23.→ ZM + NM - ( ZX + NX) = 23 (3)
Tổng số hạt trong M+ nhiều hơn trong X2- là 31 → [2.ZM + NM -1]- [2ZX + NX+2] = 31 (4)
Lấy (4) - (3) → ZM - ZX = 11
Ta có hệ
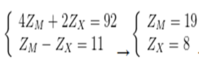
M là K và X là O
Vậy công thức là K2O.
Đáp án A.
Đúng 0
Bình luận (0)
Trong phân tử M2X có tổng số hạt là 140 , trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt . Số khối của M lớn hơn số khối của X là 23 . Tổng số hạt trong ion M+ nhiều hơn trong ion X2- là 31 hạt . Tim CTPT của M2X.
Ta có: Tổng số hạt của X: pX + nX + eX
Mà pX = eX, nên: 2pX + nX
Tổng số hạt của M: pM + nM + eM
Mà pM = eM, nên: 2pM + nM
Mà ta có 2 nguyên tử M, nên: 4pM + 2nM
Ta có: Số khối bằng: p + n
Theo đề, ta có:
2pX + nX + 4pM + 2nM = 140 (1)
(2pX + 4pM) - (nX + 2nM) = 44 (2)
(pM + nM) - (pX + nX) = 23 (3)
Từ (1), (2) và (3), ta có HPT:
\(\left\{{}\begin{matrix}2p_X+n_X+4p_M+2n_M=140\\\left(2p_X+4p_M\right)-\left(n_X+2n_X\right)=44\\\left(p_M+n_M\right)-\left(p_X+n_X\right)=23\end{matrix}\right.\)
giải ra, ta được:
pX = eX = 8 hạt.
pM = eM = 19 hạt.
=> X là oxi (O)
M là kali (K)
=> CTPT là: K2O
Đúng 1
Bình luận (0)
Trong phân tử M2X có tổng số hạt là 140 , trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt . Số khối của M lớn hơn số khối của X là 23 . Tổng số hạt trong ion M+ nhiều hơn trong ion X2- là 31 hạt . Tim CTPT của M2X.
Trong phân tử M2X có tổng số hạt là 140 , trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt . Số khối của M lớn hơn số khối của X là 23 . Tổng số hạt trong ion M+ nhiều hơn trong ion X2- là 31 hạt . Tim CTPT của M2X.
Trong phân tử
M
2
X
có tổng số hạt (proton, nơtron, electron) là 140 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion
M
+
lớn hơn số khối của ion
X
2
-
là 23. Tổng số hạt proton, nơtron, electron trong ion
M
+
nhiều hơn trong ion ...
Đọc tiếp
Trong phân tử M 2 X có tổng số hạt (proton, nơtron, electron) là 140 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion M + lớn hơn số khối của ion X 2 - là 23. Tổng số hạt proton, nơtron, electron trong ion M + nhiều hơn trong ion X 2 - là 31 hạt. Nhận xét nào sau đây không đúng?
A. M 2 X tan trong nước tạo thành dung dịch kiềm.
B. Trong các phản ứng hóa học, M chỉ thể hiện tính khử.
C. X vừa có tính oxi hóa vừa có tính khử.
D. M 2 X là hợp chất ion.
Một hợp chất M2X ( được cấu tạo từ ion M+ và X2- ). Tổng số hạt p,n,e trong phân tử M2X là 140 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44. Số khối của ion M+ lớn hơn số khối của ion X2- là 23. Tổng số hạt p,n,e trong ion M+ nhiều hơn trong ion X2- là 31 hạt
a) Viết cấu hình electron của ion M+, X2-
b) Xác định công thức phân tử M2X
Gọi các hạt trong M là p1 , e1 , n1 ( p1 = e1 )
các hạt trong X là p2 , n2 , e2 ( p2 = e2 )
\(\Sigma hatM_2X=140\)
\(\Leftrightarrow\left(2p_1+n_1\right).2+2p_2+n_2=140\)
\(\Leftrightarrow4p_1+2p_2+n_1+n_2=140\left(1\right)\)
Hạt mang điện - hạt không mang diện = 44
\(\Leftrightarrow4p_1+2p_2-n_1-n_2=44\left(2\right)\)
Số khối của ion \(M^+\) - số khôi ion \(X^{2-}\) = 23
\(\Leftrightarrow p_1+n_1-p_2-n_2=23\left(3\right)\)
Tổng hạt p,e,n trong ion \(M^+\) - tổng hạt p,n,e trong ion \(X^{2-}=31\)
\(\Leftrightarrow2p_1+n_1-1-(2p_2+n_2+2)=31\)
\(\Leftrightarrow2p_1+n_1-2p_2-n_2=34\left(4\right)\)
Ta lấy (1) + (2) => 8p1 + 4p2 = 184
(4) - (3) => p1 - p2 = 11
\(\Rightarrow\left\{{}\begin{matrix}p1=19\left(K\right)\\p2=8\left(O\right)\end{matrix}\right.\)
a) \(M^+:1s^22s^22p^63s^23p^6\)
\(X^{2-}:1s^22s^22p^6\)
b) Công thức phân tử của M2X là: \(K_2O\)
Đúng 0
Bình luận (0)
Bài 10: Một hợp chất được tạo thành từ các ion M+ và X22-. Trong phân tử M2X2 có tổng số hạt cơ bản là 164 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 52. Số khối của M lớn hơn số khối của X là 23. Tổng số hạt cơ bản trong ion M+ lớn hơn trong ion X22- là 7 hạt. Xác định CTPT M2X2
Đọc tiếp
Bài 10: Một hợp chất được tạo thành từ các ion M+ và X22-. Trong phân tử M2X2 có tổng số hạt cơ bản là 164 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 52. Số khối của M lớn hơn số khối của X là 23. Tổng số hạt cơ bản trong ion M+ lớn hơn trong ion X22- là 7 hạt. Xác định CTPT M2X2
Gọi p, e, n là số proton, số electron và số nơtron trong một nguyên tử M; p’, e’, n’ là số proton, số electron và số nơtron trong một nguyên tử X.
Trong nguyên tử số proton = số electron; các hạt mang điện là proton và electron, hạt không mang điện là nơtron.
+ Trong phân tử của M2X2 có tổng số hạt proton, nơtron và electron là 164 nên suy ra:
2(2p + n) + 2(2p’ + n’) = 164 (1)
+ Trong đó số hạt mang điện nhiều hơn hạt không mang điện là 52 nên suy ra:
(4p + 4p’) - 2(n + n’) = 52 (2)
+ Số khối của M lớn hơn số khối của X là 23 đơn vị nên ta có suy ra:
(p + n) - (p’ + n’) = 23 (3)
+ Tổng số hạt electron trong M+ nhiều hơn trong X22- là 7 hạt nên suy ra:
(2p + n - 1) - 2(2p’ + n’) + 2 = 7 (4)
Giải hệ (1), (2), (3), (4) ta được p = 19 ⇒ M là kali; p’ = 8 ⇒ X là oxi.
Công thức phân tử của hợp chất là K2O2.
*Tk
Đúng 1
Bình luận (2)
Một hợp chất ion được cấu tạo từ M+ và X2- . Trong phân tử M2X có tổng số hạt p,n,là 140 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion M+ lớn hơn số khối của ion M2- là 23 hạt. Tổng số hạt p,n,e trong ion M+ nhiều hơn trong ion M2- là 31. Viết cấu hình e của M và X .
Hợp chất A được tạo thành từ ion M+ và X2- có tổng số hạt là 116, trong A số hạt mang điện nhiều hơn số hạt không mang điện là 36. Mặt khác số khối của ion M+ nhỏ hơn số khối của ion X2- là 12. Tổng số hạt trong ion M+ ít hơn trong ion X2- là 17. Vậy A là: A. Rb2S B.Li2S C. Na2S D. K2S
Đọc tiếp
Hợp chất A được tạo thành từ ion M+ và X2- có tổng số hạt là 116, trong A số hạt mang điện nhiều hơn số hạt không mang điện là 36. Mặt khác số khối của ion M+ nhỏ hơn số khối của ion X2- là 12. Tổng số hạt trong ion M+ ít hơn trong ion X2- là 17. Vậy A là:
A. Rb2S
B.Li2S
C. Na2S
D. K2S
Cách 1
Gọi Z,N,E,Z',N',E' lần lượt là số p, n, e có trong nguyên tử M và X. Hợp chất A được tạo thành từ ion M+ và X2-.
Do đó A có dạng là
+ A có tổng số hạt là 116 nên
![]()
+ Trong A số hạt mang điện nhiều hơn số hạt không mang điện là 36:
![]()
+ Số khối của ion M+ lớn hơn số khối của ion X2- là 7:
![]()
+ Tổng số hạt trong ion M+ ít hơn trong ion X2- là 17:
![]()
Từ (1), (2), (3), (4) ta có:
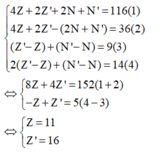
Do đó M là Na và X là S A là Na2S.
Cách 2: Từ (1) và (2) (ở Cách 1) ta có: 4Z + 2Z' = 76
Đến đây ta chỉ việc thử đáp án để nhanh chóng tìm ra đáp án không cần thiết phải xét thêm 2 dữ kiện còn lại.
Cách 3: Quan sát đáp án ta nhận thấy cả bốn đáp án đều chứa S (Z = N = 16 )
Do đó X2- là S2-. Suy ra A là M2S

Đáp án C.
Đúng 1
Bình luận (0)