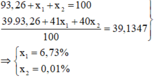Trong tự nhiên Kali có 2 đồng vị 39K và 41K. tính thành phần phần trăm về khối lượng của 39K có trong KCl, biết Cl = 35.5 và K = 39.13

Những câu hỏi liên quan
Trong tự nhiên kali gồm 3 đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của 39K trong KBr là A. 30,56%. B. 29,92%. C. 31,03%. D. 30,55%.
Đọc tiếp
Trong tự nhiên kali gồm 3 đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của 39K trong KBr là
A. 30,56%.
B. 29,92%.
C. 31,03%.
D. 30,55%.
Đáp án D
%41K = 100 - 93,26 - 0,012 = 6,728%.
Khối lượng nguyên tử trung bình của K là:
MK = 39 x 0,9326 + 40 x 0,00012 + 41 x 0,06728 = 39,13468.
Khối lượng nguyên tử trung bình của Br là:
MBr = 79,92.
Thành phần phần trăm của 39K trong KBr là
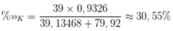
Đúng 0
Bình luận (0)
Câu 2: Trong tự nhiên kali có hai đồng vị K và K. Khối lượng nguyên tử K là 39,13. a. Xác định thành phần phần trăm của mỗi đồng vị? b. Tinh thành phần phần trăm về khối lượng của K có trong KCl
Trong tự nhiên kali có 3 đồng vị 39K (93,26%), 41K (x1%), 40K (x2%), nguyên tử khối trung bình của kali là 39,1347. Giá trị x1 và x2 lần lượt là A. 6,73% và 0,01%. B. 3,67% và 3,07%. C. 3,76% và2,98%. D. 2,89% và 3,85%.
Đọc tiếp
Trong tự nhiên kali có 3 đồng vị 39K (93,26%), 41K (x1%), 40K (x2%), nguyên tử khối trung bình của kali là 39,1347. Giá trị x1 và x2 lần lượt là
A. 6,73% và 0,01%.
B. 3,67% và 3,07%.
C. 3,76% và2,98%.
D. 2,89% và 3,85%.
Kali có 3 đồng vị: 39K, 40K và 41K. Biết số nguyên tử đồng vị 39K gấp đôi số nguyên vị 40K, số nguyên tử đồng vị 40K gấp đôi số nguyên tử 41K. Tính AK
Trong tự nhiên kali có hai đồng vị
K
19
39
và
K
19
41
. Tính thành phần phần trăm về khối lượng của
K
19
39
có trong KClO4. A. 63% B. 93,5% C. 26,3% D. 1,82%
Đọc tiếp
Trong tự nhiên kali có hai đồng vị K 19 39 và K 19 41 . Tính thành phần phần trăm về khối lượng của K 19 39 có trong KClO4.
A. 63%
B. 93,5%
C. 26,3%
D. 1,82%
Đáp án C.
Gọi phần trăm về số nguyên tử đồng vị (phần trăm về số mol) của 3919K và 4119K là x1 và x2 ta có:
x 1 + x 2 = 100 39 x 1 + 41 x 2 100 = 39 , 13 ⇒ x 1 = 93 , 5 x 2 = 6 , 5
Giả sử có 1 mol KClO4 thì tổng số mol các đồng vị của K là 1 mol, trong đó số mol 3919K là 1.0,935 =0,935 mol.
Vậy thành phần phần trăm về khối lượng của 3919K có trong KClO4 là:
% K 19 39 = 0 , 935 . 39 39 , 13 + 35 , 5 + 16 . 4 . 100 = 26 , 3 %
Đúng 0
Bình luận (0)
Trong tự nhiên có 35 Cl và 37 Cl. Khối lượng của 1 lít khí clo ở đktc là 3,17g.
a,Tính thành phần phần trăm về số nguyên tử từng đồng vị trong tự nhiên.
b,Tính số nguyên tử 37 Cl có trong 1 lít khí clo (đktc)
c,Tính thành phần phần trăm về khối lượng của đồng vị 35 Cl trong KClO.
( biết K=39, O=16)
Clo trong tự nhiên có 2 đồng vị là 35 Cl và 37 Cl. Biết nguyên tử khối trung bình của Na và Cl lần lượt là 23 và 35,5. Tính phần trăm về khối lượng của 35 Cl trong NaCl.
Gọi phần trăm đồng vị của 35Cl là x
⇒ Phần trăm đồng vị của 37Cl là 100-x
Ta có: \(A=\dfrac{35x+37\left(100-x\right)}{100}=35,5\Rightarrow x=75\%\)
Phần trăm k/lg của 35Cl trong NaCl là:\(\dfrac{35.75\%}{23+35,5}.100\%=44,87\%\)
Đúng 2
Bình luận (1)
Trong tự nhiên chlorine (Cl) có hai đồng vị bền là 35Cl và 37Cl. Biết nguyên tử khối trung bình của Cl là 35,5 và thành phần phần trăm khối lượng của đồng vị 37Cl trong KClOx là 6,678%. Cho nguyên tử khối trung bình của K và O lần lượt là 39 và 16, xem nguyên tử khối mỗi đồng vị có giá trị bằng số khối. Tính giá trị của x?
Giả sử: %35Cl trong tự nhiên là a.
⇒ %37Cl trong tự nhiên là 100 - a
Ta có: \(\dfrac{35.a+37.\left(100-a\right)}{100}=35,5\Rightarrow a=75\%=\%^{35}Cl\)
⇒ %37Cl = 25%
Mà: %37Cl trong KClOx là 6,678%
\(\Rightarrow\dfrac{25\%.37}{25\%.37+75\%.35+39+16x}=0,6678\)
\(\Rightarrow x=4\)
Đúng 3
Bình luận (0)
Trong tự nhiên Cl tồn tại chủ yếu ở 2 đồng vị 37Cl và 35Cl, có khối lượng mol trung bình là 35,45. Thành phần phần trăm về khối lượng của 35Cl trong CaOCl2 là (Cho O: 16, Ca: 40) A. 43,30%. B. 56,70%. C. 42,75%. D. 41,40%.
Đọc tiếp
Trong tự nhiên Cl tồn tại chủ yếu ở 2 đồng vị 37Cl và 35Cl, có khối lượng mol trung bình là 35,45. Thành phần phần trăm về khối lượng của 35Cl trong CaOCl2 là (Cho O: 16, Ca: 40)
A. 43,30%.
B. 56,70%.
C. 42,75%.
D. 41,40%.
Đáp án C
Gọi x là phần trăm số nguyên tử 35Cl => Phần trăm số nguyên tử 37Cl là (100 – x)

Đúng 0
Bình luận (0)