6. Cho 11,2 gam kim loại sắt tác dụng với axit H2SO4 đặc nóng, thu được bao nhiêu lít khí SO2 (đktc). Biết trong quá trình thu khí hao hụt mất 3%.

Những câu hỏi liên quan
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp
Cho 11,2 gam hỗn hợp X gồm Cu và kim loại M tác dụng với dung dịch H2SO4 loãng dư, thu được 3,136 lít khí H2. Cũng lượng hỗn hợp X như vậy cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít (đktc) khí SO2 (sản phẩm khử duy nhất ). Xác định kim loại M
TH1: Hóa trị `M` đổi `->M:\ Fe`
`Fe^0->Fe^{+2}+2e`
`2H^{-1}+2e->H_2^0`
Bảo toàn electron: `n_{Fe}=n_{H_2}=0,14(mol)`
`->n_{Cu}={11,2-0,14.56}/{64}=0,0525(mol)`
`Cu^0->Cu^{+2}+2e`
`Fe^0->Fe^{+3}+3e`
`S^{+6}+2e->S^{+4}`
Bảo toàn electron: `2n_{Cu}+3n_{Fe}=2n_{SO_2}=0,525`
`->2.0,0525+3.0,14=0,525`
Nhận.
`->M` là Iron `(Fe).`
TH2: Hóa trị `M` không đổi.
`M` hóa trị `n`
Đặt `n_{Cu}=x(mol);n_M=y(mol)`
`M^0->M^{+n}+n.e`
`2H^{-1}+2e->H_2^0`
Bảo toàn electron: `ny=2n_{H_2}=0,28`
`->y={0,28}/n(mol)`
`M^0->M^{+n}+n.e`
`Cu^0->Cu^{+2}+2e`
`S^{+6}+2e->S^{+4}`
Bảo toàn electron: `2x+ny=2n_{SO_2}=0,525`
`->x={0,525-0,28}/2=0,1225(mol)`
`->m_M=11,2-0,1225.64=3,36(g)`
`->M_M={3,36}/{{0,28}/n}=12n`
`->n=2;M_M=24`
`->M` là magnesium `(Mg).`
Vậy `M` là `Mg` hoặc `Fe.`
Đúng 2
Bình luận (0)
Cho 19,2 gam một kim loại M tác dụng hết với dung dịch H2SO4 đặc nóng thu được 6,72 lít khí SO2 duy nhất (đktc). Kim loại M là
A. Sắt.
B. Kẽm.
C. Magie.
D. Đồng.
Đáp án D
Số mol các chất là:
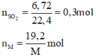
Gọi hoá trị của M là n
Sơ đồ phản ứng: M 0 + H 2 S + 6 2 O 4 ( đặc ) → M + N 2 ( SO 4 ) n + S + 4 O 2 + H 2 O
Các quá trình nhường, nhận electron:
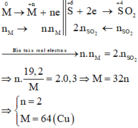
Đúng 0
Bình luận (0)
Cho 11,2g kim loại X tác dụng hết với H2SO4 đặc, nóng thu được 6,72 lít khí SO2 (đktc). Tên kim loại là:
A. đồng
B. sắt
C. kẽm
D. nhôm
Đáp án B
Gọi hóa trị của kim loại là a.
nSO2 = 0,3 mol
Bảo toàn e: nX.a = 2. nSO2
=> nX = 0,6/a
Mặt khác mX = 11,2 => MX = 56a/3
Với a = 3 MX = 56 (Fe)
Đúng 0
Bình luận (0)
Cho 18,2 gam hỗn hợp các kim loại Fe, Cr, Cu tác dụng với lượng dư dung dịch
H
2
SO
4
loãng, nóng trong điều kiện không có không khí thu được dd Y và chất rắn Z cùng 5,6 lít
H
2
(đktc). Nếu cho 18,2 gam X tác dụng với lượng dư dd
H
2
SO
4
đặc, nguội thu được 1,68 lít khí
SO
2...
Đọc tiếp
Cho 18,2 gam hỗn hợp các kim loại Fe, Cr, Cu tác dụng với lượng dư dung dịch H 2 SO 4 loãng, nóng trong điều kiện không có không khí thu được dd Y và chất rắn Z cùng 5,6 lít H 2 (đktc). Nếu cho 18,2 gam X tác dụng với lượng dư dd H 2 SO 4 đặc, nguội thu được 1,68 lít khí SO 2 (đktc). Tính thành phần phần trăm crom trong hỗn hợp?
A. 42,86%
B. 52%
C. 26,37%
D. 43%.
Cho m gam hỗn hợp 2 kim loại Al và Cu chia làm 2 phần bằng nhau :- Phần 1 : Cho tác dụng với dung dịch
H
2
SO
4
loãng, dư thu được 1,344 lít khí
H
2
(đktc).- Phần 2 : Cho tác dụng với dung dịch
H
2
SO...
Đọc tiếp
Cho m gam hỗn hợp 2 kim loại Al và Cu chia làm 2 phần bằng nhau :
- Phần 1 : Cho tác dụng với dung dịch H 2 SO 4 loãng, dư thu được 1,344 lít khí H 2 (đktc).
- Phần 2 : Cho tác dụng với dung dịch H 2 SO 4 đặc nóng, dư, thu được 2,24 lít khí SO 2 (đktc) .Xác định giá trị của m.
Các PTHH :
2Al + 3 H 2 SO 4 → Al 2 SO 4 3 + 3 H 2 (1)
2Al + 6 H 2 SO 4 → Al 2 SO 4 3 + 3 SO 2 + 6 H 2 O (2)
Cu + 2 H 2 SO 4 → Cu SO 4 + 2 H 2 O + SO 2 (3)
Theo PTHH (1) số mol Al tham gia phản ứng bằng 2/3 số mol H 2 => Khối lượng AI trong hỗn hợp : 2×2/3×0,06×27 = 2,16(g)
Số mol SO 2 được giải phóng bởi Al: 2,16/27 x 3/2 = 0,12 mol
Theo PTHH (2) và (3) số mol SO 2 giải phóng bởi Cu : 2.0,1 - 0,12 = 0,08 (mol)
Theo PTHH (3) khối lượng Cu trong hỗn hợp : 0,08. 64 = 5,12 (g)
Vậy m = 2,16 + 5,12 = 7,28 (g).
Đúng 0
Bình luận (0)
Cho m gam kim loại Cu tác dụng với dung dịch H2SO4 đặc nóng, dư thu được 5,6 lít khí SO2 (đktc). Tính giá trị của m.
A. 16 gam
B. 17 gam.
C. 18 gam.
D. 19 gam.
\(Cu+2H_2SO_4 \to CuSO_4+SO_2+2H_2O\\ n_{SO_2}=\frac{5,6}{22,4}=0,25(mol)\\ n_{Cu}=n_{SO_2}=0,25(mol)\\ m_{Cu}=0,25.64=16(g)\\ \to A\)
Đúng 2
Bình luận (0)












