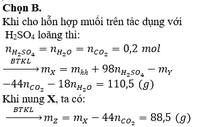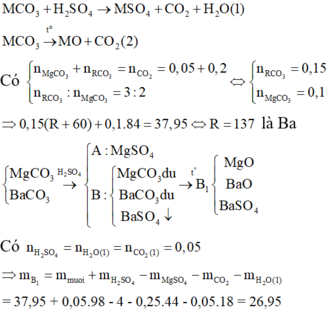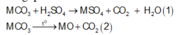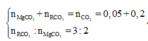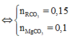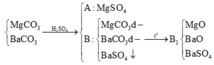hòa tan 115.3g hỗn họp MgCO3 và RCO3 bằng 500 ml dd H2SO4 loãng ta thu được dd A, chất rắn B và 4.48l khí CO2(dktc). Cô cạn dd A thu dc 12g muối khan. mặt khác đem nung chất rắn B tới khối lượng không đổi thì thu dc 11.2lit CO2(dktc) và chất rắn D. tính nồng độ mol/lit của dd H2SO4 loãng đã dùng.
khối lượng của B,D?
Xac dinh R? Biet trong X so mol RCO3 gap 2,5 lan so mol MgCO3