Cân =
SO2 + O2 ---> SO3
Chọn hệ số thích hợp để cân bằng phản ứng hóa học sau:
S O 2 + O 2 − t o → S O 3
Cho cân bằng: 2SO2 + O2 <=>SO3 ∆ H < 0. Cho một số yếu tố:
(1) Tăng áp suất ;
(2)Tăng nhiệt độ ;
(3) Tăng nồng độ O2 và SO2 ;
(4)Tăng nồng độ SO3;
(5) Tăng xúc tác;
Các yếu tố làm tăng hiệu xuất của p/ứ trên là :
A. (2),(4),(5)
B. (1),(3),(5)
C. (2),(5),(1).
D. (3),(5),(4)
Chọn đáp án B
2SO2 + O2 ⇄ SO3 ∆ H < 0. Đây là phản ứng thuận tỏa nhiệt hay nghịch thu nhiệt.
Muốn tăng hiệu suất ta phải làm cho cân bằng dịch sang phải.Do đó phải :
Giảm nhiệt độ (loại 2)
Giảm nồng độ SO3 (loại 4)
Tăng nồng độ O2 và SO2
Tăng xúc tác thật ra yếu tố này không cần thiết vì chất xúc tác không thay đổi trong quá trình phản ứng
Xét các cân bằng sau:
2SO2(k) + O2(k) ⇌ 2SO3(k) (1)
SO2(k) + 1/2 O2(k) ⇌ SO3(k) (2)
2SO3(k) ⇌ 2SO2(k) + O2 (3)
Gọi K1, K2, K3 là hằng số cân bằng ứng với các cân bằng (1), (2), (3) thì biểu thức liên hệ giữa chúng là:
A. K1= K2=( K3)-1.
B . K1=( K2)2=( K3)-1.
C. K1= K2= K3.
D. K1=2 K2=( K3)-1.
Cho phản ứng sau: 2 S O 2 ( k ) + O 2 ( k ) ⇆ k n k t 2 S O 3 ( k )
Ở t o C nồng độ cân bằng các chất: [ S O 2 ] = 0 , 2 M ; [ O 2 ] = 0 , 1 M ; [ S O 3 ] = 1 , 8 M
Tốc độ của phản ứng thuận tại t°C là
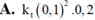
![]()
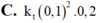
![]()
Câu 14: Axit sunfuric được sản xuất theo quy trình sau:
S + X à Y
Y + X à Z
Z + H2O à H2SO4
X, Y, Z lần lượt là:
A. SO3, H2, O2 . B. O2, SO2, SO3
C. H2, O2, SO2 D. SO2, SO3, O2
Câu 15: Chỉ dùng dung dịch BaCl2 có thể phân biệt được 2 dung dịch củng nồng độ nào sau đây?
A. HCl và HNO3 B. K2SO4 và K2CO3
C. HCl và H2SO4 D. H2SO4 và H2SO3
Câu 1: Có những chất sau: HCl, NaOH, CO2, các cặp chất có thể phản ứng với nhau là: A. 2. B. 3. C. 4. D.5
Em cần lời giải chi tiết ạ
Z tác dụng nước tạo H2SO4 => Z: SO3
Mà: Y tác dụng X ra SO3 và S tác dụng X ra Y => X: O2 , Y: SO2
=> Chọn B
Trong công nghiệp sản xuất H2SO4, giai đoạn oxi hóa SO2 thành SO3, được biểu diễn bằng phương trình phản ứng:
2 S O 2 ( K ) + O 2 ( K ) ⇆ V 2 O 5 , t o 2 S O 3 ( K ) , △ H < 0
Cân bằng hóa học sẽ chuyển dời về phía tạo ra sản phẩm là SO3, nếu
A. tăng nồng độ khí O2 và tăng áp suất
B. giảm nồng độ khí O2 và giảm áp suất
C. tăng nhiệt độ và giảm áp suất
D. giảm nhiệt độ và giảm nồng độ khí SO2
Cân bằng hóa học chuyển dời về phía tạo ra sản phẩm là SO3, có nghĩa cân bằng chuyển dịch về chiều thuận. Các yếu tố có thể làm điều đó là:
- Tăng nồng độ SO2 hoặc O2
- Giảm nồng độ SO3
- Tăng áp suất nt > ns
- Giảm nhiệt độ
Cho 4,48l khí SO2 tác dụng với 2,24l khí O2 theo phương trình hoá học
SO2 + O2 --V2O5->,tO SO3
Sau khi phản ứng kết thúc ta thu được 5,6ℓ hỗn hợp khí gồm SO2, O2, SO3.
a. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứng
b. Tính hiệu suất của phản ứng
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{hh}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Gọi \(n_{SO_3}=a\left(mol\right)\)
PTHH: 2SO2 + O2 --to--> 2SO3
a <----- 0,5a <--- a
\(\rightarrow0,2-a+0,1-a+a=0,25\Leftrightarrow a=0,05\left(mol\right)\)
\(\rightarrow\left\{{}\begin{matrix}V_{O_2}=\left(0,1-0,05\right).22,4=1,12\left(l\right)\\V_{SO_2}=\left(0,2-0,05\right).22,4=3,36\left(l\right)\\V_{SO_3}=0,05.22,4=1,12\left(l\right)\end{matrix}\right.\)
\(H=\dfrac{0,05}{0,2}=25\%\)
Câu V.
1. Cho 4,48l khí SO2 tác dụng với 2,24l khí O2 theo phương trình hoá học
SO2 + O2![]() SO3
SO3
Sau khi phản ứng kết thúc ta thu được 5,6ℓ hỗn hợp khí gồm SO2, O2, SO3.
a. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứng
b. Tính hiệu suất của phản ứng
2. Cho 7,2g Mg tác dụng với 2,24l khí O2 sau phản ứng kết thúc thu được hỗn hợp chất rắn A. Hoà tan A bằng 100g dung dịch HCl 29,2% thì thu được dung dịch B và khí C.
a. Viết các phương trình hoá học xảy ra
b. Tính thể tích khí C
c. Tính C% của các chất có trong dung dịch B.
Các khí đều được đo ở điều kiện tiêu chuẩn
Ai giúp mình làm bài tập dạng này với :((
VD: S ---> SO2 ---> SO3 ---> H2SO4 ---> FeSO4
S + O2 ---> SO2
2SO2 + O2 ---> SO3
SO3 + H2O ---> H2SO4
H2SO4 + FeO ---> FeSO4 + H2O
de dau ban cho cai vd lam j
Xét phản ứng: SO 2 ( k ) + O 2 ( k ) ⇌ SO 3 ( k ) ; ( ∆ H < 0 ) . Để thu được nhiều SO 3 ta cần
A. thêm xúc tác
B. giảm áp suất
C. tăng nhiệt độ
D. giảm nhiệt độ