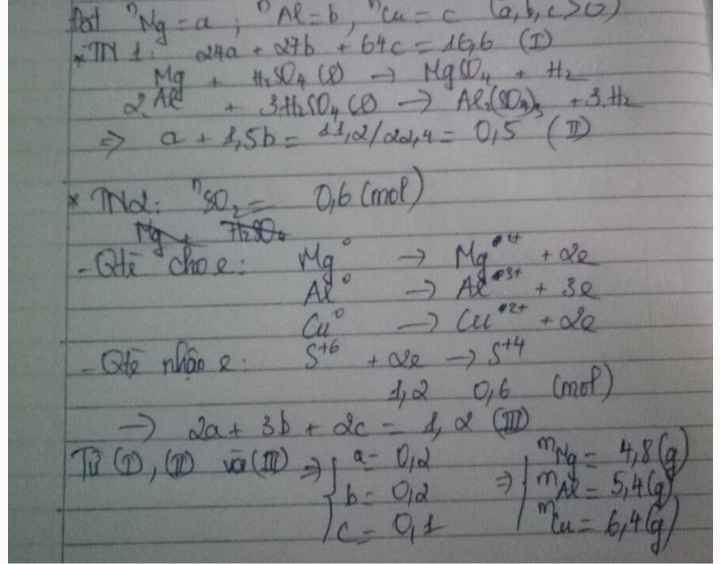cho mg hh X gồm mg và fe tác dụng với dd HCL dư thu được 8,96 lít khí nếu cho mg hh X tác dụng với dd H2So4 đặc nóng dư thì thu được 11,2 lít khí So2. viết các phương trình hóa học xãy ra và tính ra

Những câu hỏi liên quan
41. Hoà tan 24,8g hh X gồm Fe, Mg, Cu trong dd H2SO4 đặc, nóng dư thu được dd A. Cô cạn dd A thu được 132 g muối khan. Nếu cho 24,8 g X tác dụng với dd HCl dư thu được 11,2 lít khí (đkc).
a. Viết phương trình phản ứng b. Tính % khối lượng mỗi kim loại trong hh X.
Gọi x, y, z là số mol Fe, Mg, Cu
=> \(56x+24y+64z=24,8\) (1)
X+ H2SO4 đặc nóng
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Mg + 2H2SO4→ MgSO4 + SO2↑ + 2H2O.
Cu + 2H2SO4→ CuSO4 + SO2↑ + 2H2O.
Các muối là \(Fe_2\left(SO_4\right)_3,MgSO_4,CuSO_4\)
=> \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{n_{Fe}}{2}=\dfrac{x.}{2};n_{MgCl_2}=n_{Mg}=y;n_{CuCl_2}=n_{Cu}=z\)
=> \(\dfrac{400x}{2}+120y+160z=132\) (2)
X + HCl dư thu được khí là H2
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
=> x+y=0,5 (mol) (3)
Từ (1), (2), (3) => x, y ,z
Xem lại đề vì hệ vô nghiệm
Đúng 2
Bình luận (1)
Hòa tan hết 17.44g hh gồm Fe, Fe2o3, CuO ,Cu ,Mg bằng dd H2SO4 đặc nóng sau pứ thu dc dd y và 2.464 lít khí SO2 dktc cho dd y tác dụng với NaOH dư, lọc kết tủa đem nung trong không khí đến khối lượng ko đổi thì dc m g chất rắn. tính m GIẢI CHI TIẾT GIÚP EM VỚI Ạ !
Xem chi tiết
Cho 13,2g hh Mg và Fe tác dụng với lượng dư dd HCl,sau phản ứng thu được dd X và 7,84 lít khí H2( đktc)
a) Viết phương trình phản ứng xảy ra và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
b) Cô cạn dung dịch X thu được m gam muối khan.Tính m
mn giúp em với
Xem chi tiết
nH2= 0,35(mol)
a) PTHH: Mg + 2 HCl -> MgCl2 + H2
x_________2x_______x______x(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
y________2y________y_____y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}24x+56y=13,2\\x+y=0,35\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
b) m=m(muối khan)= mMgCl2 + mFeCl2= 95.x+127y=95.0,2+127.0,15= 38,05(g)
Đúng 1
Bình luận (0)
a)
Gọi
\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 13,2(1)\)
\(Mg + 2HCl \to MgCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\)
Theo PTHH : \(n_{H_2} = a + b = 0,35(mol)\)(2)
Từ (1)(2) suy ra a = 0,15 ;b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,15.56}{13,2}.100\% = 63,64\%\\ \Rightarrow m_{Mg} = 100\% - 63,64\% = 36,36\%\)
b)
Ta có :\(n_{HCl} = 2n_{H_2} = 0,7(mol)\)
Bảo toàn khối lượng :
\(m_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 13,2 + 0,7.36,5 - 0,35.2=38,05(gam)\)
Đúng 1
Bình luận (0)
Cho 13,2g hh Mg và Fe tác dụng với lượng dư dd HCl,sau phản ứng thu được dd X và 8,6765
lít khí H2( đktc) a) Viết phương trình phản ứng xảy ra và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu b) Cô cạn dung dịch X thu được m gam muối khan.Tính mSửa đề: đktc → đkc
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: 24nMg + 56nFe = 13,2 (1)
\(n_{H_2}=\dfrac{8,6765}{24,79}=0,35\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}+n_{Fe}=0,35\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,2.24}{13,2}.100\%\approx36,36\%\\\%m_{Fe}\approx63,64\%\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
⇒ m muối khan = 0,2.95 + 0,15.127 = 38,05 (g)
Đúng 2
Bình luận (0)
Cho 8g hh Fe và Mg tác dụng hoàn toàn với dd HCl dư thu được 4,48 lít khí dư (đktc). Tính thành phần % đúng với tỉ lệ của các chất ban đầu.
Hh X gồm Fe,Cu,Ag.Chia 110,4g X thành 3 phần bằng nhau.Cho phần 1 tác dụng với Cl2 dư,thu đc m gam chất rắn.Phần 2 cho tác dụng với dd H2SO4 loãng dư thu được 2,24 lít khí H2 đktc.Hòa tan phần 3 trong 120g dd H2SO4 98% đun nóng thu được dd Y và 8,96 lít khí SO2 đktc a)Tính m b)Tính C% các chất trong dd Y
Hh X gồm Fe,Cu,Ag.Chia 110,4g X thành 3 phần bằng nhau.Cho phần 1 tác dụng với Cl2 dư,thu đc m gam chất rắn.Phần 2 cho tác dụng với dd H2SO4 loãng dư thu được 2,24 lít khí H2 đktc.Hòa tan phần 3 trong 120g dd H2SO4 98% đun nóng thu được dd Y và 8,96 lít khí SO2 đktc a)Tính m b)Tính C% các chất trong dd Y
Cho 16,6 gam hh X gồm Al,Cu,Mg tác dụng vs H2SO4 loãng dưthu đc 11,2 lít khí .còn nếu cho 16,6g hỗn hợp trên tác dụng vs dd H2SO4 đặc,to dư thì giải phóng 13,44 lít khí .Tính khối lượng mỗi kim loại
hỗn hợp x gồm 2 kim loại Mg và R-thí nghiệm 1: cho 8 gam hỗn hợp x vào dd hcl dư thu được 4,48 lít khí ở đktc -thí nghiệm 2: cho 16 gam hỗn hợp X tác dụng với dd h2so4 đặc, nóng, dư thu được một khí z sản phẩm khử duy nhất không màu mùi hắc. khí z này được hấp thụ hoàn toàn vào 450 ml dd 2M thu được 75,2 gam muối kali.1 viết các pthh xảy ra và tính số mol khí z. các pu xảy ra hoàn toàn2. xác định R
Đọc tiếp
hỗn hợp x gồm 2 kim loại Mg và R
-thí nghiệm 1: cho 8 gam hỗn hợp x vào dd hcl dư thu được 4,48 lít khí ở đktc -thí nghiệm 2: cho 16 gam hỗn hợp X tác dụng với dd h2so4 đặc, nóng, dư thu được một khí z sản phẩm khử duy nhất không màu mùi hắc. khí z này được hấp thụ hoàn toàn vào 450 ml dd 2M thu được 75,2 gam muối kali.
1 viết các pthh xảy ra và tính số mol khí z. các pu xảy ra hoàn toàn
2. xác định R